预约演示
更新于:2025-05-07
Beijing Novotel Biotechnology Co., Ltd.
北京诺博特生物科技有限公司|私营公司|2016|中国北京市
北京诺博特生物科技有限公司|私营公司|2016|中国北京市
更新于:2025-05-07
概览
标签
内分泌与代谢疾病
神经系统疾病
心血管疾病
合成多肽
重组多肽
小分子化药
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 小分子化药 | 1 |
| 生物类似药 | 1 |
| 重组多肽 | 1 |
| 合成多肽 | 1 |
| 排名前五的靶点 | 数量 |
|---|---|
| GLP-1R(胰高血糖素样肽-1受体) | 2 |
| SCNA(电压门控钠通道α亚基家族) | 1 |
关联
5
项与 北京诺博特生物科技有限公司 相关的药物靶点 |
作用机制 SCNA阻滞剂 |
在研机构 |
原研机构 |
最高研发阶段临床3期 |
首次获批国家/地区 美国 |
首次获批日期2005-06-23 |
靶点 |
作用机制 GLP-1R激动剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
作用机制 透明质酸调节剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床申请批准 |
首次获批国家/地区- |
首次获批日期- |
5
项与 北京诺博特生物科技有限公司 相关的临床试验CTR20251508
在肥胖受试者中评价司美格鲁肽注射液与Wegovy®的疗效和安全性:一项多中心、随机、开放、平行对照Ⅲ期临床研究
主要目的:评价司美格鲁肽注射液与Wegovy®在肥胖受试者中减重的疗效相似性。
次要目的:评价司美格鲁肽注射液与Wegovy®在肥胖受试者中的安全性。
开始日期- |
申办/合作机构  北京质肽生物医药科技有限公司 北京质肽生物医药科技有限公司 [+1] |
CTR20230095
利多卡因丁卡因乳膏用于成人浅层皮肤手术前对完整皮肤的局部麻醉有效性及安全性随机、阳性药自身对照、双盲、多中心、等效性临床研究
以原研药 PLIAGLIS ®为阳性对照,通过随机、双盲、自身对照的临床试验,验证试验药物利多卡因丁卡因乳膏用于成人浅层皮肤手术前对完整皮肤局部麻醉的有效性。 通过实验室检查、临床症状、体征、不良事件等,验证利多卡因丁卡因乳膏的安全性。
开始日期2023-03-29 |
申办/合作机构  山东良福制药有限公司 山东良福制药有限公司 [+1] |
CTR20210968
在健康受试者中比较利拉鲁肽注射液和诺和力®的随机、开放、单剂量、双交叉Ⅰ期临床研究
主要研究目的:本研究以北京诺博特生物科技有限公司生产的利拉鲁肽注射液(3ml:18mg)为受试制剂(T),以原研厂家丹麦诺和诺德公司生产的利拉鲁肽注射液(3ml:18mg,商品名:诺和力®)为参比制剂(R),评价受试制剂(T)和参比制剂(R)药代动力学的相似性。
次要研究目的:观察受试制剂(T)和参比制剂(R)在健康受试者中的安全性和免疫原性。
开始日期2021-07-16 |
申办/合作机构 |
100 项与 北京诺博特生物科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 北京诺博特生物科技有限公司 相关的专利(医药)
登录后查看更多信息
11
项与 北京诺博特生物科技有限公司 相关的新闻(医药)2024-12-05
·氨基观察
氨基观察-创新药组原创出品
作者 | 黄凯
多个重磅药物迎来新进展。
12月4日,Merus宣布,FDA已加速批准HER2/HER3双抗Bizengri上市,用于治疗携带NRG1基因融合的晚期不可切除或转移性胰腺导管腺癌或非小细胞肺癌成年患者,这些患者在接受既往全身治疗后出现疾病进展。新闻稿指出,这是美国FDA批准的首款治疗这一患者群体的靶向疗法。
同时,也是FDA批准了阿斯利康的PD-L1抑制剂度伐利尤单抗,用于治疗在接受同步含铂化疗和放疗后疾病未进展的局限期小细胞肺癌成人患者。这是40年来LS-SCLC治疗迎来的突破。
翰宇药业签订GLP-1合同。
12月5日,翰宇药业公告,公司与DS3签订《产品供应协议》,DS3拟向公司采购价约1400万美元(折合人民币约1.02亿元)的GLP-1原料药。
在过去的一天里,国内外医药市场还有哪些热点值得关注?让氨基君带你一探究竟。
/ 01 /
市场速递
1)翰宇药业与DS3签订1.02亿元GLP-1原料药供应协议
12月5日,翰宇药业公告,公司与DS3签订《产品供应协议》,DS3拟向公司采购价约1400万美元(折合人民币约1.02亿元)的GLP-1原料药。
2)智飞生物与GSK签署了《独家经销和联合推广协议补充协议》
12月5日,智飞生物公告,公司与葛兰素史克生物、葛兰素史克香港签署了《独家经销和联合推广协议补充协议》,优化调整了2023年10月8日签署的原《独家经销和联合推广协议》中约定的重组带状疱疹疫苗采购计划的相关条款,并进一步拓展了公司在中国大陆地区拥有独家进口、分销和共同推广重组带状疱疹疫苗的权利期限。此外,补充协议还进一步明确公司将与GSK独家探索并积极促成在中国大陆地区初步为期10年的呼吸道合胞病毒(RSV)疫苗商业化合作。
/ 02 /
资本信息
1)凯德维斯完成近2亿元B轮融资
12月5日,武汉凯德维斯生物宣布完成近2亿元B轮融资,本轮资金将用于公司在妇科肿瘤诊疗领域各产品的临床开发和市场拓展。
/ 03 /
医药动态
1)香雪生命TAEST16001注射液获临床许可
12月5日,据CDE官网,香雪生命TAEST16001注射液获临床许可,拟用于治疗基因型为HLA-A*02:01,肿瘤抗原NY-ESO-1表达为阳性的晚期食管癌。
2)兆科药业重组安菲博肽注射液获临床许可
12月5日,据CDE官网,兆科药业重组安菲博肽注射液获临床许可,拟用于进行机械取栓的急性缺血性脑卒中成年患者。
3)民为生物MWN109注射液获临床许可
12月5日,据CDE官网,民为生物MWN109注射液获临床许可,拟开展治疗代谢功能障碍相关脂肪性肝炎(MASH)的研究。
4)再鼎医药ZL-1102凝胶获临床许可
12月5日,据CDE官网,再鼎医药ZL-1102凝胶获临床许可,拟用于局部治疗慢性斑块状银屑病。
5)诺博特生物重组人透明质酸酶注射液获临床许可
12月5日,据CDE官网,诺博特生物重组人透明质酸酶注射液获临床许可,拟用于促进皮下输液的扩散以替代静脉输液。
/ 04 /
器械跟踪
1)联影医疗磁共振成像系统获注册许可
12月5日,据NMPA官网,联影医疗磁共振成像系统获注册许可。
2)三坛医疗脊柱外科手术导航定位系统获注册许可
12月5日,据NMPA官网,三坛医疗脊柱外科手术导航定位系统获注册许可。
3)大博医疗脊柱椎间融合器获注册许可
12月5日,据NMPA官网,大博医疗脊柱椎间融合器获注册许可。
/ 05 /
数字医疗日报
1)华科精准脑外科手术计划软件获注册许可
12月5日,据NMPA官网,华科精准脑外科手术计划软件获注册许可。
/ 06 /
海外药闻
1)阿斯利康PD-L1获FDA批准治疗局限期小细胞肺癌
日前,美国FDA批准了阿斯利康的PD-L1抑制剂度伐利尤单抗(durvalumab)用于治疗在接受同步含铂化疗和放疗后疾病未进展的局限期小细胞肺癌(LS-SCLC)成人患者。这是40年来LS-SCLC治疗迎来的突破。
2)RNA疗法新锐与GSK达成战略合作
12月5日,Rgenta Therapeutics宣布,与葛兰素史克签订一项多年期多靶点的战略研究合作协议,旨在推进新型靶向RNA小分子剪接调节剂在肿瘤等多个疾病领域的发现和开发。
3)FDA加速批准HER2/HER3双抗上市
12月4日,Merus宣布,FDA已加速批准Bizengri上市,用于治疗携带NRG1基因融合(NRG1+)的晚期不可切除或转移性胰腺导管腺癌或非小细胞肺癌成年患者,这些患者在接受既往全身治疗后出现疾病进展。新闻稿指出,这是美国FDA批准的首款治疗这一患者群体的靶向疗法。
PS:欢迎扫描下方二维码,添加氨基君微信号交流。
加速审批疫苗上市批准
2024-10-15
2024年10月12日,由质肽生物与爱美客技术发展股份有限公司全资子公司北京诺博特生物科技有限公司合作开发的司美格鲁肽注射液(体重管理适应症),获得国家药品监督管理局药品审评中心(CDE)临床试验默示许可。
(图源:国家药品监督管理局药品审评中心)
关于司美格鲁肽注射液(Wegovy®)
质肽生物 司美格鲁肽 肥胖
临床申请申请上市
2024-05-22
·赛柏蓝
编者按:本文来自新康界;赛柏蓝授权转载,编辑相宜国家药监局发布2024年05月21日药品批准证明文件送达信息,共有66个受理号获批,全部均为报产获批、视同通过一致性评价的产品。其中,涉及礼来苏州制药有限公司的3品规替尔泊肽注射液等。消息一出,立即引起了医药圈的高度关注。因为这意味着,网红“减肥神药”司美格鲁肽在中国迎来了强劲的对手,同时也预示着国内减重药物市场的竞争在快速升级。01替尔泊肽不同剂量平均减重5kg、7kg在药监局发布获批文件的当天,礼来官网也发布了替尔泊肽注射液相应文章。礼来相关负责人表示,该药能够直接和间接地作用于多种导致T2DM病理生理缺陷的器官与组织,可在胰岛β细胞等核心致病组织中发挥更强疗效。同时,替尔泊肽注射液潜在直接作用于脂肪组织,降低脂肪含量,增加胰岛素敏感性,进一步带来强效降糖等临床综合获益。来源:礼来中国官网据悉,本次获批主要基于在T2DM患者中开展的全球关键III期注册试验SURPASS 1-5及亚太地区关键III期注册试验SURPASS-AP-Combo(83.4%的受试者为中国患者)。其中,SURPASS-AP-Combo12纳入的T2DM患者基线平均糖尿病病程为7.7年、平均HbA1c为8.71%、平均体重为76.6kg、平均BMI为27.9kg/m2,47.5%的受试者基线时使用磺脲类药物。其中穆峰达®5mg、10mg受试者体重平均降低5.0kg、7.0kg,甘精胰岛素组体重平均增加1.5kg。02庞大的减重处方药蓝海礼来生产的替尔泊肽和诺和诺德生产的司美格鲁肽都是目前全球最新一代的GLP-1药物。《Science》杂志评选的“2023年度十大科学突破”,就把GLP-1减肥药物评为了“年度科学突破之首”。在GLP-1类药物出现之前,一直未出现公认安全并且有效的减肥药物。也因此,司美格鲁肽和替尔泊肽一经获批上市,就引起市场的热捧。替尔泊肽降糖版Mounjaro在2022年5月在美获批上市;替尔泊肽减肥版本Zepbound也在2023年11月获得美国食品药品监督管理局(FDA)批准上市。两种版本均在上市以后大卖。财报显示,2024年一季度,替尔泊肽为礼来贡献了23.24亿美元的收入,占总营收的比重约为26%。其中,减肥版Zepbound上市不足5个月,一季度销售额已达5.17亿美元。而诺和诺德的司美格鲁肽(商品名:诺和泰)早在2021年就在中国获批治疗二型糖尿病;在美国市场,目前获批的剂型已增至3款,分别是Ozempic(注射用降糖药),Wegovy(注射用减重药)和Rybelsus(口服降糖药)。财报显示,今年一季度,三款相关产品共计实现营收422亿丹麦克朗(约60.81亿美元),支撑起了诺和诺德约2/3的营收。其中,减肥版Wegovy销售额同比增长106%,达93.77亿丹麦克朗(约13.51亿美元)。摩根士丹利预测,2030年,全球减重市场处方药规模或将突破770亿美元。03零售药店有望迎来新增长点对于GLP-1药物在国际市场的热捧,国内零售市场也正在爆发。司美格鲁肽虽上市时间不长,且受到适应症及相关政策的限制,但已经爆发出可观的市场潜力。数据显示,全国零售药店中,司美格鲁肽在2022年就创出近3亿的零售销售额。虽然其后受到各方面的影响,销售额一度大幅下降,但当前已恢复快速的增长,今年一季度销售额已超过8000万。全国零售药店司美格鲁肽销售情况而华东医药的GLP-1类新药(商品名:利鲁平)去年3月在国内获批减重适应症,仅在数据可见的三个季度内,零售药店市场已实现从零到超1300万的业绩突破,市场旺盛程度可见一斑。面对庞大的减肥药物需求,国内外药企都在争相抢道。目前国内已有112款GLP-1类新药进入临床阶段,涉及企业包括恒瑞医药、信立泰、甘李药业、华东医药、联邦制药、诺博特生物、双鹭药业、仁会生物、鸿运华宁等。此外,有媒体梳理发现,目前国内正在进行超过20个减重及肥胖症治疗的临床试验,其中多个已进入III期临床阶段。同时,多款药品已完成临床III期试验,或准备申请上市。随着GLP-1药物临床试验的推进和获批药物数量的增加,未来超适应症使用的情况可能会逐渐减少,合规性风险也将大大降低。有业内人士预计,司美格鲁肽有望在今年内获批减重适应症,届时将迎来市场的爆发,尤其在零售药店或出现一波销售热潮。不过,鉴于当前多数GLP-1药物在国内并未获批作为减肥药使用,消费者通过电商平台等渠道自行购买注射液使用,仍有较大风险。有专家提醒,盲目使用司美格鲁肽甚至自行增加剂量都是有风险的,一定要在医生的指导下,严格按医嘱用药。参考资料:国家药监局、礼来中国官网、中国新闻周刊、21世纪经济报道END内容沟通:13810174402医药代表交流群扫描下方二维码加入银发经济市场机遇交流群扫描下方二维码加入左下角「关注账号」,右下角「在看」,防止失联
上市批准财报临床3期医药出海
100 项与 北京诺博特生物科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 北京诺博特生物科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年09月02日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床申请批准
1
3
临床3期
其他
1
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
司美格鲁肽(深圳翰宇) ( GLP-1R ) | 肥胖 更多 | 临床3期 |
利多卡因/丁卡因 ( SCNA ) | 麻醉 更多 | 临床3期 |
司美格鲁肽生物类似药 (质肽生物) ( GLP-1R ) | 肥胖 更多 | 临床3期 |
重组人透明质酸酶( 北京诺博特生物) ( Hyaluronic acid ) | 药物辅助 更多 | 临床申请批准 |
利拉鲁肽生物类似药(诺博特生物) ( GLP-1R ) | 肥胖 更多 | 无进展 |
登录后查看更多信息
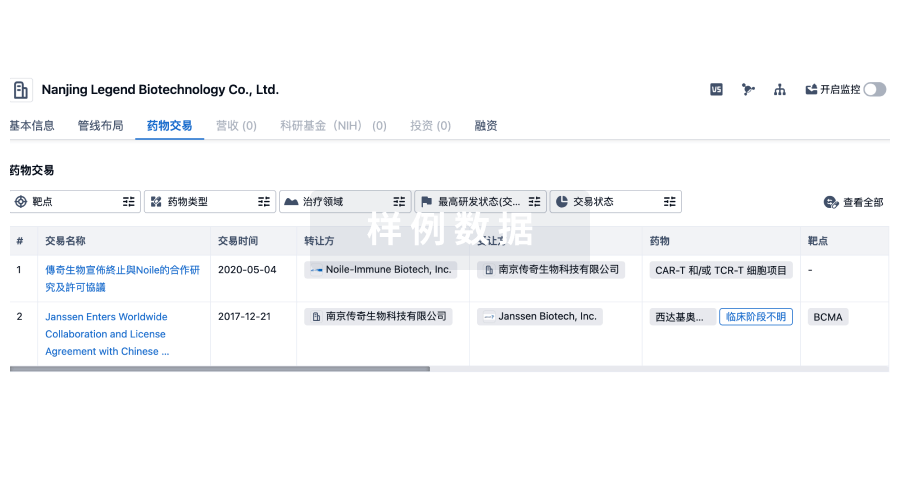
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
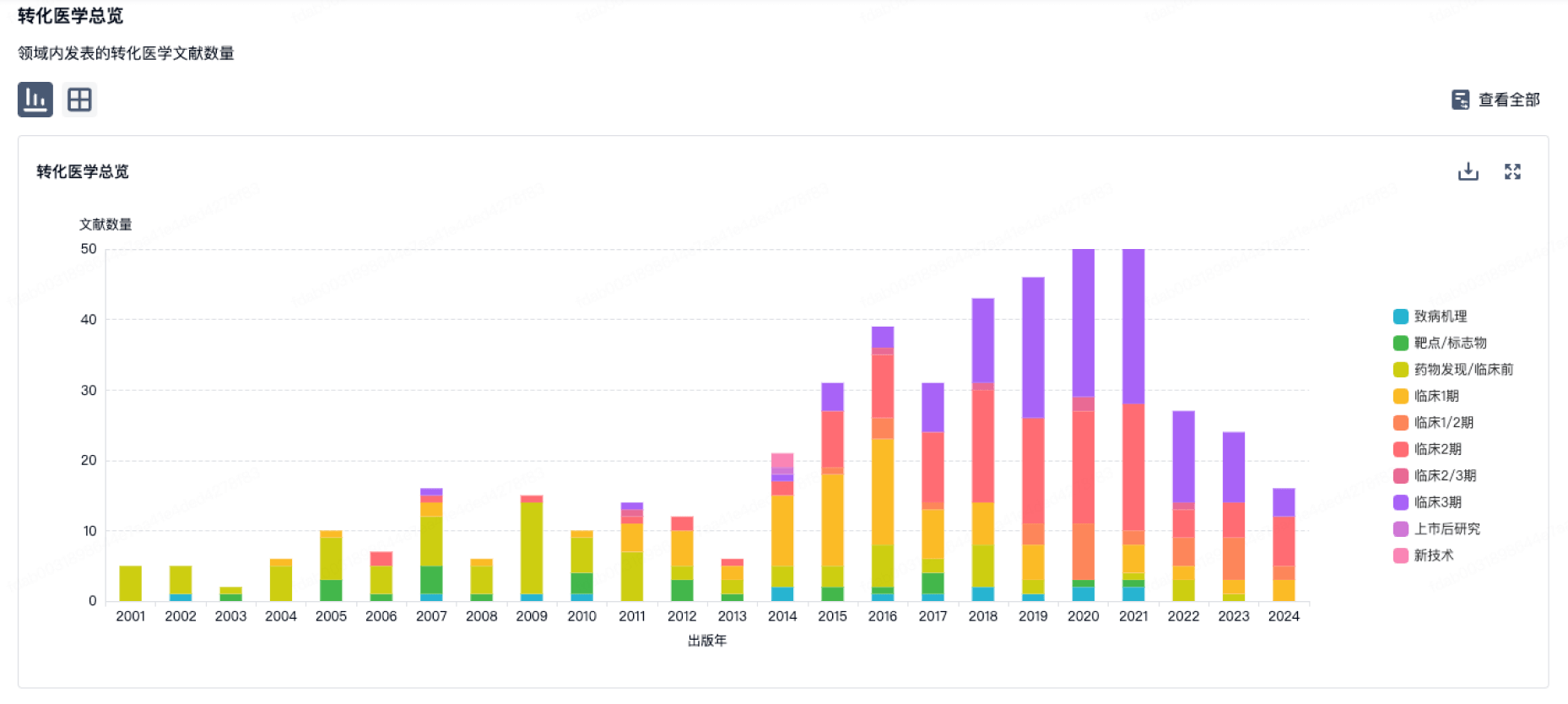
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
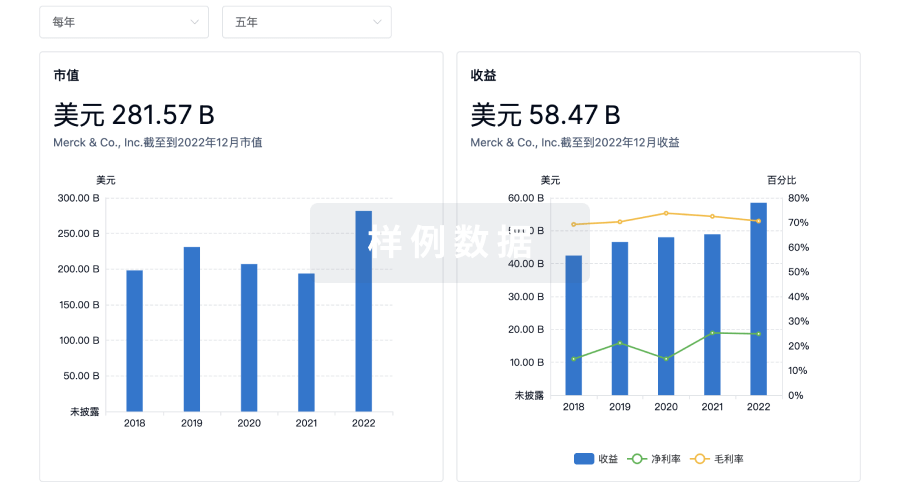
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
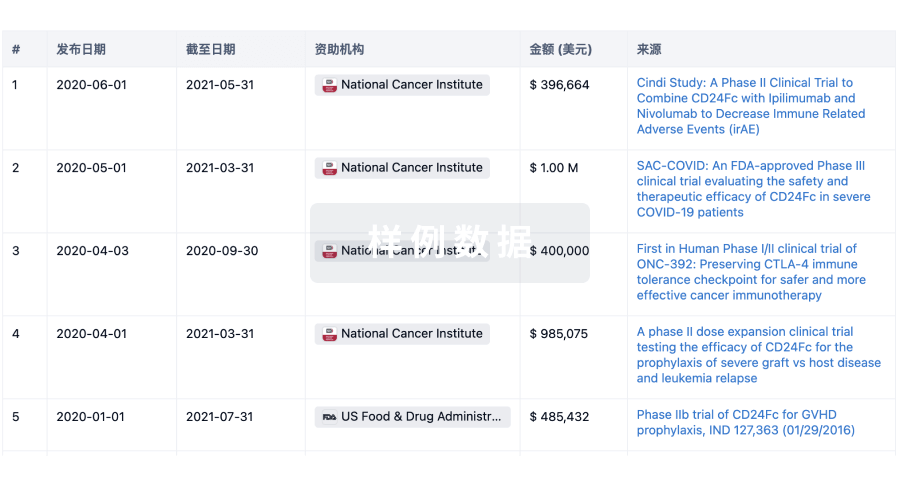
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
