从阿斯利康DS-8201a纳入突破性治疗品种,浅谈HER2阳性NSCLC治疗进展
2024-01-11
突破性疗法抗体药物偶联物申请上市临床结果
Preview
来源: CPHI制药在线
DS-8201a(德曲妥珠单抗,Enhertu/优赫得)是一种以HER2为靶点的新一代ADC,由人源化抗HER2抗体、酶切肽连接体和新型DNA拓扑异构酶Ⅰ抑制剂德卢替康(deruxtecan,DXd)组成。截至目前,DS-8201a已在美国获批多个适应症:既往接受过两种或以上抗HER2疗法的无法切除或转移性HER2阳性乳腺癌(2019.12);既往接受过曲妥珠单抗治疗的局部晚期或转移性HER2阳性胃或胃食管交界腺癌(2021.01);既往接受过一种抗HER2靶向疗法的无法切除或转移性HER2阳性乳腺癌(2022.05);既往接受过系统治疗的无法切除或转移性HER2突变阳性成人非小细胞肺癌(NSCLC)(2022.08);无法切除或转移性HER2低表达乳腺癌(2022.08)。
DS-8201a(Enhertu)最早由第一三共开发。2019年3月,阿斯利康与第一三共就该药达成一项总价值高达69亿美元的免疫肿瘤学合作。Enhertu上市后市场表现不错,2020年至2022年其全球销售额分别为2.75亿美元、4.26亿美元、12.6亿美元。2023年Enhertu销售额持续增长,前三季度销售额高达16.52亿美元。
在国内,DS-8201a(德曲妥珠单抗)最早于2023年2月被NMPA批准单药用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。今年7月,该药在国内获批第二个适应症:既往在转移性疾病阶段接受过至少一种系统治疗的,或在辅助化疗期间或完成辅助化疗之后6个月内复发的,不可切除或转移性HER2低表达(IHC 1+或IHC 2+/ISH-)成人乳腺癌患者。
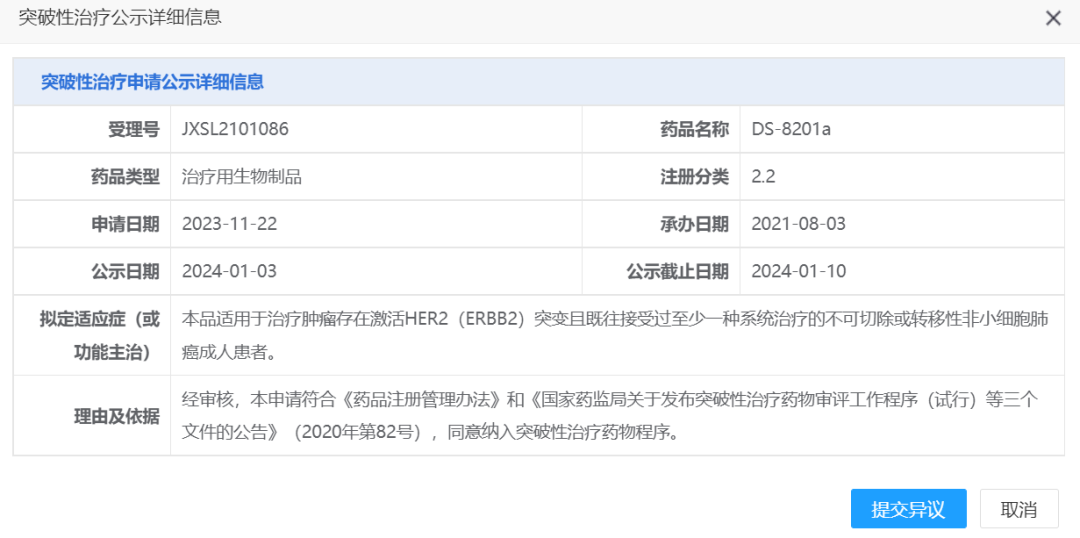
DS-8201a是FDA批准的第一个用于治疗HER2突变阳性非小细胞肺癌的药物。世界肺癌大会(WCLC 2023)上公布的DESTINY-Lung02研究结果证实DS-8201a在HER2突变NSCLC经治患者中显示出强大且持久的疗效和可管理的安全性特征。具体数据为:盲态独立中心评审委员会(BICR)评估的5.4mg/kg DS-8201a治疗组的客观缓解率(ORR)为49.0%,中位无进展生存期(mPFS)达9.9个月,中位总生存期(mOS)达19.5个月。此次DS-8201a二线治疗不可切除或转移性HER2阳性非小细胞肺癌(NSCLC)的适应症被CDE纳入突破性治疗程序,将加速该适应症在国内的获批进度。
肺癌是第二常见恶性肿瘤。据全球癌症流行统计数据,2020年全球肺癌新发病例约220.7万例,约占所有癌症病例的11.4%。2020年全球肺癌死亡约179.6万例,约占所有癌症死亡病例的18%。非小细胞肺癌(NSCLC)是肺癌中最常见的组织学类型,约占所有肺癌的85%。
与HER2野生型患者相比,HER2突变NSCLC患者生存率较差。约47%的HER2突变NSCLC患者在初诊或接受治疗中就被诊断存在脑转移。目前,临床上对于HER2突变NSCLC的探索集中在抗HER2治疗。但研究发现,既往的抗HER2治疗方案对HER2突变NSCLC患者的整体疗效获益并不理想,mPFS为3.2个月-6.9个月,ORR为15.6%-44%。总体来看,HER2突变NSCLC治疗领域还存在很大为满足的市场需求。
除了DS-8201a,全球还有几款药物被开发用于治疗HER2突变NSCLC,如Spectrum Pharma的poziotinib(波齐替尼,HM781-36B)、恒瑞医药的艾瑞妮、三生国健的伊尼妥单抗 poziotinib是一款泛-HER酪氨酸激酶抑制剂,能不可逆地阻断所有HER家族酪氨酸激酶受体的信号传递。WCLC 2023上公布的Poziotinib三线治疗HER2 20外显子插入NSCLC的ZENITH20研究数据显示:69名患者接受Poziotinib 16mg每日一次作为三线或更后续的全身治疗,IRC评估的ORR为30%(21/69),超过整个研究定义的17%的临床意义阈值。中位DOR为5.5个月,中位PFS为5.6个月。而且,poziotinib疗效与既往治疗的类型和顺序无关。遗憾的是,2022年11月,FDA拒绝批准poziotinib用于治疗先前接受过治疗、携带HER2外显子20插入突变(Ex20ins)的局部晚期或转移性NSCLC。
Pyrotinib是恒瑞自主研发,且拥有知识产权的口服HER1、HER2、HER4酪氨酸激酶抑制剂(TKI),已被NMPA批准三个适应症,即联合卡培他滨用于HER2阳性晚期乳腺癌的二线治疗;HER2阳性早期或局部晚期乳腺癌的新辅助治疗;HER2阳性晚期乳腺癌的一线治疗。此外,艾瑞妮还被开发用于HER2突变NSCLC的一线、二线、三线治疗。
中国医学科学院肿瘤医院王燕教授在《Thorac Cancer》杂志上发表的";Pyrotinib联合抗血管生成药物治疗HER2变异的晚期非小细胞肺癌:一项回顾性真实世界研究";数据显示:2015年11月30日至2022年1月31日,107例(表1)HER2变异的晚期NSCLC患者接受了艾瑞妮联合抗血管生成药物作为二线或后线治疗。截至2022年5月13日,82例患者经历了PFS事件。21例患者出现部分缓解(PR),80例患者疾病稳定(SD),6例患者在治疗开始1个月内出现疾病进展(PD)。患者的ORR为19.6%(21/107),DCR为94.4%(101/107),中位PFS为7.13个月(95% CI:6.26-8.01) ,中位OS为19.50个月(95% CI: 12.83-26.17)。安全性方面,最常见的3级或以上治疗相关不良事件包括腹泻(17.6%)、高血压(11.0%)、恶心(3.3%)等。这表明Pyrotinib联合抗血管生成药物有望为晚期HER2变异NSCLC提供新选择。
伊尼妥单抗是我国第一个自主研发、Fc段修饰和生产工艺优化的创新抗HER2单抗,已被批准联合化疗治疗HER2阳性转移性乳腺癌。2023 ASCO上公布的伊尼妥单抗联合Pyrotinib治疗HER2突变NSCLC的开放标签、Ib期研究数据显示:2021年8月6日至2022年8月25日,该研究共入组48例患者,Pyrotinib240 mg和320 mg剂量递增期未发生DLT。选择Pyrotinib320 mg作为扩展剂量。44例患者被纳入疗效分析,中位PFS为5.5个月,ORR和DCR分别为36.6%和85.4%。最常见治疗相关不良反应为腹泻、皮疹和呕吐。不良反应一般为1-2级,仅7例患者报告了3级不良反应。
内容来源于网络,如有侵权,请联系删除。
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。





