《自然·医学》:重大突破!CAR-T细胞疗法最常见/最棘手的神经毒性,终于有解了
2023-07-05
细胞疗法临床2期免疫疗法ASH会议临床1期
时隔五年,纪念斯隆-凯特琳癌症中心的Michel Sadelain团队,终于带着激动人心的临床研究数据和大家见面了。
今天,Sadelain团队在著名期刊《自然·医学》发表重磅研究成果[1],宣布给CAR-T细胞疗法最常见、最棘手的毒性之一,免疫效应细胞相关的神经毒性综合征(ICANS),找到了一个可靠的解决方案。
他们发起的这项2期临床研究的期中数据表明,预防性使用IL-1受体拮抗剂anakinra可大幅降低靶向CD19的CAR-T细胞疗法导致的ICANS的发生率,而不影响CAR-T细胞的治疗效果。
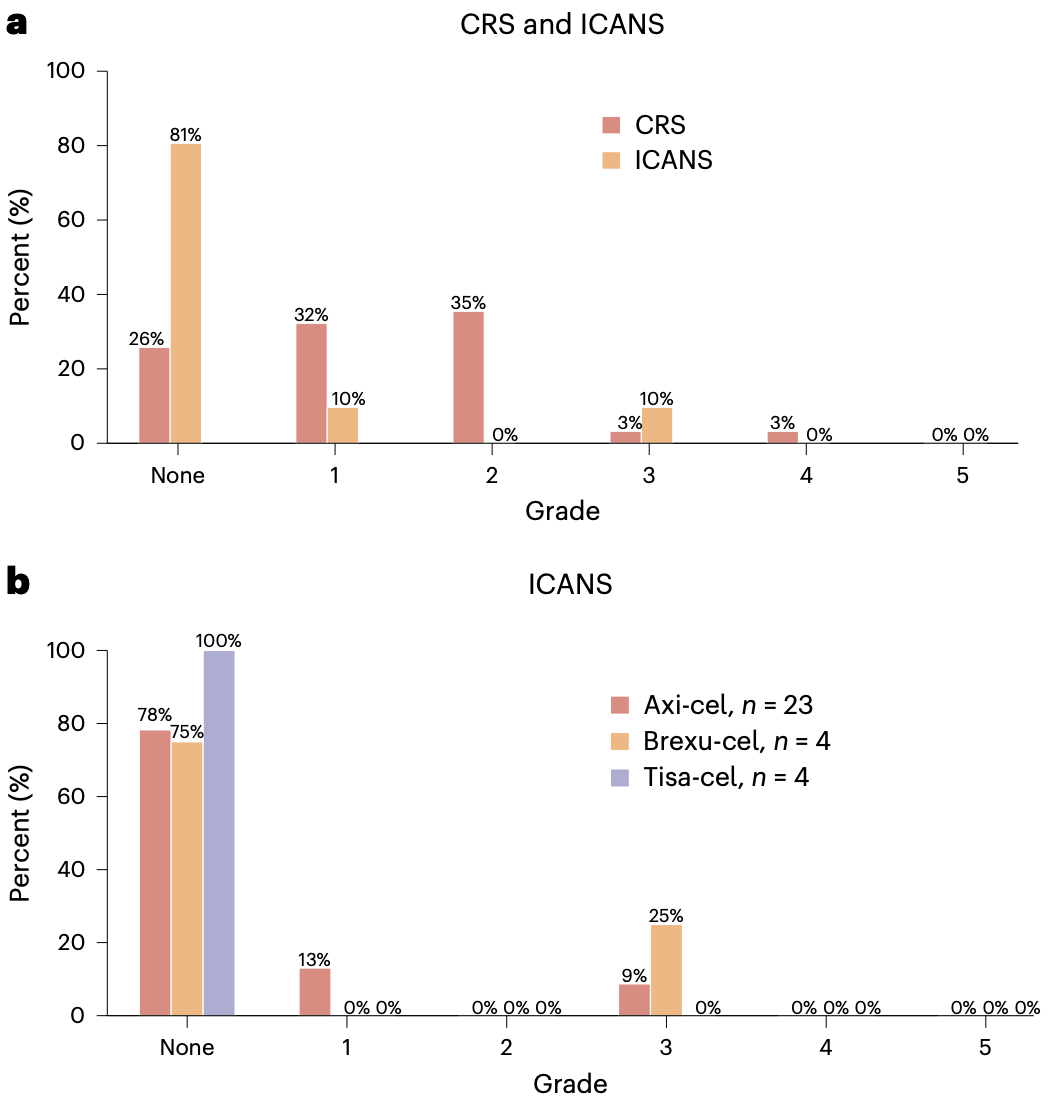
具体来说,在接受axicabtagene ciloleucel(axi-cel)cel)和brexucabtagene autoleucel(brexu-cel)cel)治疗的患者中,22%的患者发生了任何级别的ICANS,11%的患者发生了≥3级ICANS。要知道,在之前的临床试验和真实世界数据中,axi-cel和brexu-cel报告的任何级别ICANS为55-69%,≥3级ICANS为31-38%[2-5]。不难看出,这些初步数据表明,anakinra确实大幅降低了ICANS的发生率。

Preview
来源: 生物谷
论文首页截图
在CAR-T细胞疗法的临床使用过程中,最让人心惊胆战的毒性有两个,一个就是前面介绍的ICANS,另一个是有“细胞因子风暴”之称的细胞因子释放综合征(CRS)。
CRS近几年研究的比较多,IL-6受体拮抗剂托珠单抗(tocilizumab)已经获得FDA的批准,用于CRS的治疗[6]。至于ICANS,目前还没有针对性的有效疗法,临床上的常用处理药物是皮质类固醇[7]。有科学家研究了预防性使用皮质类固醇的效果,发现严重ICANS发生率确实有降低的趋势(13%-17%),但任何等级的ICANS发生率仍高达58-61%[8,9]。
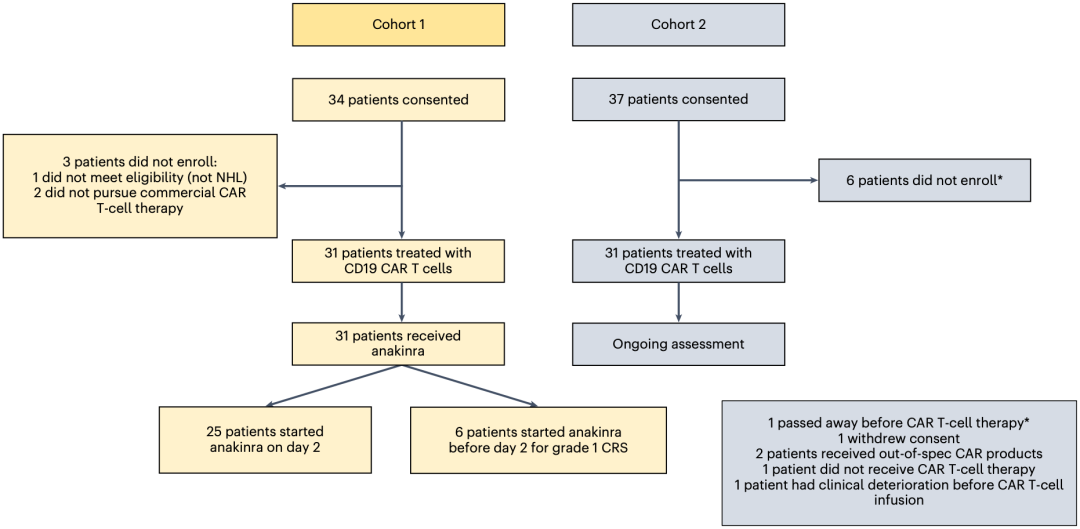
为了进一步在人体内证实anakinra的效果,在Sadelain团队Jae H. Park的领导下,一项在纪念斯隆-凯特琳癌症中心进行的单臂、2期临床试验(NCT04148430)启动了。这个研究包括两个队列。
在2019年11月11日到2021年4月5日间,队列1共入组31名患者。所有患者的中位年龄为62岁(范围:25-77岁),58%被诊断为复发/难治性大B细胞淋巴瘤(LBCL)、19%被诊断为高级别B细胞淋巴瘤(HGBCL)、13%被诊断为套细胞淋巴瘤(MCL),剩余10%为原发性纵隔B细胞淋巴瘤(PMBCL),所有患者之前接受的治疗中位数为三线(范围:2-5)。
Preview
来源: 生物谷
研究设计
Preview
来源: 生物谷
不同级别CRS和ICANS的发生情况,以及不同疗法的ICANS发生情况
那么预防性使用anakinra会不会降低CAR-T细胞的治疗效果呢?初步研究数据表明,这个担心可能是多余的。
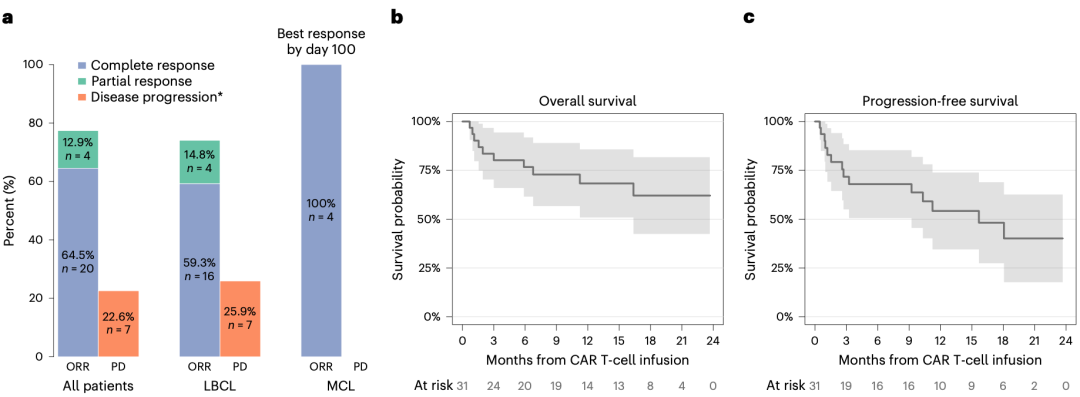
在中位随访时间为16个月(范围:1-24个月)的研究中,到第100天,31名患者中有24名出现了部分缓解或更好的最佳总体疗效(77%)。有20名患者达到了完全缓解(65%),4名患者实现了部分缓解(13%)。
Preview
来源: 生物谷
Anakinra对疗效的影响
Preview
来源: 生物谷
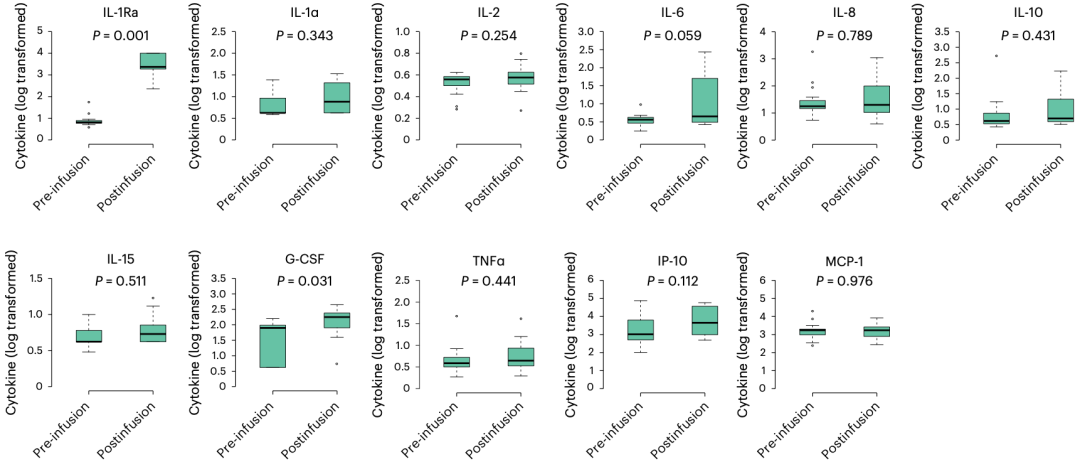
细胞因子的变化
希望anakinra在后续研究中取得更大的成功,帮接受CAR-T细胞治疗的患者除掉ICANS这个难题。
参考文献:
[1].Park, J.H., Nath, K., Devlin, S.M. et al. CD19 CAR T-cell therapy and prophylactic anakinra in relapsed or refractory lymphoma: phase 2 trial interim results. Nat Med, 2023. https://doi-org.libproxy1.nus.edu.sg/10.1038/s41591-023-02404-6
[2].Wang M, Munoz J, Goy A, et al. KTE-X19 CAR T-Cell Therapy in Relapsed or Refractory Mantle-Cell Lymphoma. N Engl J Med. 2020;382(14):1331-1342. doi:10.1056/NEJMoa1914347
[3].Nastoupil LJ, Jain MD, Feng L, et al. Standard-of-Care Axicabtagene Ciloleucel for Relapsed or Refractory Large B-Cell Lymphoma: Results From the US Lymphoma CAR T Consortium. J Clin Oncol. 2020;38(27):3119-3128. doi:10.1200/JCO.19.02104
[4].Pennisi M, Jain T, Santomasso BD, et al. Comparing CAR T-cell toxicity grading systems: application of the ASTCT grading system and implications for management. Blood Adv. 2020;4(4):676-686. doi:10.1182/bloodadvances.2019000952
[5].Riedell PA, Hwang WT, Nastoupil LJ, et al. Patterns of Use, Outcomes, and Resource Utilization among Recipients of Commercial Axicabtagene Ciloleucel and Tisagenlecleucel for Relapsed/Refractory Aggressive B Cell Lymphomas. Transplant Cell Ther. 2022;28(10):669-676. doi:10.1016/j.jtct.2022.07.011
[6].https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-tisagenlecleucel-b-cell-all-and-tocilizumab-cytokine-release-syndrome
[8].Oluwole OO, Bouabdallah K, Muñoz J, et al. Prophylactic corticosteroid use in patients receiving axicabtagene ciloleucel for large B-cell lymphoma. Br J Haematol. 2021;194(4):690-700. doi:10.1111/bjh.17527
[9].Topp MS, van Meerten T, Houot R, et al. Earlier corticosteroid use for adverse event management in patients receiving axicabtagene ciloleucel for large B-cell lymphoma. Br J Haematol. 2021;195(3):388-398. doi:10.1111/bjh.17673
[10].Giavridis T, van der Stegen SJC, Eyquem J, Hamieh M, Piersigilli A, Sadelain M. CAR T cell-induced cytokine release syndrome is mediated by macrophages and abated by IL-1 blockade. Nat Med. 2018;24(6):731-738. doi:10.1038/s41591-018-0041-7
[11].Norelli M, Camisa B, Barbiera G, et al. Monocyte-derived IL-1 and IL-6 are differentially required for cytokine-release syndrome and neurotoxicity due to CAR T cells. Nat Med. 2018;24(6):739-748. doi:10.1038/s41591-018-0036-4
[12].Neelapu SS, Locke FL, Bartlett NL, et al. Axicabtagene Ciloleucel CAR T-Cell Therapy in Refractory Large B-Cell Lymphoma. N Engl J Med. 2017;377(26):2531-2544. doi:10.1056/NEJMoa1707447
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。




