《自然》:CAR-T细胞抗癌疗法迎来革命性突破!
2022-07-26
免疫疗法细胞疗法放射疗法
过继T细胞治疗,是目前全世界肿瘤治疗研究和临床试验的热点。
过继T细胞治疗,是目前全世界肿瘤治疗研究和临床试验的热点。
为了提高过继T细胞治疗效果,患者往往需要预先接受放疗或者化疗性清髓。这种预处理方案,可能是通过平衡体内细胞因子产生,清除体内部分免疫抑制性细胞(如调节性T细胞和髓源性抑制细胞)等机制,提高了过继T细胞在体内的增殖能力和持久生存能力[2]。但是,高剂量的放化疗也给机体带来了严重的副作用,使得很多患者无法耐受清髓方案,而失去获益机会[3]。
他们首次设计出一种融合了正交IL-2受体(oIL-2R)和IL-9受体(IL-9R)嵌合受体,可在不需要预先放化疗清髓的情况下,活化过继T细胞,并赋予其干细胞样记忆T细胞和效应T细胞的双重表型,使之有效地发挥抗肿瘤功能。

Preview
来源: 生物谷
论文首页截图
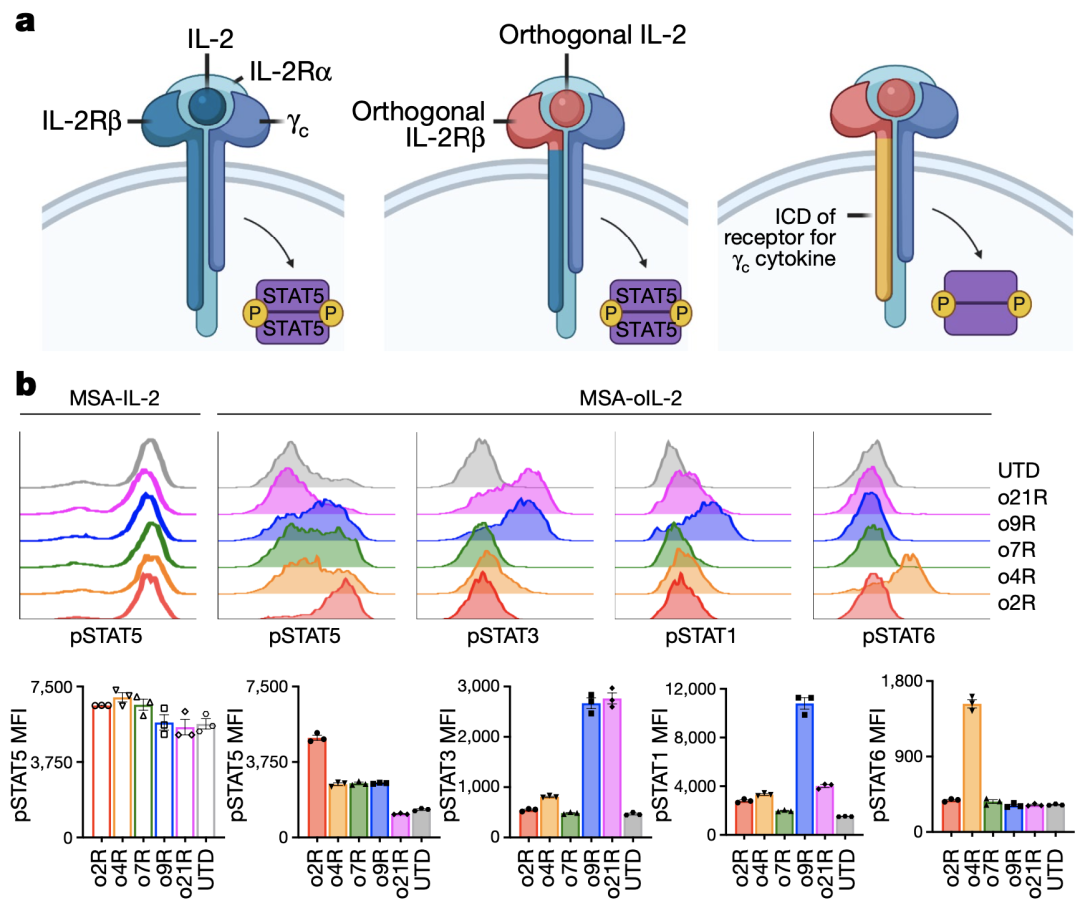
Preview
来源: 生物谷
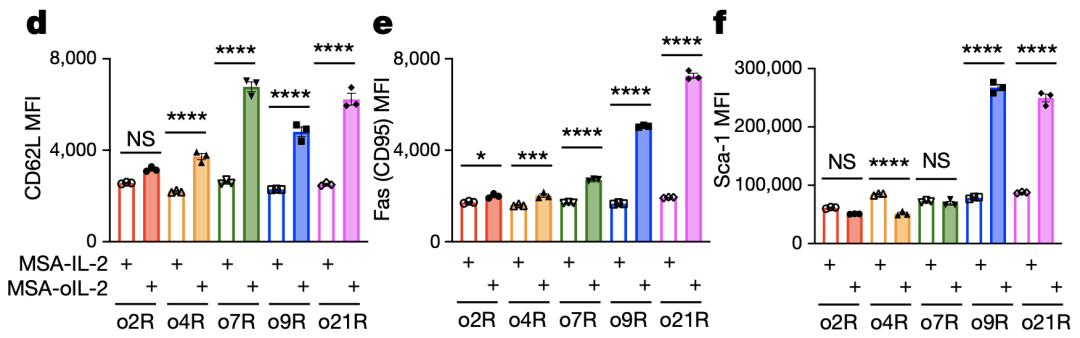
Preview
来源: 生物谷
激活o9R后,细胞表型趋向于干细胞样记忆T细胞
鉴于o9R独特的信号转导和赋予细胞重要的表型特征,研究人员想利用这种新设计的过继T细胞来治疗实体瘤。
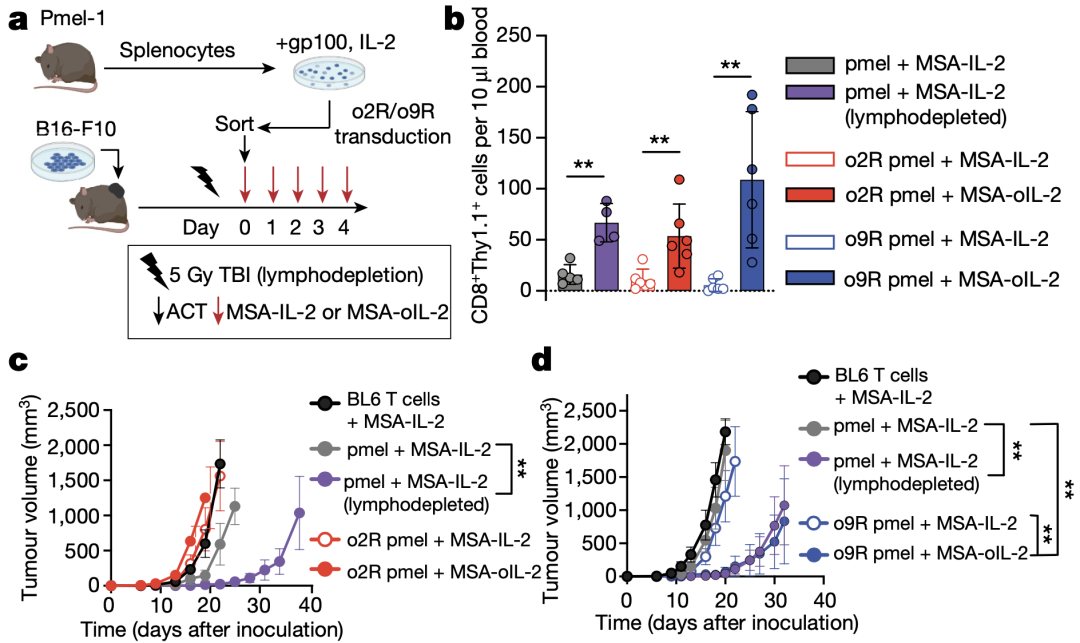
Preview
来源: 生物谷
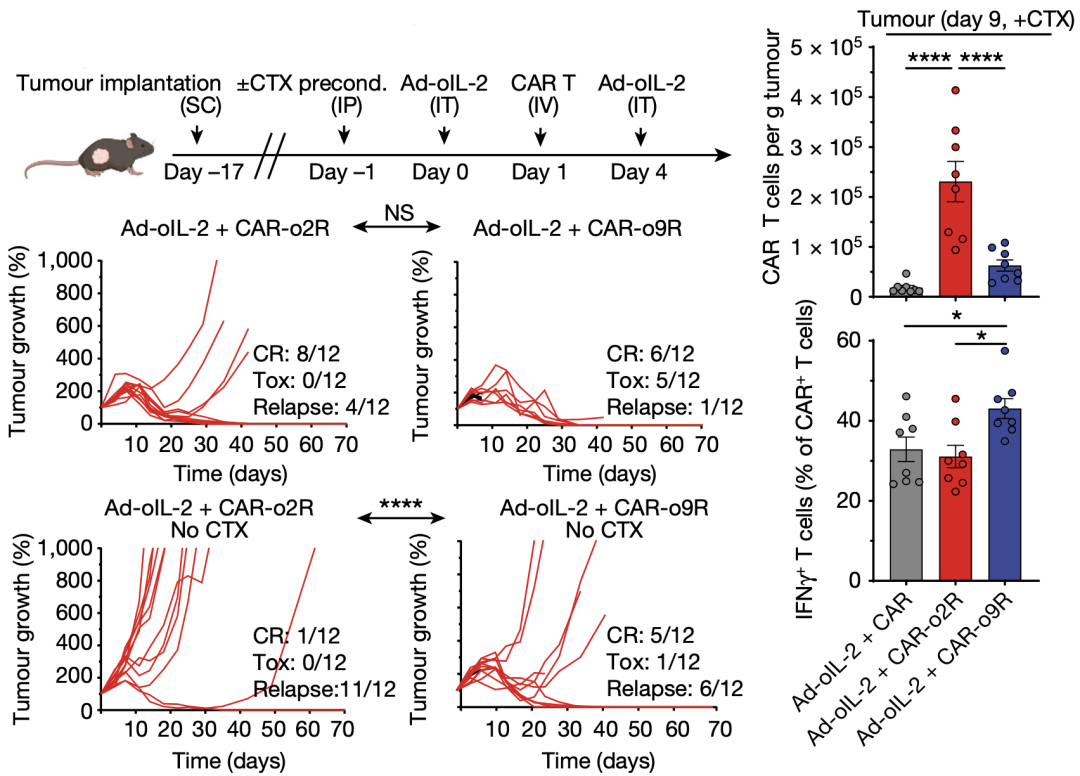
接下来,为了研究o9R信号转导在CAR-T中的作用,研究人员利用一种免疫治疗抵抗的模型——表达间皮素(mesothelin)的胰腺癌小鼠,并构建了CAR。同时,为了探讨o9R信号通路对肿瘤微环境中CAR-T细胞功能障碍的影响,他们设计了仅在瘤内用腺病毒载体递送oIL-2(Ad-oIL-2)。
结果显示,在没有预先淋巴细胞清除性化疗的情况下,Ad-oIL-2加CAR-o9R联合治疗,获得了更高比例的完全缓解(5/12)和更长的生存期。虽然与pmel模型相比,肿瘤中CAR-o9R比CAR-o2R T细胞浸润数量更少,但是CAR-o9R T细胞的转录组变化仍旧与o9R pmel T细胞相似。
Preview
来源: 生物谷
局部递送Ad-oIL-2 与CAR-o9R 联合治疗,胰腺癌小鼠完全缓解率更高和细胞杀伤作用更强
那么,这种新方法是否有潜力应用于临床呢?作者设计了人源的正交IL-2Rβ(ho2R)和嵌合IL-2Rβ-IL-9R(ho9R),并以此为基础分别构建了可识别肿瘤抗原NY-ESO-1和mesothelin的TCR T细胞和CAR-T细胞。结果显示,与小鼠相似,ho9R激活了一致的磷酸化信号、干细胞样的功能表型以及更强的多功能性效应分子表达和杀伤能力。
总的来说,这个研究设计了一种新的嵌合受体o9R来改造T细胞,使之获得了一种独特的干细胞记忆T细胞和效应T细胞的双重身份,能够在体内长期存活增殖并杀伤肿瘤。
这个新方法,对于过继T细胞在实体瘤治疗来说,无疑具有重要意义。同时,这个研究构建并在体外验证的人源o9R T细胞,也为后续的临床转化提供了有吸引力的数据。
参考文献
[1] Schietinger A, Philip M, Krisnawan VE, et al. Tumor-Specific T Cell Dysfunction Is a Dynamic Antigen-Driven Differentiation Program Initiated Early during Tumorigenesis. Immunity. 2016;45(2):389-401. doi:10.1016/j.immuni.2016.07.011
[2] Rosenberg SA, Restifo NP. Adoptive cell transfer as personalized immunotherapy for human cancer. Science. 2015;348(6230):62-68. doi:10.1126/science.aaa4967
[3] Dudley ME, Yang JC, Sherry R, et al. Adoptive cell therapy for patients with metastatic melanoma: evaluation of intensive myeloablative chemoradiation preparative regimens. J Clin Oncol. 2008;26(32):5233-5239. doi:10.1200/JCO.2008.16.5449
[4] Kalbasi A, Siurala M, Su LL, et al. Potentiating adoptive cell therapy using synthetic IL-9 receptors [published online ahead of print, 2022 Jun 8]. Nature. 2022;10.1038/s41586-022-04801-2. doi:10.1038/s41586-022-04801-2
[5] Sockolosky JT, Trotta E, Parisi G, et al. Selective targeting of engineered T cells using orthogonal IL-2 cytokine-receptor complexes. Science. 2018;359(6379):1037-1042. doi:10.1126/science.aar3246
[6] Leonard WJ, Lin JX, O'Shea JJ. The γc Family of Cytokines: Basic Biology to Therapeutic Ramifications. Immunity. 2019;50(4):832-850. doi:10.1016/j.immuni.2019.03.028
[7] Krishna S, Lowery FJ, Copeland AR, et al. Stem-like CD8 T cells mediate response of adoptive cell immunotherapy against human cancer. Science. 2020;370(6522):1328-1334. doi:10.1126/science.abb9847
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。