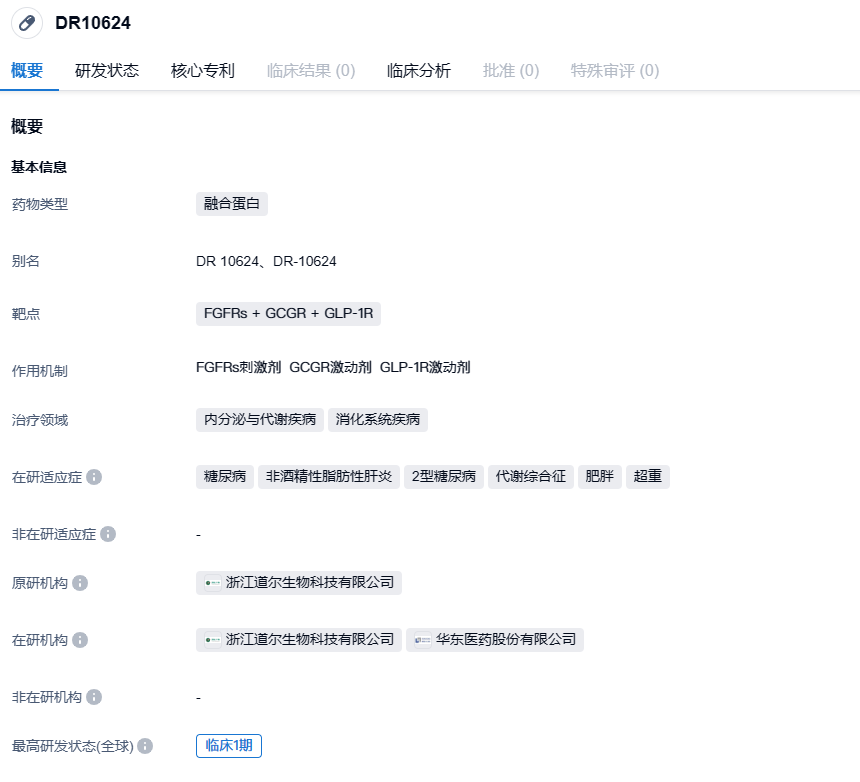
华东医药全球首创GLP-1R/GCGR/FGF21R三靶激动剂DR10624减肥适应症获批临床
2023年7月30日,华东医药发布一则公告,称其控股子公司道尔生物申报的GLP-1R/GCGR/FGF21R三靶激动剂注射用DR10624临床试验申请获得批准,适应症为超重或肥胖人群的体重管理。
DR10624为华东医药子公司道尔生物开发的一种靶向 GLP-1 受体(GLP-1R)、GCG 受体(GCGR)和 FGFR1c/Klothoβ(FGF21R)的长效三靶点激动剂。由 N 端靶向 GLP-1R/GCGR 的嵌合肽段与工程化改造的 IgG1 Fc 融合,并在 Fc 的 C 末端融合重组的 FGF21 突变体。DR1024 由中国仓鼠卵巢(CHO)细胞表达,经纯化后获得。DR10624 结构上为对称二聚体,具有 GLP-1R、GCGR与FGF21R三重激动剂的生物学活性,同时融合有去糖基化改造的 IgG1Fc 以延长半衰期。临床前的动物研究显示,DR10624 具有明显的降脂、减重、降糖等疗效。
围绕GLP-1靶点,华东医药已构筑了包括口服、注射剂在内的长效及多靶点全球创新药和生物类似药相结合的全方位和差异化的产品管线。截至目前,全球尚无同时靶向GLP-1R、GCGR和FGF21R的长效三靶点激动剂药物上市,此次注射用DR10624在中国的临床试验获批是该款新药研发进程和全球临床转化中的重要进展,将进一步丰富公司在内分泌治疗领域的产品管线。截止目前DR10624已在新西兰开展I 期临床试验,并完成首例患者给药。
①2022年4月,道尔生物获得新西兰药品和医疗器械安全管理局(Medsafe)、健康及残疾伦理委员会(HDEC)的最终批准,获准在当地开展注射用 DR10624 的 I 期临床试验。
②2022年6月,DR10624 在新西兰完成 I 期临床试验的首例受试者给药。
③2023年7月,DR10624 在新西兰完成了治疗肥胖症的 I 期多次递增剂量给药(MAD)临床试验的首例受试者给药。
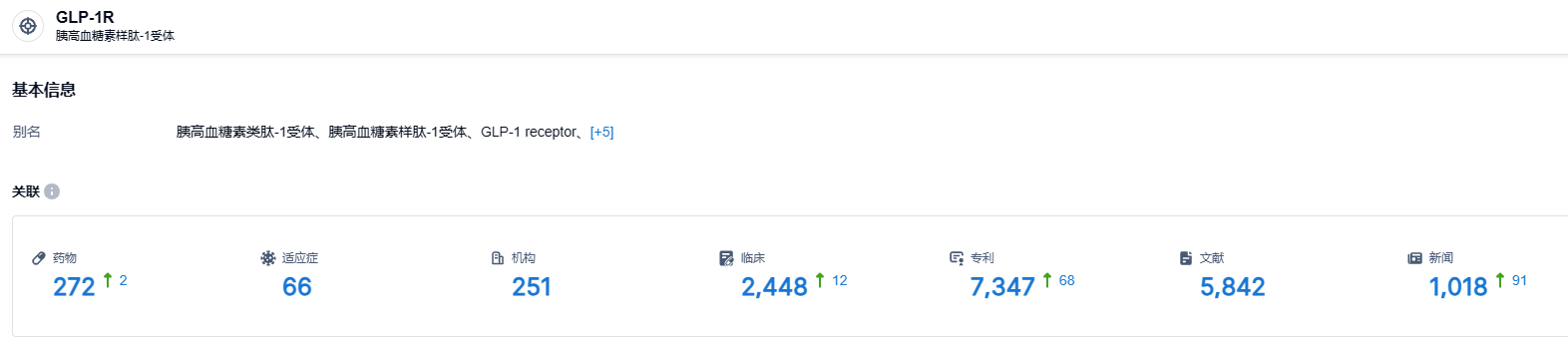
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 GLP-1R靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年8月1日,GLP-1R 靶点共有在研药物272个,包含的适应症有66种,在研机构251家,涉及相关的临床试验2448件,专利多达7347件……期待DR10624的后续表现。