恒瑞医药HER2 ADC瑞康曲妥珠单抗上市申请获受理,针对非小细胞肺癌
9月13日,恒瑞医药发布公告,SHR-A1811(瑞康曲妥珠单抗)的上市申请获得NMPA受理,并于今日纳入优先审评,用于既往接受过至少一种系统治疗的局部晚期或转移性HER2突变成人非小细胞肺癌患者。
SHR-A1811(瑞康曲妥珠单抗)是恒瑞医药自主研发的、以HER2为靶点的抗体偶联药物(ADC),注射用SHR-A1811可通过与HER2表达的肿瘤细胞结合并内吞,在肿瘤细胞溶酶体内通过蛋白酶剪切释放毒素,诱导细胞周期阻滞从而诱导肿瘤细胞凋亡。SHR-A1811由曲妥珠单抗、可裂解四肽连接子和新型拓扑异构酶 I 抑制剂载荷 SHR9265 组成,DAR 值为 5.7。与 DS8201 相比,恒瑞在结构上进行了优化,在 SHR-A1811 的有效载荷与连接子临近处引入了一个手性环丙基。SHR-A1811目前已开展多项Ⅰ~Ⅲ期临床研究,涵盖HER2表达或突变的晚期实体瘤、晚期胃癌或胃食管结合部腺癌、结直肠癌、晚期非小细胞肺癌、转移性乳腺癌等。此前,该药物已有6个适应症获得突破性疗法认定,包括:1)既往接受过一种或一种以上治疗方案的HER2阳性不可切除或转移性胆道癌患者;2)既往至少一线抗HER2治疗失败的HER2阳性晚期胃癌或胃食管结合部腺癌患者;3)单药治疗既往经奥沙利铂、氟尿嘧啶和伊立替康治疗失败、HER2阳性结直肠癌;4)单药治疗既往含铂化疗失败的HER2突变的晚期非小细胞肺癌患者;5)HER2低表达的复发或转移性乳腺癌;6)HER2阳性的复发或转移性乳腺癌患者。
I/II期SHR-A1811-I-103研究结果显示,瑞康曲妥珠单抗在既往接受过治疗的HER2过表达、扩增或突变的转移性NSCLC患者中表现出了良好的临床疗效和持久反应,并且具备良好的安全性。该研究共纳入了63例接受标准治疗失败的HER2突变肺癌受试者,在不同剂量水平下接受了SHR-A1811治疗,中位随访时间为11.1个月。全剂量组患者中位无进展生存期(mPFS)为9.5个月,经研究者评估确认的客观缓解率(ORR)为38.1%(95% CI:26.1-51.2),疾病控制率(DCR)高达90%以上,中位缓解持续时间(DoR)为10.3个月(95% CI:5.45-NR);4.8mg/kg剂量组中位PFS为8.4个月(95% CI:7.1-15.0),超过40%的患者在接受治疗后达到了疾病缓解,ORR为41.9%(95% CI:27.0-57.9),DCR为95.3%(95% CI:84.2-99.4),中位DoR为13.7个月(95% CI:5.5-NR)。
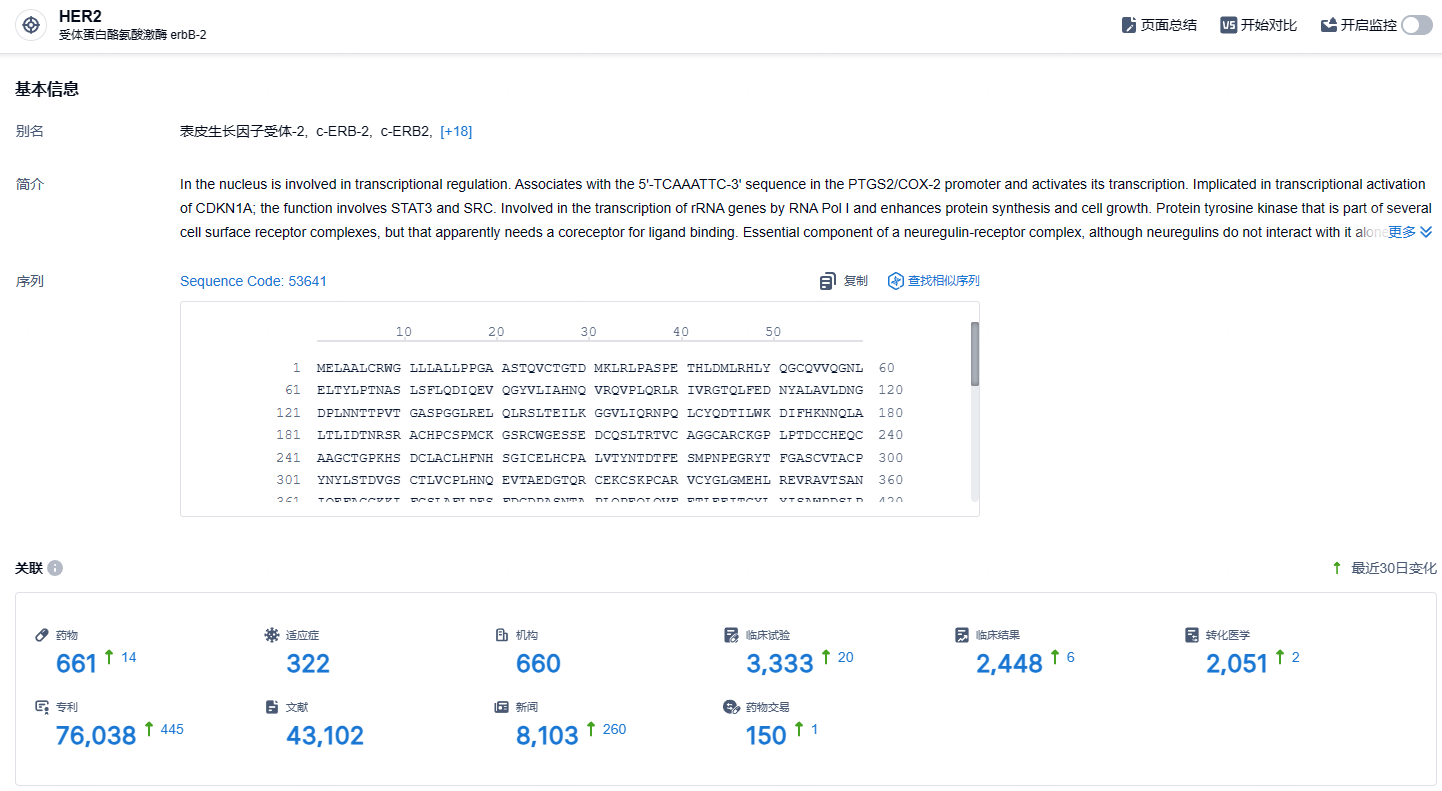
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 HER2 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年9月14日,HER2靶点共有在研药物661个,包含的适应症有322种,在研机构660家,涉及相关的临床试验3333件,专利多达76038件……SHR-A1811 首次临床申请始于 2020 年 5 月,次月就启动首个临床试验,当前已经针对乳腺癌、非小细胞肺癌、胃癌、结直肠癌开展了近20 项临床试验。SHR-A1811在T-DXd的结构基础上进一步优化,在多癌种中取得了良好的ORR及安全性数据,有望为恒瑞医药的肿瘤新药拓宽护城河。