全球首个!赛诺菲靶向IL-4Rα新药度普利尤单抗两项III期临床成功
9月11日,赛诺菲宣布度普利尤单抗(商品名:Dupixent)治疗大疱性类天疱疮(BP)的II/III期ADEPT研究和治疗慢性自发性荨麻疹(CSU)的III期LIBERTY-CUPID研究C部分均取得了积极结果。这也是BP领域第一款在后期研究中取得积极进展的生物制剂,赛诺菲计划基于以上积极结果在今年递交度普利尤单抗的补充生物制品许可申请(sBLA)。
度普利尤单抗是赛诺菲和再生元合作开发的一款人源性单克隆抗体,靶向IL-4Rα。研究表明,IL-4和IL-13是2型炎症的关键驱动因素,2型炎症在哮喘、慢性鼻窦炎伴鼻息肉病、特应性皮炎等炎症性疾病中发挥重要作用。度普利尤单抗能够通过IL-4和IL-13“双靶点”的创新作用机制阻断2型炎症通路,降低2型炎症的病理性反应,从机制上治疗2型炎症相关疾病。2017 年 3 月,度普利尤单抗获FDA批准成为首个用于治疗成人中重度特应性皮炎的靶向生物药,商品名为 Dupixent®。
ADEPT研究是一项为期52周的随机、双盲、安慰剂对照临床试验(n=106),评估了度普利尤单抗(300mg,每2周1次)联合口服糖皮质激素(OCS)对比安慰剂联合OCS治疗中度至重度成人BP患者的疗效和安全性。结果显示,治疗第36周,度普利尤单抗组实现持续缓解的患者比例高于安慰剂组(20% vs. 4%,p=0.0114)。BP是一种慢性复发性疾病,其特征是严重瘙痒和水泡、皮肤红肿和慢性疼痛。目前,该疾病尚无针对性疗法获批。
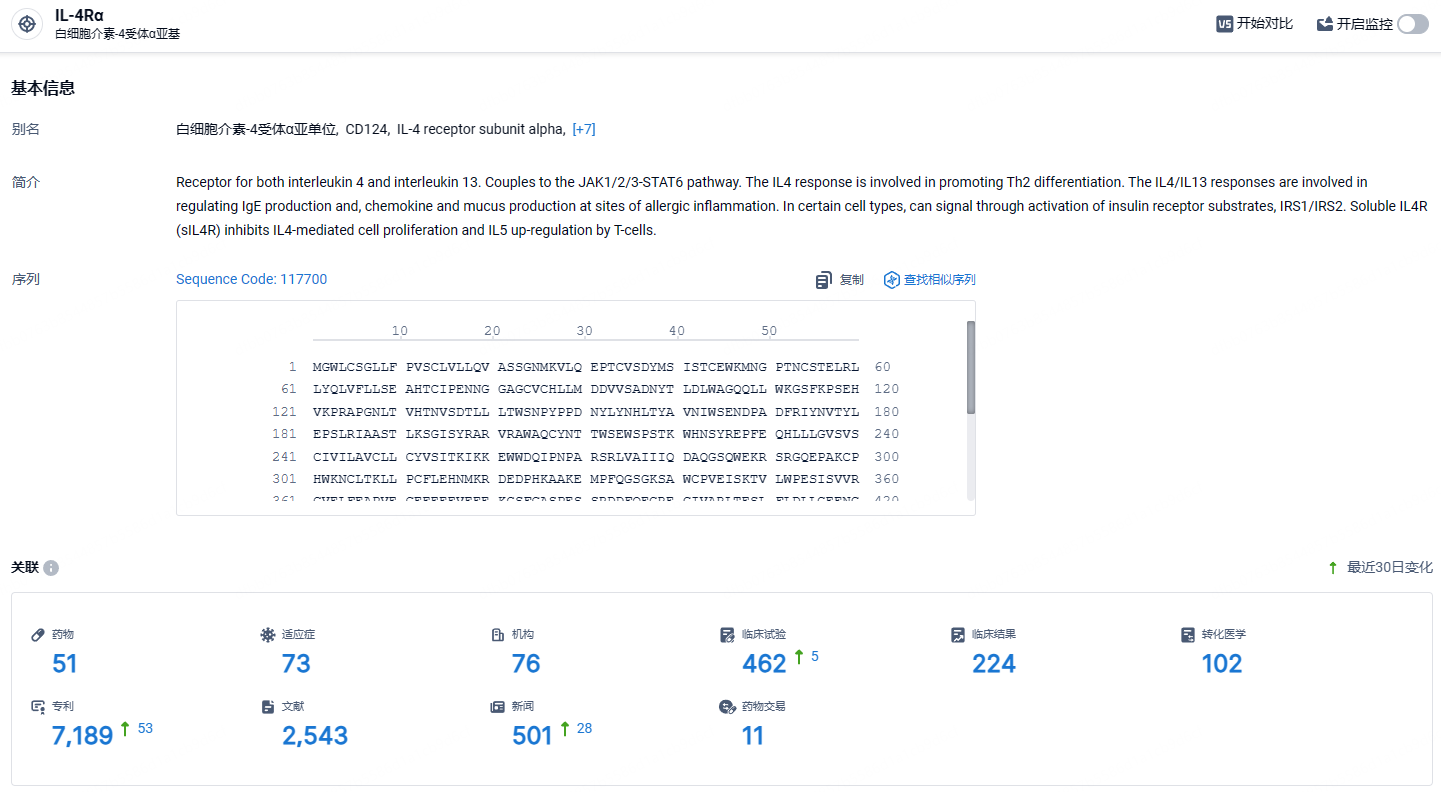
根据智慧芽新药情报库所披露的信息 (点击下方图片直达IL-4Rα靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年9月12日,IL-4Rα靶点共有在研药物51个,包含的适应症有73种,在研机构76家,涉及相关的临床试验462件,专利多达7189件……度普利尤单抗是第一款领域横跨皮肤科、呼吸科、变态反应用药的生物制剂,优秀的临床数据,使得其具有非常强的市场潜力。自2017 年上市以来度普利尤单抗全球销售额增长迅速,至2023年达到107.15亿欧元。期待度普利尤单抗商业化再创佳绩。