常山药业长效GLP-1R激动剂艾本那肽申报上市,治疗2型糖尿病
2024年4月24日,常山药业宣布,由其控股子公司常山凯捷健生物开发的GLP-1受体激动剂艾本那肽注射液首个新药上市申请(NDA)已获中国国家药品监督管理局(NMPA)受理,申报的适应症为治疗2型糖尿病。
艾本那肽是一种长效胰高血糖素样肽-1 受体(GLP-1R)激动剂,是利用药物亲和力偶合物(DACTM)技术,将艾塞那肽进行化学修饰后,与重组人血白蛋白结合形成的一个全新的稳定化合物,每周注射一次。艾本那肽是常山凯捷健进行研发注册的 1 类创新药,用于治疗 2 型糖尿病。GLP⁃1RA 通过激活胰高血糖素样肽-1(GLP⁃1)受体以葡萄糖浓度依赖的 方式刺激胰岛素分泌和抑制胰高糖素分泌,同时增加肌肉和脂肪组织葡萄糖摄取, 抑制肝脏葡萄糖的生成而发挥降糖作用,并可抑制胃排空,抑制食欲。2023年9月18日,常山药业发布公告,宣布每周1次GLP-1R激动剂艾本那肽(CJC-1134-PC)治疗2型糖尿病的两项III期研究达到主要终点。
试验方案编号为CSCJC DM301的研究是一项多中心、随机、双盲、安慰剂对照III期临床试验,旨在评价艾本那肽在接受二甲双胍单药或二甲双胍联合胰岛素促泌剂治疗后血糖控制不佳的2型糖尿病患者中的有效性和安全性。主要疗效分析提示,试验组和安慰剂组双盲治疗24周后,统计数据表明试验组相对于安慰剂组的优效性成立。次要疗效分析结果显示,艾本那肽可提高接受二甲双胍单药或二甲双胍联合胰岛素促泌剂治疗后血糖控制不佳的2型糖尿病患者的HbA1c达标率,维持HbA1c在目标水平。安全性方面,艾本那肽在这类2型糖尿病患者中具有较好的安全性,未出现新增的非预期安全性风险,与其他GLP-1RA的安全性特征基本一致。
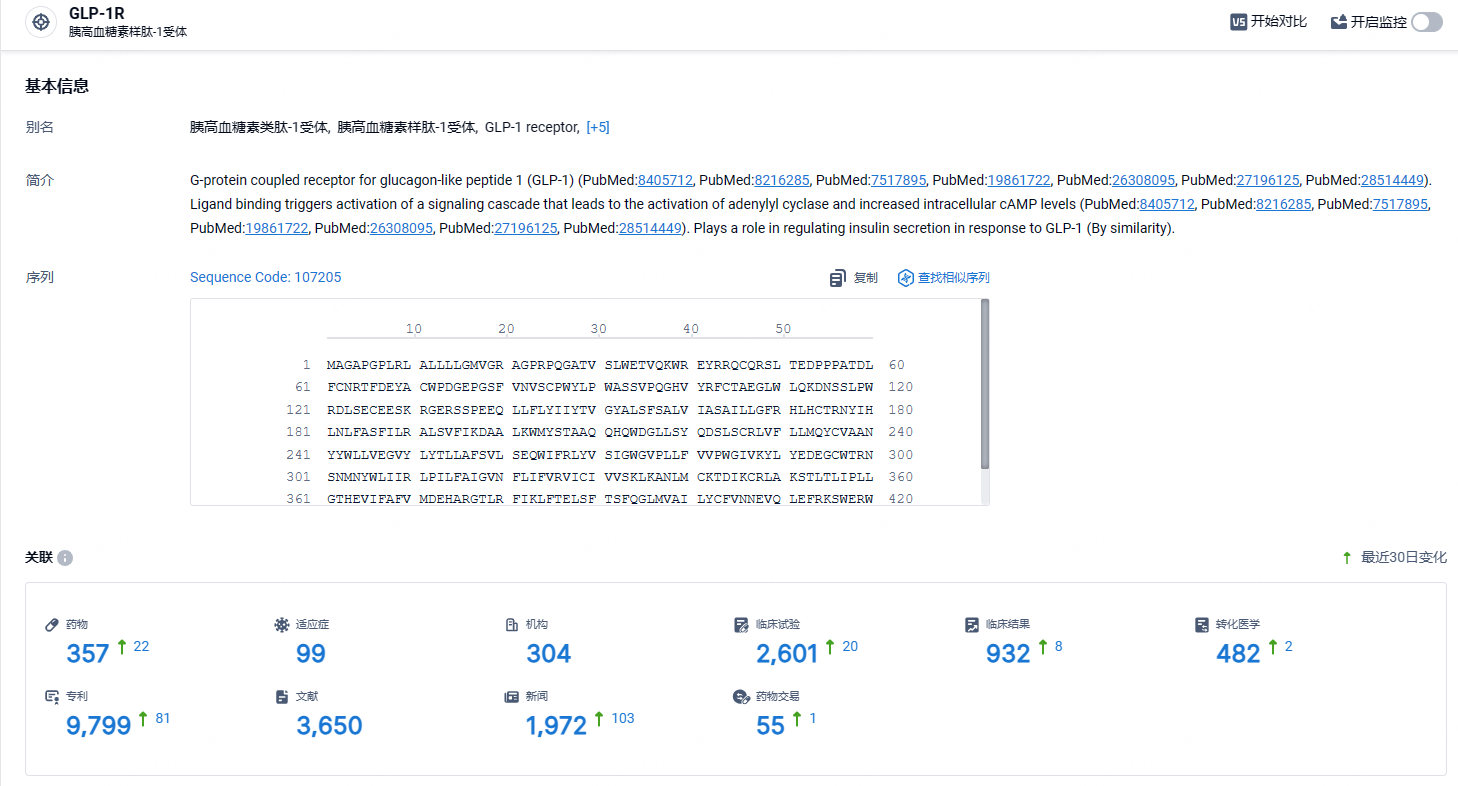
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 GLP-1R靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年4月27日,GLP-1R靶点共有在研药物357个,包含的适应症有99种,在研机构304家,涉及相关的临床试验2601件,专利多达9799件……GLP-1受体激动剂类产品相对安全,兼具减肥、降糖和心血管获益的功效,是相对成熟稳定和安全的靶点。GLP-1R单靶点或多靶点新药正在如火如荼的进行临床研究,红海市场初见端倪。围绕GLP-1受体靶点,众多国内企业都进行了布局,期待艾本那肽的后续表现。