BMS终止历时七年基因疗法合作,AAV治心衰要被放弃?
2022-12-01
基因疗法引进/卖出
上周批准的B型血友病基因疗法Hemgenix(350万美元,约合2500万元)又又又一次刷新了史上最贵药物的世界纪录。而正当CSL Behring和uniQure正在为Hemgenix的成功获批而欣喜之时,uniQure却在一份11月28日向美国证券交易委员会披露的文件中表示,百时美施贵宝(BMS)方面做出决定,将在2023年2月21日终止与uniQure方面已经维持了7年,价值10亿美元,以充血性心力衰竭为方向的基因治疗战略合作。不过,在提交的文件中,uniQure没有透露BMS选择终止协议的原因。这项合作最初始于2015年,那时的合作最初集中在一项基因S100A1上,这是一种钙结合蛋白,S100A1是心脏功能的主要调节因子,可通过SERCA2a、PLN、RyR2等多种途径发挥其调控钙循环的功能,在充血性心力衰竭模型中显示出恢复大部分心脏功能的潜力。而通过递送S100A1-AAV有治疗心力衰竭疾病的潜力。随后双方在2020年对协议设计的付款事宜,合作项目,排他性问题进行了修订,从现在来看,这些合作项目总共涉及了uniQure管线中未披露的四个项目。BMS的放弃虽然未曾说明原因,但也一定程度上打出了一个“问号”:采用基因治疗递送心脏来治疗心衰这件事本身可行吗?
基因治疗治心衰的尝试
目前基因治疗递送至心衰的主要靶点有:肌质网钙离子ATP酶2a(SERCA2a),腺苷酸环化酶 6(AC6),基质细胞衍生因子1(SDF-1)和S100A1等等,其中进入人体临床且采用AAV的仅有SERCA2a,在安全性方面基因治疗似乎与安慰剂并无差异,但在有效性方面这些基因疗法似乎都遇到了阻碍。
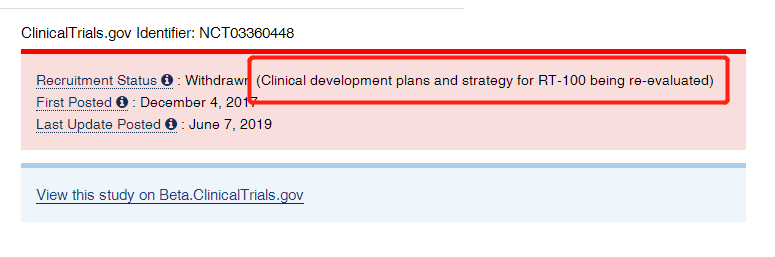
以SERCA2a为例,使用AAV治疗心脏的临床开始于Roger J. Hajjar博士领导的使用AAV1递送SERCA2a。(又名MYDICAR)SERCA2a基因过表达可增强肌浆网钙泵逆浓度梯度重新摄取心肌细胞内钙离子,从而改善心肌高钙环境。在广泛小动物,大动物,体外的临床实验中,AAV1-SERCA2a均证明了AAV1改善了心肌收缩性。然而,2007年在患者中开展的I/II a期试验CUPID却并不如人意。尽管早期试验证明有临床事件减少,但2015年随后发布的临床数据表明,AAV1/SERCA2a在测试剂量下并未改善心力衰竭和射血分数降低患者的临床进程,临床也随之终止。这一失败导致了开发MYDICAR的Celladon公司因此一蹶不振,裁员80%,最后不得不选择与Eiger公司合并,而后MYDICAR也遭到“雪藏”。而对于AAV临床失败的原因,研究人员也有对此的解释,在他们检查了不幸死亡或接受心脏移植的受试者的心脏后发现,在分析的组织中几乎没有发现病毒载体基因组,这表明基因转导有缺陷,而不是转基因功能无效,这一结果表明,递送问题仍然是AAV的首要需要解决的问题。以AC6为例,2016年Hammond等人报道了Ad5.hAC6(研发代码RT-100RT-100)在心衰患者中的安全性和有效性数据,但其结果并不理想。虽然在心力衰竭患者中冠状动脉内递送Ad5.hAC6似乎是安全的,(基因治疗组和安慰剂组患者均有出现不良事件,其中不良事件指住院或死亡,但两组之间并没有统计学上差异。)但在一些关键指标上Ad5.hAC6的有效性似乎并不足以证明自己。同患者基因治疗组与安慰剂组比较,患者的运动耐量无显著差异。而评价心衰的重要指标射血分数(EF值)在4周时较安慰剂组上升(P<0. 04),但在12周时EF值又无统计学差异(P = 0. 16)。在住院率方面,基因治疗组患者的住院率为9. 5%,而安慰剂组的住院率为28.6%(P = 0.1)。这些结果似乎表明Ad5(腺病毒)在心脏内递送具有持久性问题,研究人员也在发表论文中认为需要III期临床试验进行摸索。然而,可惜的是,进行该治疗的公司Renova Therapeutics在2019年时以重新评估RT-100RT-100的临床开发计划和战略为由撤回了III期临床,从该公司官网也并无后续太多关于RT-100RT-100的信息了。
Preview
来源: 生物制药小编
以SDF-1为例,表达SDF-1蛋白JVS-100有别于上述两种基因治疗方法,是通过质粒进行治疗的基因疗法。虽然安斯泰来在2018年时与Juventas Therapeutics公司就JVS-100达成了合作协定,然而,JVS-100的I期临床和II临床的数据差异似乎较大,I期临床展现出了6至12个月各项指标的改善,但在II期临床中,15mg 30mg JVS-100以及安慰剂组三组患者的上述指标并没有展现出统计学差异,但是对于心脏功能极差的患者(EF<26% ),在治疗的12个月时其EF值的增加量与安慰剂组比较具有统计学差异,这表明JVS-100由于其机制是通过通过促进心肌细胞的修复达到改善心功能的目的,因此对于心功能更差的患者SDF-1的效果可能更好。而目前,Juventas Therapeutics官网Pipeline上已经没有JVS-100的任何开发计划。
小编总结
总体而言,BMS终止合作的做法完全在意料之中,两家公司选择合作的2015年本就不是心衰AAV治疗的好时间,毕竟MYDICAR就是那段时间暂停的,隔了7年时间再选择停止,可能是为这没有意义的长跑划下了一个句号。
参考来源:https://clinicaltrials.gov/ct2/show/NCT00534703?term=SERCA2a+AAV&draw=2&rank=1Hammond HK, Penny WF, Traverse JH, Henry TD, Watkins MW, Yancy CW, Sweis RN, Adler ED, Patel AN, Murray DR, Ross RS, Bhargava V, Maisel A, Barnard DD, Lai NC, Dalton ND, Lee ML, Narayan SM, Blanchard DG, Gao MH. Intracoronary Gene Transfer of Adenylyl Cyclase 6 in Patients With Heart Failure: A Randomized Clinical Trial. JAMA Cardiol. 2016 May 1;1(2):163-71. doi: 10.1001/jamacardio.2016.0008. PMID: 27437887; PMCID: PMC5535743.
内容来源于网络,如有侵权,请联系删除。
药物
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。




