“渐冻症”新药!Albrioza获全球首个监管批准:显著改善临床功能下降,降低死亡风险!
2022-06-14
小分子药物

Preview
来源: 生物谷
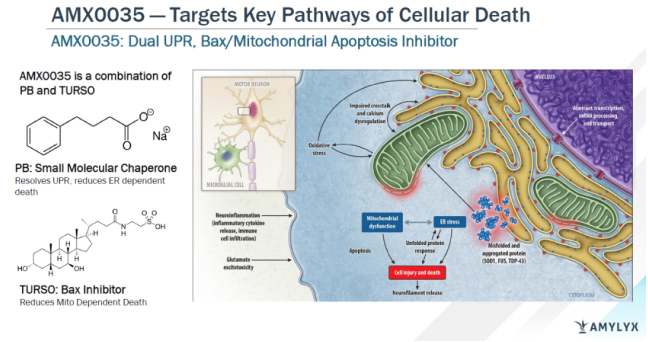
Albrioza(AMX0035,PB-TURSO)是一种由苯丁酸钠(sodium phenylbutrate,PB)和牛磺酸二醇(taurursodiol,TURSO,又名ursodoxicoltaurine)组成的专有口服固定剂量复方制剂。PB是一种小分子伴侣,旨在减少未折叠蛋白反应(UPR),防止因UPR导致的细胞死亡。TURSO是一种Bax抑制剂,旨在通过凋亡减少细胞死亡。PB和TURSO在固定剂量配方中联合使用,靶向肌萎缩侧索硬化症(ALS)和其他神经退行性疾病中的内质网和线粒体依赖性神经元退行性变通路,减少神经元死亡和功能障碍。
Preview
来源: 生物谷
AMX0035作用机制
Preview
来源: 生物谷
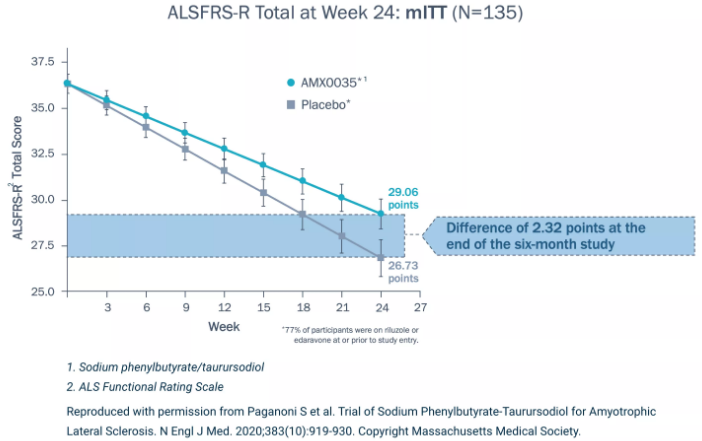
CENTAUR试验6个月安慰剂对照期数据
肌萎缩侧索硬化症(amyotrophic lateral sclerosis,简称ALS),俗称“渐冻症”,这是一种不可逆的致死性运动神经元病,主要症状为四肢和躯干肌肉表现进行性加重的肌肉无力和萎缩,逐渐失去运动功能,像被“冻住”一般,所以俗称“渐冻人”。该病一般进展迅速,半数以上患者确诊后平均生存时间为3-5年,最后多死于呼吸肌无力导致的呼吸衰竭。据估计,ALS在全球范围内的发病率约为十万分之二。尽管大约5%-10%的病例与遗传有关,但ALS的病因至今不明,可能涉及遗传和环境因素。目前已上市的药物仅能延缓病情进展,还没有能够治愈ALS的药物。
今年5月,美国FDA批准三菱田边制药Radicava ORS(edaravone,依达拉奉,口服混悬剂),用于治疗ALS。Radicava ORS专为ALS患者群体开发,将提供灵活的给药选择(口服或通过喂食管服用),无需调整剂量。Radicava ORS与Radicava(依达拉奉注射液)具有相同的活性药物成分和相同的疗效,后者是美国FDA在2017年5月批准上市的静脉注射(IV)疗法,在关键临床试验中被证实可帮助减缓ALS患者身体功能丧失。
截至目前,美国FDA已批准6款药物治疗ALS,除了Albrioza之外,有3款为不同剂型的利鲁唑产品【Exservan(利鲁唑口腔膜剂)、Rilutek(利鲁唑片剂)、Tiglutik(利鲁唑混悬剂)】,另2款为不同剂型的依达拉奉产品【Radicava(edaravone,依达拉奉静脉注射液)、Radicava ORS(依达拉奉口服混悬液)】。
利鲁唑(riluzole)被认为可以通过降低谷氨酸水平来减少运动神经元的损伤,谷氨酸是一种兴奋性神经递质,在神经细胞和运动神经元之间传递信息。依达拉奉(edaravone)是一种自由基清除剂,被认为能够缓解氧化应激的影响,而这可能是ALS发病和病情发展的关键因素。依达拉奉的抗氧化作用被认为能够为神经系统提供神经保护性支持,潜在延缓疾病发展或限制额外伤害。(生物谷Bioon.com)
原文出处:Amylyx Pharmaceuticals Announces Health Canada Approval of ALBRIOZA™ for the Treatment of ALS
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
-靶点
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


