Nature子刊:揭示人源葡萄糖转运子SGLT1的抑制机制
2022-11-21
钠-葡萄糖共转运蛋白(SGLT)是人体中负责葡萄糖重吸收的重要转运蛋白,能够利用钠离子的电化学势进行葡萄糖的逆浓度梯度转运
作为II型糖尿病治疗的重要靶点,利用SGLT2抑制剂来治疗糖尿病的思路就是通过抑制SGLT2的糖转运功能,使得SGLT2无法从原尿中重吸收葡萄糖,导致多余的葡萄糖从尿液中排出以达到间接降低血糖的目的。已经有很多SGLT2抑制剂如恩格列净(Empagliflozin)、卡格列净(Canagliflozin)、达格列净(Dapagliflozin)6等小分子药物被研发出来用于临床治疗II型糖尿病。此外,最近的临床试验表明,与单独使用SGLT2抑制剂相比,同时抑制SGLT1和SGLT2在治疗II型糖尿病中可能会更有优势7,并且靶向SGLT1的抑制剂还有治疗便秘的效果8。
SGLT的抑制剂均是以天然产物根皮苷的结构为基础优化产生,根据它们的选择性可以将这些抑制剂分为三类:SGLT2特异性抑制剂,如恩格列净(Empagliflozin),卡格列净(Canagliflozin),达格列净(Dapagliflozin)等;SGLT1特异性抑制剂,如KGA-2727,mizagliflozin以及SGLT1-SGLT2非选择性抑制剂,如LX2761,索格列净(sotagliflozin)等。因此,了解这些药物是如何抑制SGLT的功能对于药物开发和优化具有重要意义。
Preview
来源: 生物谷
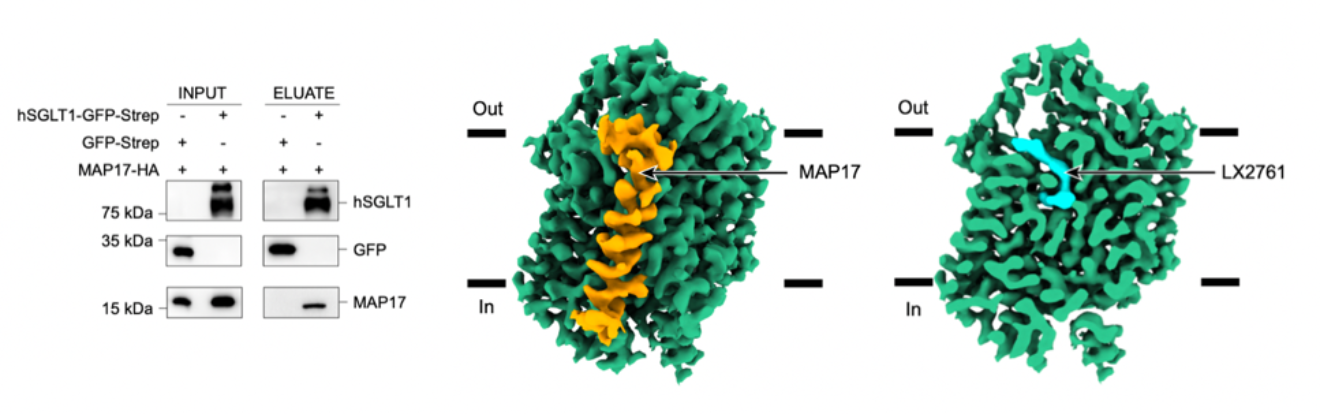
Preview
来源: 生物谷
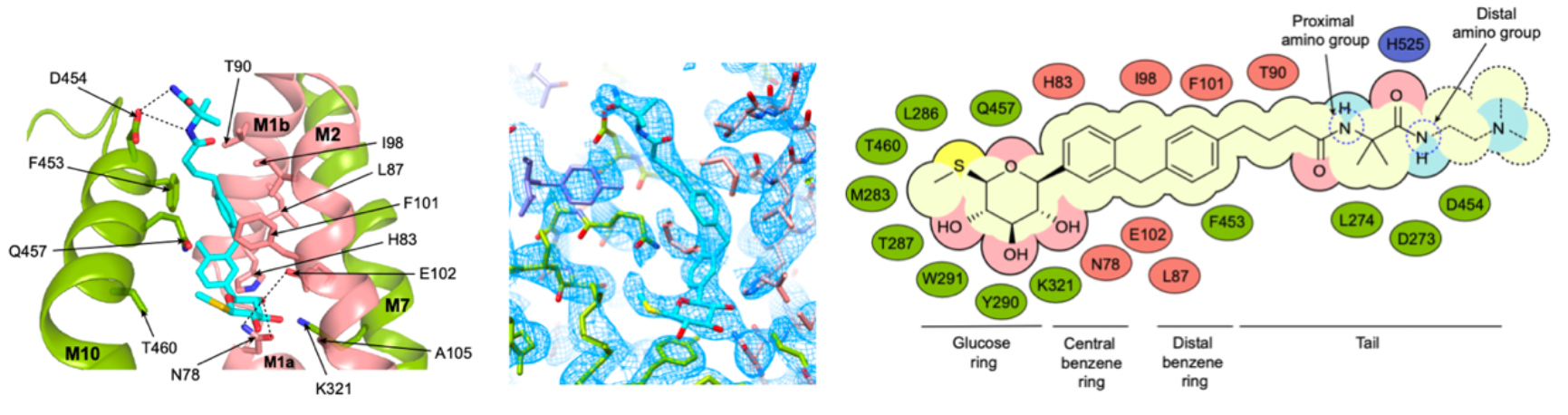
图2. 抑制剂LX2761的结合位点
为了解释SGLT1特异性抑制剂mizagliflozin的选择性机制,作者将SGLT1和SGLT2的抑制剂结合口袋进行了比较,发现在SGLT1中的结合口袋要略大于SGLT2,而这一差异来源于SGLT1第160位氨基酸的差异:SGLT1第160位丙氨酸对应于SGLT2的第157位缬氨酸。作者通过分子动力学模拟对mizagliflozin与SGLT1的结合模式进行了模拟,并将模拟结果与SGLT2的结构进行了比对。结果发现,由于LX2761的中央苯环基团被mizagliflozin的异丙基吡唑基取代,在SGLT2的V157位氨基酸处形成了空间冲突,这可能导致了mizagliflozin对SGLT2的效力降低。因此,作者分别构建了SGLT1的A160V和SGLT2的V157A突变体,发现在SGLT1中将A突变为V会降低mizagliflozin的效力,而在SGLT2中将V突变为A则会提高mizagliflozin的效力。因此,作者鉴定了SGLT1的A160为影响Mizagliflozin选择性的主要位点之一。
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
-热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


