更新于:2024-07-01
Elgemtumab
更新于:2024-07-01
概要
基本信息
原研机构 |
在研机构- |
最高研发阶段终止临床1/2期 |
首次获批日期- |
最高研发阶段(中国)- |
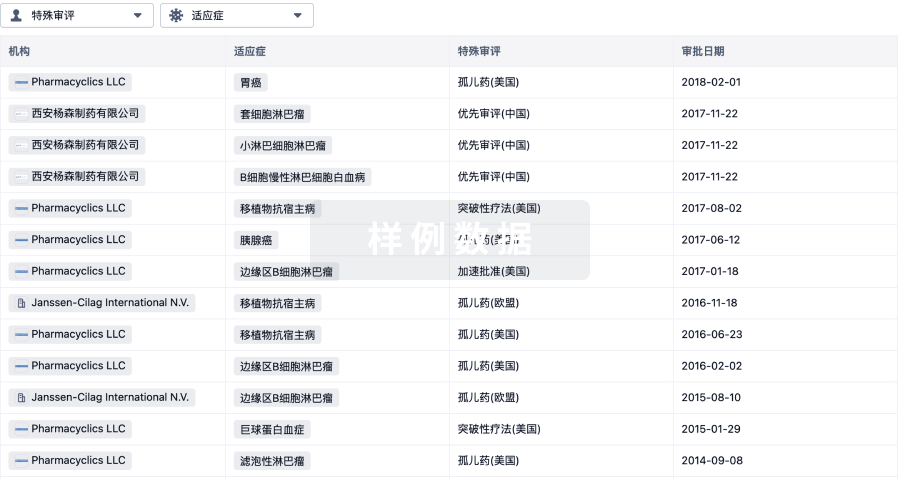
特殊审评- |
序列信息
Sequence Code 133807L

来源: *****
Sequence Code 1049009444H

来源: *****
关联
10
项与 Elgemtumab 相关的临床试验A Phase Ib/II, Multicenter Study of LJM716 in Combination With Cetuximab in Patients With Platinum-pretreated Recurrent/Metastatic Head and Neck Squamous Cell Carcinoma
To establish whether LJM716 in combination with cetuximab is safe and has beneficial effects in patients with platinum-pretreated recurrent/metastatic head and neck squamous cell carcinoma.
开始日期2015-03-01 |
A Phase I, Open-Label Study Evaluating the Safety and Tolerability of LJM716, BYL719 and Trastuzumab in Patients With Metastatic HER2+ Breast Cancer
This is a Phase I study. The purpose of this study is to determine what is the best dose of the study drug BYL719 in combination with the study drug LJM716 and traztuzumab (Herceptin®). The study will test the safety of the combination of these three drugs, and to find out the effects, good and/or bad, that these three drugs have on the patient and breast cancer.
开始日期2014-06-16 |
申办/合作机构 |
A phase Ib/II, multicenter study of LJM716 in combination with cetuximab in patients with platinum-pretreated recurrent/metastatic head and neck squamous cell carcinoma
开始日期2014-06-11 |
申办/合作机构 |
100 项与 Elgemtumab 相关的临床结果
登录后查看更多信息
100 项与 Elgemtumab 相关的转化医学
登录后查看更多信息
100 项与 Elgemtumab 相关的专利(医药)
登录后查看更多信息
9
项与 Elgemtumab 相关的文献(医药)2021-07-15·Clinical cancer research : an official journal of the American Association for Cancer Research1区 · 医学
A Phase I Study of Alpelisib in Combination with Trastuzumab and LJM716 in Patients with PIK3CA-Mutated HER2-Positive Metastatic Breast Cancer
1区 · 医学
Article
作者: Wang, Rui ; Chandarlapaty, Sarat ; Shah, Payal Deepak ; Patil, Sujata ; Fornier, Monica N. ; Pareja, Fresia ; Jhaveri, Komal ; Modi, Shanu ; Rosen, Neal ; Ratzon, Fanni ; Iasonos, Alexia ; Drago, Joshua Z. ; Sklarin, Nancy T.
Abstract:
Purpose::
Activating mutations in PIK3CA promote resistance to HER2-targeted therapy in breast cancer; however, inhibition of PI3K alone leads to escape via feedback upregulation of HER3. Combined inhibition of HER2, HER3, and PI3K overcomes this mechanism preclinically.
Patients and Methods::
This phase I study investigated the MTD of alpelisib given in combination with trastuzumab and LJM716 (a HER3-targeted antibody) in patients with PIK3CA-mutant HER2-positive (HER2+) metastatic breast cancer (MBC) using the continual reassessment method. Secondary analyses included efficacy and exploratory correlative studies.
Results::
Ten patients were treated initially with daily alpelisib (arm A). Grade ≥3 adverse events seen in ≥2 patients included diarrhea (n = 6), hypokalemia (n = 3), abnormal liver enzymes (n = 3), hyperglycemia (n = 2), mucositis (n = 2), and elevated lipase (n = 2). The MTD of alpelisib in arm A was 250 mg daily. This prompted the opening of arm B in which 11 patients received intermittently dosed alpelisib. Grade ≥3 adverse events seen in ≥2 patients included diarrhea (n = 5), hypokalemia (n = 3), and hypomagnesemia (n = 2). The MTD of alpelisib in arm B was 350 mg given 4 days on, 3 days off. Among 17 patients assessed, 1 had a partial response, 14 had stable disease, and 2 had disease progression at best response. Five patients had stable disease for >30 weeks. mRNA profiling of pre- and on-treatment tissue demonstrated PIK3CA target engagement by alpelisib via induction of downstream signaling and feedback pathways.
Conclusions::
Combination treatment with alpelisib, trastuzumab, and LJM716 was limited by gastrointestinal toxicity. Further efforts are warranted to target the PI3K pathway in HER2+ MBC.
2019-10-01·Xi bao yu fen zi mian yi xue za zhi = Chinese journal of cellular and molecular immunology
[Preparation and identification of single-chain fragment variable against epidermal growth factor receptor 3].
Article
作者: Qiu, Chuangnan ; Zhao, Lin ; Li, Huangjin ; Liu, Mengmiao ; Wen, Biyan ; He, Peiyan
Objective To express, purify and identify the single-chain fragment variable (scFv) against human epidermal growth factor receptor 3 (HER3). Methods We searched NCBI for the light chain sequence and heavy chain sequence of anti-HER3 mAb LJM716 to construct the gene of scFv against HER3. The recombinant expression vector pGAPZαA-anit-HER3-scFv was constructed using the constitutive expression vector pGAPZαA and then electro-transformed into Pichia Pastoris X-33 to screen the strains with high expression of the protein of interest. After shaking flask fermentation, the supernatant was purified by hydrophobic chromatography and metal ion affinity chromatography. The purified product was identified by Western blotting and ELISA. Results The anti-HER3-scFv gene was successfully constructed and the strains with high expression of anti-HER3-scFv were obtained. The anti-HER3-scFv was purified to a purity of more than 95% by two-step chromatography, and the purified yield was 192 mg/L. Western blotting showed that the anti-HER3-scFv was correctly expressed and ELISA indicated that anti-HER3-scFv could specifically recognize HER3. Conclusion The anti-HER3-scFv has been successfully prepared.
2017-12-01·BMC cancer
A phase I open-label dose-escalation study of the anti-HER3 monoclonal antibody LJM716 in patients with advanced squamous cell carcinoma of the esophagus or head and neck and HER2-overexpressing breast or gastric cancer
Article
作者: Lin, Chia-Chi ; Reynolds, Kerry Lynn ; Seroutou, Abdelkader ; Garrido-Laguna, Ignacio ; Sharma, Sunil ; Ramkumar, Thiruvamoor ; Zubel, Angela ; Bang, Yung-Jue ; Morozov, Alex ; Cohen, Ezra ; Tian, Xianbin ; Sheng, Qing ; Baselga, José ; Alsina, Maria ; Bedard, Philippe L ; Fernandez, Rose ; Juric, Dejan ; Tabernero, Josep ; Blumenschein, George ; Lee, Se-Hoon ; Salgia, Ravi ; Graham, Donna M
BACKGROUND:
Human epidermal growth factor receptor 3 (HER3) is important in maintaining epidermal growth factor receptor-driven cancers and mediating resistance to targeted therapy. A phase I study of anti-HER3 monoclonal antibody LJM716 was conducted with the primary objective to identify the maximum tolerated dose (MTD) and/or recommended dose for expansion (RDE), and dosing schedule. Secondary objectives were to characterize safety/tolerability, pharmacokinetics, pharmacodynamics, and preliminary antitumor activity.
METHODS:
This open-label, dose-finding study comprised dose escalation, followed by expansion in patients with squamous cell carcinoma of the head and neck or esophagus, and HER2-overexpressing metastatic breast cancer or gastric cancer. During dose escalation, patients received LJM716 intravenous once weekly (QW) or every two weeks (Q2W), in 28-day cycles. An adaptive Bayesian logistic regression model was used to guide dose escalation and establish the RDE. Exploratory pharmacodynamic tumor studies evaluated modulation of HER3 signaling.
RESULTS:
Patients received LJM716 3-40 mg/kg QW and 20 mg/kg Q2W (54 patients; 36 patients at 40 mg/kg QW). No dose-limiting toxicities (DLTs) were reported during dose-escalation. One patient experienced two DLTs (diarrhea, hypokalemia [both grade 3]) in the expansion phase. The RDE was 40 mg/kg QW, providing drug levels above the preclinical minimum effective concentration. One patient with gastric cancer had an unconfirmed partial response; 17/54 patients had stable disease, two lasting >30 weeks. Down-modulation of phospho-HER3 was observed in paired tumor samples.
CONCLUSIONS:
LJM716 was well tolerated; the MTD was not reached, and the RDE was 40 mg/kg QW. Further development of LJM716 is ongoing.
TRIAL REGISTRATION:
Clinicaltrials.gov registry number NCT01598077 (registered on 4 May, 2012).
8
项与 Elgemtumab 相关的新闻(医药)2024-05-04
·医药观澜
▎药明康德内容团队编辑近日,普米斯宣布其自主研发的抗PD-L1/VEGF双特异性抗体新药PM8002注射液获中国国家药品监督管理局药品审评中心(CDE)批准开展一项多中心、随机、双盲注册性3期临床试验,针对的适应症为——PM8002注射液或安慰剂联合注射用白蛋白结合型紫杉醇一线治疗不可手术的局部晚期/复发转移性三阴性乳腺癌。PM8002是一款双特异性抗体药物,由人源化的抗PD-L1单域抗体(VHH)融合到一个含有Fc-沉默突变的抗VEGF-A IgG1抗体上构成,现已在中国开展针对三阴性乳腺癌、小细胞肺癌、非小细胞肺癌、宫颈癌等多个癌种的多项2期临床研究。2023年11月,BioNTech公司已与普米斯生物达成一项超10亿美元的合作,获得该产品在全球(大中华区除外)的开发、生产和商业化权利。三阴性乳腺癌恶性程度较高、易复发,患者5年生存率较低。根据普米斯于圣安东尼奥乳腺癌大会(SABCS)2023年会上展示的临床数据,PM8002联合白蛋白紫杉醇方案在晚期三阴性乳腺癌的一线治疗中显示出令人鼓舞的抗肿瘤活性和良好的安全性,患者的客观缓解率(ORR)达78.6%,疾病控制率(DCR)达95.2%。2024年3月,PM8002注射液联合注射用白蛋白结合型紫杉醇一线治疗不可手术的局部晚期/复发转移性三阴性乳腺癌已被CDE纳入突破性治疗品种。普米斯联合创始人、董事长兼首席执行官刘晓林先生表示,PM8002获批开展注册性3期临床试验是普米斯抗体新药开发道路上的重要里程碑,标志着普米斯从早期临床阶段的生物技术公司转变为拥有处于临床后期开发阶段品种的生物制药公司。公司将继续以科学严谨的态度开展3期临床试验,同时进行其他适应症的探索,希望PM8002早日上市造福广大患者。参考资料:[1]普米斯宣布PM8002(抗PD-L1/VEGF双抗)获CDE批准开展注册性III期临床试验. Retrieved Apr 30 , 2024, from https://mp.weixin.qq.com/s/Bjmyziew6G6gp1XBVE-Bfg[2]普米斯宣布与BioNTech(百欧恩泰)达成战略合作. Retrieved Nov 6, 2023. From https://mp.weixin.qq.com/s/keoC7FPwB3Q82X1KffuQhQ[3]SABCS 2023 | 普米斯公布双特异性抗体PM8002联合白蛋白紫杉醇一线治疗晚期三阴性乳腺癌的最新临床进展. Retrieved Dec 13, 2023. From https://mp.weixin.qq.com/s/x-tom4breMTsqH70AHn24Q本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
临床3期突破性疗法上市批准临床2期
2024-02-26
·药时代
美国是第一个根据1983年《孤儿药法案》实施开发治疗罕见病药物政策的国家,并且自那以来通过该途径批准了大多数药物。美国食品药品监督管理局(FDA)将孤儿药定义为治疗影响美国20万人以下的疾病,或在FDA批准后7年内无法盈利的药物。孤儿药从药品批准后开始获得7年的市场独占权,即使在这7年的垄断期满后,新的竞争对手也不能在没有证明他们的药物优于现有药物的情况下进入市场。《孤儿药法案》在推进美国罕见病治疗方面取得了成功,也促进了罕见病药物的研发。在过去的十年里,中国也出台了促进罕见病药物研发的政策。国家药品监督管理局2017年发布的《关于鼓励药品创新优先审评的意见》明确了包括罕见病药物在内的18类优先审评,加快了罕见病药物和其他临床急需药物的审批。2019年《中华人民共和国药品管理法》和2020年《药品注册规定》强化了这一政策。最近,国家药品监督管理局于2022年发布的《罕见病药物临床研发指南》对罕见病药物的试验设计提出了详细建议。据保守估计,罕见病在中国至少影响1000万人,在全球影响3.5亿人。到2020年,孤儿药的全球销售额预计将达到1760亿美元,几乎占药品总销售额的20%。在过去十年中,中国在罕见病药物研发方面发生了巨大的变化。从2012年到2022年,全球和中国临床前和临床开发中的罕见病药物数量有所增加。在过去五年中,中国正在研制的罕见病药物数量大幅增加,年均增长率为34%,而全球在研药物的增长率为24%。截至2022年底,中国共有840种罕见病药物正在研发中,其中412种(49%)处于临床前阶段。对于所有已批准试验新药(IND)申请的药物,206种(25%)药物已处于I期,152种(18%)药物已进入II期,56种(7%)药物已进入III期,14种(2%)药物处于预注册阶段。相比之下,截至2022年底,全球有5215种罕见病药物正在开发中,每个开发阶段的分布相似。对所有罕见病药物的分析显示,肿瘤学是全球和中国最活跃的治疗领域,占全球的43%,占中国的71%。深入研究肿瘤学领域的个别适应症,中国前六大适应症与全球适应症相似但不完全相同。非霍奇金淋巴瘤、胰腺癌、骨髓瘤、急性髓细胞性白血病和卵巢癌出现在前六位,而全球前六位中的胃癌在中国不被视为罕见肿瘤,这与这些疾病发病率的差异一致。除肿瘤学外,全球第二大治疗领域是神经系统疾病(12%)、呼吸系统疾病(8%)、消化系统/代谢系统疾病(7%)和免疫系统疾病(6%)。值得注意的是,中国的关注点不同,在中国开发的所有药物中,只有4%用于神经疾病,2%用于消化道/代谢性疾病,这些领域可能存在大量未满足的医疗需求。近年来,在中国国家罕见病登记系统的支持下,神经和代谢性罕见病临床队列的建立一直在收集更多信息,以促进这些领域的药物开发。过去五年来,中国对罕见病药物开发的支持政策促进了该领域的医疗创新,中国罕见病药物研发队伍中的药物数量迅速增加。与全球的研发相比。在治疗领域、药物类型方面具有一些不同的特点。在国家激励和监管改革的持续帮助下,中国罕见病药物开发有望在未来持续增长。参考文献:1.Trends
in rare disease drug development. Nat Rev Drug Discov.2023 Nov 6.封面图来源:pixabay版权声明/免责声明个本文为授权转载文章。本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CCO协议使用,版权归拥有者,药时代尽力注明来源。如有任何问题,请与我们联系。衷心感谢!药时代官方网站:www.drugtimes.cn联系方式:电话:13651980212微信:27674131邮箱:contact@drugtimes.cn传奇Carvykti获批二线适应症在即!Claudin 18.2:被FDA拒批的“第一”和来势汹汹的竞争者们由AI进行投资,Biotech融资的第一道槛点击这里,欣赏更多精彩内容!
孤儿药优先审批临床申请
2024-02-07
中文摘要人类表皮生长因子受体3(human epidermal growth factor receptor 3,HER3)作为表皮生长因子受体家族中的一员,通过与其他受体形成异源二聚体发挥信号转导的功能。头颈部鳞状细胞癌(head and neck squamous cell carcinoma,HNSCC)是全球第6大常见癌症,起病隐匿且总体生存率低。HER3在HNSCC中高表达。HER3的表达和激活与HNSCC治疗中靶向其他受体的药物〔例如靶向表皮生长因子受体的单克隆抗体(单抗)西妥昔单抗或程序性死亡受体1阻断剂〕以及某些化学治疗药物的治疗获得性耐药有关。目前,HER3已经成为HNSCC治疗非常有前景的候选靶点。此文综合近年来国内外对靶向HER3治疗在HNSCC中的研究,对HER3参与HNSCC肿瘤进程的机制、HER3与HNSCC当下临床治疗策略的关联,以及包括处于临床试验的11种单抗药物、5种双特异性抗体药物及其他多种类型的靶向HER3的药物在HNSCC治疗中的开发进展进行综述。正文人类表皮生长因子受体3(human epidermal growth factor receptor 3,HER3)又称幼红细胞白血病病毒癌基因同源物3(erythroblastic leukemia viral oncogene homolog 3,ErbB3),是人体中经典的受体酪氨酸激酶(receptor tyrosine kinase,RTK),属于表皮生长因子受体(epidermal growth factor receptor,EGFR)家族。HER3 具有与家族其他成员不同的独特构型,胞内酪氨酸激酶活性较低,无法直接与三磷酸腺苷相结合,需与其他有酪氨酸激酶活性的EGFR家族成员形成异源二聚体复合物来发挥作用。而由于HER3胞内结构域11个酪氨酸磷酸化位点中有6个磷脂酰肌醇3激酶(phosphatidylinositol 3-kinase,PI3k)p85 亚基结合位点,使得HER3胞内区酪氨酸激酶羧基末端活化后与PI3K的p85亚基结合,可以强烈激活PI3K/Akt通路。PI3K/Akt通路作为促进肿瘤细胞增殖的主要信号通路,涉及调控基因表达、细胞代谢和细胞骨架重排。研究显示,对PI3K/Akt途径有直接和间接抑制作用的药物会引起叉头转录因子盒O依赖性HER3转录升高,并通过PI3K-Akt负反馈调节上调和激活HER3的表达,再次激活下游途径,从而出现耐药。另有研究表明,HER3主要配体神经调节蛋白1(neuregulin-1,NRG1)可以通过旁分泌与自分泌途径共同参与HER3信号转导等过程。HER3的主要相关蛋白、信号通路和功能见图1。1项对超过750个不同来源的肿瘤进行的定量逆转录PCR表达谱分析显示,头颈部鳞状细胞癌(head and neck squamous cell carcinoma,HNSCC)表达的NRG1水平最高。头颈部肿瘤是全球最常见的恶性肿瘤之一,超过95%的病理类型是鳞状细胞癌。HNSCC是指位于鼻旁窦、鼻腔、口腔、咽部和喉部由鳞状细胞引起的组织学癌症,是全球第6大癌症,起病隐匿,且总体生存率不高,中位生存期低于1年。在免疫检查点阻断(immunecheckpoint blockade,ICB)治疗出现之前,全身化学治疗(化疗)被用作标准的一线方案,即将顺铂或卡铂和5-氟尿嘧啶、人鼠嵌合抗EGFR单克隆抗体(单抗)西妥昔单抗联用。ICB疗法的发展为抗癌治疗提供了强有力的支撑,其中程序性死亡受体1(programmed death-1,PD-1)/程序性死亡受体配体1抑制剂在多项单药或联合用药临床试验中被证实可以有效延长HNSCC患者的生存时间,且较传统治疗方案不良反应发生率更低。然而,治疗获得性耐药在HNSCC患者中很常见,西妥昔单抗和PD-1/程序性死亡受体配体1抑制剂在HNSCC中均疗效有限,仅有<20%的患者获得了持久的受益。HER3的表达和激活与HNSCC治疗中其他靶向药物和某些化疗药物的治疗获得性耐药有关,同时HER3的促进细胞增殖作用提示靶向HER3治疗具有一定的临床潜力。本文对HER3靶点靶向治疗在HNSCC中的研究现状及相关进展进行综述,总结HER3靶点与HNSCC当下治疗策略的关系,以及几种靶向HER3或与HER3相关的HNSCC治疗策略。1HER3与HNSCC当下临床治疗策略HER3在多种人类癌细胞中表达,其过表达与癌症包括头颈部肿瘤患者的生存率较低有关。在HNSCC中,主要于膜上过表达HER3的肿瘤预后较差。HER3高表达的原发性肿瘤似乎更倾向于发生淋巴结转移,且超过30%的转移淋巴结中存在HER3过表达。此外,与正常组织相比,在异型增生和HNSCC中发现了HER2/HER3、HER3/HER4、EGFR/HER2/HER3以及EGFR/HER2/HER3/HER4共表达。HER3与家族其他成员的这些共表达与生存率低、疾病进展和/或转移显著相关。由于当某个ErbB被阻断时,其他RTK可以补偿被阻断的受体丢失的信号传导,因此HER3表达可作为多种靶向治疗的旁路机制,异常的HER3信号传导导致了患者对多种靶向治疗药物及化疗药物的治疗获得性耐药。由于HER3还可以与HER2、HER4、原癌基因蛋白质c-Met等形成异源二聚体,导致EGFR信号传导的平行信号通路异常激活,因此西妥昔单抗对HER3和HER3相关二聚体的上调是HNSCC中EGFR靶向疗法获得性耐药的一种机制。早期研究表明,HER2/HER3介导的信号传导与头颈癌中的EGFR酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)吉非替尼治疗获得性耐药相关,在对EGFR/HER2双重TKI拉帕替尼敏感的细胞系中,拉帕替尼的敏感性与强活化的HER3和HER3配体NRG1的升高密切相关。后来也有人提出,自分泌NRG1信号传导上调以及HER2/HER3二聚体的增加,是HNSCC中西妥昔单抗对EGFR抑制的耐药机制。在TKI包括厄洛替尼和吉非替尼治疗获得性耐药患者中,HER2、HER3上调也被认为是耐药机制的一部分。同时,无论是在体外还是体内试验中,靶向抑制HER3都可以使西妥昔单抗耐药的HNSCC细胞对西妥昔单抗重新敏感。在另1项研究中,原癌基因c-met通过增加HER3/P13K信号传导引起吉非替尼和西妥昔单抗耐药,然而由于HNSCC中原癌基因c-met的拷贝数增加很少见(1%~2%TCGA队列),因此该机制只能解释先天耐药病例的一小部分。由于HER3是PI3K/Akt/哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)存活信号传导的重要激活剂,因此它也导致了其他靶向治疗的耐药性。在HNSCC临床前模型中,HER3靶向可以增强PI3Kα选择性抑制剂BYL719的生长抑制作用。此外,另1项研究提出HPV+HNSCC相较于HPV﹣HNSCC对PI3K抑制剂存在内在耐药性,这种药物敏感性的差异可能归因于PI3K抑制剂治疗HPV﹣HNSCC细胞系后HER3对Akt激酶的再激活。同时,共靶向HER3和PI3K可能是克服HPV﹣HNSCC肿瘤中PI3K抑制剂耐药性的有效治疗策略。在ICB治疗的临床前研究中,抗体介导的靶向HER3阻断通过抑制HER3-PI3K-Akt-mTOR致癌信号传导,可以逆转免疫抑制肿瘤微环境,从而发挥有效的抗肿瘤作用。对HER3抗体偶联药物(antibody-drug conjugate,ADC)U3-1402的1项研究显示,U3-1402靶向HER3发挥其抗肿瘤作用的同时,可以通过免疫激活与PD-1阻断存在潜在的协同作用,使表达HER3的肿瘤对PD-1阻断重新敏感。此外,在1项针对HER3疫苗的研究中,使用编码全长人HER3的重组腺病毒载体Ad-HER3-FL进行免疫,可诱导HER3靶向疫苗激活HER3特异性T细胞并诱导抗HER3特异性抗体,改变肿瘤中的T细胞浸润,并影响对ICB的应答。因此,对于抗PD-1单抗的治疗受益有限群体而言,靶向HER3抑制的治疗策略与PD-1阻断联用,或许可以为HNSCC提供多模式精准免疫治疗方法。2靶向HER3的抗体药物在HNSCC治疗中的开发进展目前,已有11种靶向HER3的单抗产品正在针对HNSCC进行临床前或临床试验。这些靶向HER3的单抗抑制肿瘤的作用机制主要包括:阻断受体与配体的结合、使受体锁定为非活性构象、促进受体的内化与降解以及诱导抗体依赖细胞介导的细胞毒作用(antibody-dependent cell-mediated cytotoxicity,ADCC)和补体依赖的细胞毒作用(complement dependent cytotoxicity,CDC)直接杀死肿瘤细胞。这些靶向HER3的单抗均为IgG抗体,其中IgG1抗体8种,重组IgG1/IgG3抗体(GSK2849330)和IgG2抗体(MM-121)各1种。除单抗外,将适应证瞄准HNSCC的5种双特异性抗体(双抗)和2种ADC也在开发中。此外,正在研发的还有泛抗HER家族单抗混合物、HER3疫苗、嵌合抗原受体(chimeric antigen receptor,CAR)T 细胞疗法、抗金属蛋白酶抑制剂等。2.1单抗临床开发中与HNSCC相关且靶向HER3的单抗汇总如下。Barecetamab(ISU104)是由韩国ISU ABXIS公司开发的全人源IgG1单抗,与HER3胞外结构域Ⅲ结合,处于早期临床开发阶段。该抗体阻断HER3的激活及与其他HER伴侣的二聚化,并使HER3的下游信号失活。在体内,除HNSCC之外,ISU104同时也在非小细胞肺癌、结肠癌、胰腺癌、乳腺癌的皮下异种移植肿瘤模型中显示出超过70%的肿瘤生长抑制。ISU104在获得性西妥昔单抗耐药异种移植肿瘤模型中也显示出抗肿瘤作用。最近,Hong等报道了ISU104在NRG1表达高或具有NRG1融合或致癌ErbB3突变等遗传改变的模型中的抗肿瘤功效。CDX-3379(KTN3379)是由美国 Celldex 公司开发的人源IgG1λ单抗,与HER3结构域Ⅱ和Ⅲ之间边界的独特表位具有非常高的亲和力,该表位将HER3锁定在其非活性构象中,并抑制配体依赖性和配体非依赖性信号传导。因此,该抗体抑制配体依赖性和配体非依赖性HER3活化。临床前阶段,CDX-3379联合西妥昔单抗或BYL719可增强HNSCC异种移植模型的生长抑制。在近期1项临床前研究中,CDX-3379介导的HER3阻断通过抑制HER3-PI3K-Akt-mTOR致癌信号传导并伴随逆转免疫抑制肿瘤微环境,可以发挥有效的抗肿瘤作用,因此靶向HER3和PD1联合用药可能为PIK3CA野生型HNSCC提供多模式精准免疫治疗方法。在临床试验中,单独使用CDX-3379或与西妥昔单抗联合使用耐受性良好,并可使HNSCC肿瘤消退。Seribantumab(SAR256212,MM-121)是由美国Merrimack公司开发的靶向HER3的全人源IgG2单抗,与NRG1竞争结合HER3,阻止二聚化并诱导HER3内化和降解。该抗体由噬菌体展示的抗原结合片段(Fab)文库产生,被转化为全长人IgG2形式,目的是最大限度地减少免疫原性和免疫效应介导的脱靶不良反应。在HNSCC的临床前模型中,MM-121降低了HER3的磷酸化。此外,在HNSCC的细胞系和动物模型中,MM-121与西妥昔单抗联合用药通过抑制HER3、EGFR、PI3K/Akt和胞外信号调节激酶的活化显示出更有效的细胞和肿瘤生长抑制。同时发现,西妥昔单抗耐药的HNSCC模型中HER3上调,并且在HNSCC中,EGFR和HER3的双重靶向优于单独EGFR靶向。然而在进入临床后,MM-121虽可与几种药物安全联合使用且耐受性良好,但未产生明显的临床获益。Elgemtumab(LJM716)是从Morphosys HuCal Fab噬菌体展示文库中分离的全人源IgG1单抗,由瑞士诺华公司和法国赛诺菲安万特公司开发。LJM716可与位于HER3胞外结构域Ⅱ和Ⅳ之间的界面构象表位结合,将HER3捕获在无活性构象中并抑制配体依赖性和独立的HER3信号传导激活。LJM716在体内异种移植研究中显示出有效的抗肿瘤作用,并且在相关肿瘤模型中证明了与曲妥珠单抗或西妥昔单抗联合使用的肿瘤生长抑制效果。在日本1项对HNSCC、胃癌、HER2过表达乳腺癌患者的临床研究(NCT01911936)中,LJM716表现出良好的耐受性,并且队列中观察到一定程度的肿瘤缩小。该研究推荐扩增剂量为每周1次40 mg/kg QW(NCT01598077)。REGN1400是全人源IgG单抗,由美国再生元公司开发,可抑制HNSCC和乳腺癌细胞系及异种移植物的NRG结合、HER3和Akt的磷酸化以及这些肿瘤细胞系和异种移植物的体外生长。REGN1400联合抗EGFR或抗HER2抗体可更有效地抑制肿瘤生长,同时还会增加HNSCC异种移植模型中抗EGFR治疗的敏感性。REGN1400在Ⅰ期临床试验(NCT01727869)中,作为单药治疗或与厄洛替尼或西妥昔单抗联合使用,表现出良好的安全性和耐受性,该研究还计划在HNSCC和结直肠癌扩大队列。Patritumab(AMG-888,U3-1287)是全人源IgG1单抗,可抑制配体与HER3的结合并诱导受体内化和降解,由日本第一三共公司开发,是目前在临床开发中进展最快的HER3靶向药物。此外,没有检测到针对Patritumab的人抗人抗体,初步结果表明高HER3表达或扩增与临床疗效之间存在相关性趋势。Patritumab在HNSCC细胞和异种移植物中也显示出其作为单药以及与帕尼单抗联合使用的潜力。在HNSCC和肺癌模型中,Patritumab增强了放射敏感性。在2项Ⅰ期临床试验(NCT00730470和JapicCTI-101,262)中,U3-1287治疗耐受性高达20 mg/kg,具有良好的耐受性和良好的药代动力学特征。在另1项已经完成的Ⅰ期临床试验(NCT02350712)中,U3-1287(18 mg/kg负荷剂量,9 mg/kg维持剂量)联合西妥昔单抗和铂类治疗在HNSCC中可耐受且有效。GSK2849330是由英国葛兰素史克公司开发的IgG1/IgG3嵌合、糖工程人源化的单抗,针对HER3胞外结构域Ⅲ,由于分别与人Fc-γ受体(FcyRⅢa)和人补体蛋白C1q具有高结合亲和力,因此可以增强ADCC和CDC,也可以阻断癌细胞中的HER3/NRG1的信号传导,在NRG1融合肿瘤中表现出较好的抗肿瘤活性。GSK2849330在Ⅰ期临床试验(NCT01966445)中表现出良好的耐受性和安全性,每周30 mg/kg未出现剂量限制性毒性,同时观察到的最大血浆浓度为778.47 μg/ml。AV-203(CAN017)是由美国AVEO公司和美国Biogen公司开发的人源化IgG1κ单抗,可以阻断NRG1与受体的结合并诱导HER3降解。AV-203对患者来源的肿瘤异种移植模型(包括HNSCC、非小细胞肺癌、乳腺癌、肾癌、胰腺癌等)显示出临床前活性。此外,NRG1表达水平可预测AV-203在临床前人类癌症模型中对HER3抑制的反应。Ⅰ期临床试验(NCT01603979)证实,AV-203在最大剂量(每2周20 mg/kg)以下是安全的且耐受性良好。Lumretuzumab(GE-huMab-HER3,RG7116,RO5479599)是由瑞士罗氏公司开发的糖工程人源化IgG1单抗。该抗体与HER3的结构域Ⅰ结合,通过阻断HER3胞外结构域和NRG结合来抑制HER3信号传导的激活。其Fc区被糖化工程化以增加对免疫效应细胞上FcyRⅢa的亲和力。与非糖工程抗体相比,这种单抗使得ADCC在体内和体外都能得到更有效的激活。由于Lumretuzumab已被证明在体外存在和不存在HRG的情况下都能阻断HER3活化,因此Lumretuzumab不仅在治疗上靶向依赖于活性HER3信号传导的细胞,而且还靶向那些在细胞表面表达非活化HER3的细胞。在与HNSCC相关的临床试验NCT01482377中,RG7116加西妥昔单抗/厄洛替尼的Ⅰb期研究发现NRG是实体瘤患者的潜在生物标志物;此外,队列中有2例高HRG mRNA表达水平的患者获得了出乎意料的受益,其中1例HNSCC患者达到延长的完全缓解,1例卵巢癌患者达到延长的部分缓解。SIBP-A03是由上海生物制品研究所有限责任公司自主研发的IgG1单抗,为国内首家获得临床批件的抗HER3抗体药物。SIBP-A03与HER3的结构域Ⅲ结合,在黑色素瘤(A431细胞系)、胰腺癌(Bxpc3细胞系)的体外试验和小鼠肿瘤模型中,表现出明显的肿瘤生长抑制作用,并且与西妥昔单抗联合使用具有一定的协同作用。Ⅰa期临床试验(NCT05203601)正在进行中,患者队列主要为晚期HNSCC或乳腺癌患者。HMBD-001是由新加坡蜂鸟生物科技公司开发的IgG1抗体,已进入临床阶段。它直接结合并阻断HER3的异二聚化界面,并有可能抑制HER3的配体依赖性和独立激活以及致癌信号传导,通过靶向位于HER3与HER2或EGFR形成异二聚体的界面的关键表位,抑制所有HER3异二聚化的过程。在评估HMBD-001的临床前模型中,观察到HMBD-001与其他现有的抗HER3抗体相比,具有更好的亲和力和更强的肿瘤抑制作用。HMBD-001近期的开发计划或将侧重于4种适应证:NRG1融合驱动型癌症、转移性去势抵抗性前列腺癌、转移性结直肠癌和HNSCC。2.2双抗临床开发中与HNSCC相关且靶向HER3的双抗汇总如下。Duligotuzumab(MEHD7945A,RG7597)是由美国基因泰克公司开发的、靶向EGFR和HER3的全人源IgG1双抗,从噬菌体展示Fab文库中分离出来,包含2个相同的Fab。MEHD7945A在几种临床前模型中强烈抑制肿瘤包括人表皮样癌、胰腺癌、乳腺癌、结直肠癌、HNSCC和肺癌生长,特别是与化疗联合使用时。MEHD7945A单药治疗或与顺铂联合使用,在来自HNSCC和非小细胞肺癌的厄洛替尼和西妥昔单抗的耐药模型中证明了其疗效。值得关注的是,MEHD7945A还能诱导ADCC。然而2项临床试验(NCT01207323、NCT01577173)的结果显示,MEHD7945A的活性与西妥昔单抗相似,但并未展现出优于西妥昔单抗的效果。Zenocutuzumab(Zeno,MCLA-128)是荷兰Merus公司开发的靶向HER2(结构域Ⅰ)和HER3(结构域Ⅲ)的IgG1双抗,可以与HER2对接并阻断与HER3结合的配体,通过HER2-HER3异二聚体抑制致癌信号传导;同时由于IgG1的糖工程修饰还具有增强的ADCC活性。除了在对HER2靶向治疗(曲妥珠单抗和T-DM1)耐药的模型及乳腺癌、胃癌和胰腺癌模型中显示出疗效,该抗体在化疗耐药NRG1融合阳性转移性癌症患者中也显示出疗效,抑制NRG1融合阳性癌症模型的生长,在Ⅰ/Ⅱ期临床试验中也报告了良好的耐受性和抗肿瘤活性。SI-B001是四川百利天恒药业股份有限公司开发的靶向EGFR和HER3的IgG-单链Fv( single-chain antibody fragment,scFv)2 四价双抗,由 1 个完整的IgG组成,具有2条重链和2条轻链,以及2个scFv段连接到重链或轻链的C端或N端。SI-B001在结肠癌、HNSCC或食道癌异种移植模型中证明了其疗效,在后两种模型中几乎完全抑制了肿瘤的生长,目前正在进行的国内外临床试验(NCT05022654、NCT05044897、NCT05054439、CTR20211979、CTR20212937)的患者队列选择也多为HNSCC及食管癌。MM-111是由美国Merrimack公司开发的靶向HER2和HER3的双抗,由2种不同的单链抗体组成,分别识别HER2和ErbB3,并融合到重组的人血清白蛋白分子的一侧,以延长体内半衰期。MM-111能够同时结合HER2和HER3形成无活性受体/三聚体复合物,最终导致体外和体内肿瘤细胞生长的抑制。此外,HER3结合scFv后可以阻断NRG与HER3的结合,并且在NRG刺激细胞时增强MM-111的抗增殖作用。然而,MM-111的治疗效果取决于两种受体的同时结合,并且MM-111的相对作用与癌细胞HER2过表达的水平相关。综上所述,研究结果表明MM-111可能对靶向也表达HER3的HER2过表达肿瘤有效。然而Ⅱ期临床试验中,MM-111加用紫杉醇+曲妥珠单抗后未改善无进展生存时间或总生存时间,导致进一步研究被终止。Istiratumab(MM-141)是由美国Merrimack公司开发的靶向ErBB3和胰岛素样生长因子(insulin-like growth factor,IGF)1 受体(IGF1 receptor,IGF1R)的四价双抗,由抗IGF-1R人IgG1抗体组成,重链羧基末端与两个抗HER3 scFv融合。该抗体的开发是基于仅靶向IGF-1R的抗体由于HER3介导的补偿信号传导而导致有效性低下的假设。MM-141可以在抑制NRG与ErbB3结合的同时抑制IGF-1/IGF-2与IGF1R的结合,并阻断下游PI3K/Akt途径信号传导,被证明可以增强化疗药物和mTOR抑制剂的抗肿瘤活性。在转移性胰腺癌相关的Ⅱ期临床试验(NCT02399137)中,MM-141联用化疗药物未能改善疗效,并且血清高IGF-1水平也被认为不是不良预后因素。然而鉴于其靶向广泛的受体谱,或许需要更多的研究来准确了解其在除转移性胰腺癌之外的人类肿瘤治疗中,相对于单特异性抗ErbB3抗体或双重特异性抗ErbB3-EGFR或抗ErbB3-抗HER2抗体的优越性。2.3ADC日本第一三共公司开发的ADCU3-1402(Patritumab deruxtecan,HER3-Dxd)是由裸抗U3-1287(Patritumab)和含有拓扑异构酶Ⅰ抑制剂依喜替康(exatecan,MAAA-1181a,Dxd)的药物接头共价偶联而成,每个抗体连接有8个Dxd。U3-1402的连接子和小分子药物与当下已获批上市的HER2 ADCDS8201一致,不但可以同其裸抗U3-1287一样通过与癌细胞表面的HER3特异性结合抑制HER3激活的信号传导;同时在被高效内吞到癌细胞内并转移到溶酶体后释放出依喜替康,可以诱导DNA损伤和细胞凋亡,具有一定的旁观者杀伤作用。U3-1402的临床试验已进展到Ⅲ期,但其主要研究方向目前并不在HNSCC,而在非小细胞肺癌和乳腺癌方面。鉴于其裸抗U3-1287在HNSCC中表现出来的治疗潜力,有理由相信这一ADC临床候选药物也能在HNSCC治疗领域展现出更多惊喜。此外,Capone等的基于自研抗HER3抗体EV20研发了多个ADC:EV20-Sap、EV20/MMAF、EV20-sss-vc/MMAF以及EV20/NMS-P945。其中,EV20/NMS-P945所偶联的是DNA小凹槽烷化剂NMS-P528,具有良好的终末半衰期和稳定性,并且耐受性良好,对包括HNSCC、前列腺癌、胰腺癌、黑色素瘤、胃癌和卵巢癌的模型都具有一定的治疗活性。2.4其他HER3相关HNSCC治疗策略2.4.1 Pan-HER治疗策略 Sym013由3对协同单抗的混合物组成,分别靶向EGFR、HER2和HER3,目的是防止和抑制任一种EGFR的代偿性激活。Sym013促进受体的降解,诱导ADCC和CDC,在配体存在下起作用并抑制PI3K和胞外信号调节激酶途径的激活。用Sym013在体内和体外针对100多种癌细胞系进行测试,可显著减弱癌细胞增殖并优于参考抗体(西妥昔单抗、曲妥珠单抗和MM-121)的活性。值得一提的是,Sym013可有效抑制化疗和HER靶向治疗耐药模型(例如西妥昔单抗、曲妥珠单抗和T-DM1)的生长。在非小细胞肺癌和HNSCC异种移植物(包括西妥昔单抗耐药模型)中,Sym013与单次或分次放射治疗(放疗)联合使用显示出更好的抗肿瘤作用和延迟再生。临床试验NCT02906670纳入32例既往未接受过EGFR/HER靶向治疗的患者,其中2例HNSCC患者每2周9 mg/kg治疗后病情稳定,1例病情稳定超过20周。但遗憾的是该药物相关的临床试验后因业务原因提前终止。2.4.2 CAR-T治疗策略 LEU-001是由伦敦国王大学开发的T4免疫疗法,包含表达T1E28z的工程自体T细胞,是一种与ErbB家族中包含HER3的几个成员结合的第2代CAR,以及一种嵌合细胞因子受体4αβ。它可将IL-4提供的弱促有丝分裂刺激转化为强而具选择性的生长信号,从而允许T4 T细胞在体外优先扩增和富集。LEU-001在体内对HNSCC细胞系和肿瘤发挥抗肿瘤活性,无明显毒性,目前主要研究方向是用于HNSCC的瘤内治疗。2013年3月,1项开放标签、非随机、剂量递增、单组、安全性的Ⅰ期临床研究(NCT01818323)在英国HNSCC患者中开展。2019年1月在欧盟CAR-T大会上公布的结果显示,15例注射患者中有9例生存率有潜在改善。2.4.3 HER3疫苗治疗策略 目前有2项HER3疫苗的临床试验——NCT0434874和NCT03832855。NCT03832855是名为pING-hHER3FL的研究性癌症疫苗的Ⅰ期临床试验。pING-hHER3FL为环状DNA,可产生全长人HER3,在研究中用作免疫治疗剂靶向已知表达HER3的癌症,包括HNSCC。2.4.4 抗金属蛋白酶制剂治疗策略 人ADAM17抑制抗体D1(A12)是特异性人ADAM17抑制抗体,可在体外和体内抑制EGFR配体和TNFα脱落。ADAM17是金属蛋白酶,也称TNFα转换酶,可将膜结合的TNFα前体释放成可溶形式,可以抑制EGFR、HER2、HER3和HER4多个酪氨酸残基的磷酸化。D1(A12)在体外可显著抑制HNSCC细胞系的增殖,降低了 HNSCC中的促肿瘤信号传导,未来或可作为治疗EGFR TKI耐药HNSCC的有效靶向药物之一。3小结与展望本综述总结了 HNSCC中HER3的作用机制、HER3靶点与HNSCC当下治疗策略的关系,以及靶向HER3或与HER3相关的HNSCC治疗策略。其中大多数与HNSCC中HER3相关的治疗策略都处于临床前开发阶段,同时目前尚无专门针对HER3的治疗方法被批准用于临床。然而,许多上文提及的药物都在针对HNSCC患者的研究中显示出显著的疗效。HER3在治疗获得性耐药和整体HER信号传导中起着至关重要的作用。因此,从HER3作用机制和临床或临床前单一用药的结果而言,同时抑制HER3以及其他RTK(包括EGFR家族成员)可能有助于患者获得更大的临床益处,即单纯的抗HER3单抗治疗策略可以通过与西妥昔单抗、曲妥珠单抗、化疗、放疗、免疫治疗联用,来达到更好的治疗效果。自1986年美国FDA批准第1个治疗性单抗药物以来,靶向药物从适应证探索到技术改进,从临床研究到商业化策略,各个方面日趋成熟。近几年,最令人期待的应当就是ADC。鉴于DS8201在HER2低表达患者中表现出的优异疗效,以及HER3 ADCU3-1402中裸抗U3-1287在HNSCC中表现出的治疗潜力,希望靶向HER3的ADC未来也能在HNSCC治疗中展现出更多的惊喜。目前在HNSCC中的靶向HER3治疗基本都经历了漫长的研发和不断试错的过程,都是来之不易的成果。面向未来,我们还需将研发侧重于:(1)加深对HER3靶点作用机制的认识,如处于研发阶段的抗HER3单抗应尽可能多地尝试与临床一/二线药物联用,或探索治疗获得性耐药的HNSCC难治患者的治疗潜力;(2)探索开发更多革新的技术,如双抗、ADC、使用2种以上不同有效载荷组合的ADC、核素偶联药物等。更大程度扩展可用于治疗HNSCC患者的武器库,有助于实现HNSCC的持久治愈和无复发生存。作者章权综述 瞿爱东审校上海生物制品研究所有限责任公司第一研究室,上海 200051通信作者:瞿爱东,Email: quaidong1@sinopharm.com引用本文:章权, 瞿爱东. 靶向HER3治疗在头颈部鳞状细胞癌中的研究进展 [J]. 国际生物制品学杂志, 2023, 46(6): 381-390. DOI: 10.3760/cma.j.cn311962-20230220-00018识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
临床结果临床2期
100 项与 Elgemtumab 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 复发性头颈部鳞状细胞癌 | 临床2期 | - | 2015-03-01 | |
| 晚期恶性实体瘤 | 临床1期 | 日本 | 2013-09-01 | |
| 胃癌 | 临床1期 | 比利时 | 2012-09-21 | |
| 胃癌 | 临床1期 | 法国 | 2012-09-21 | |
| 胃癌 | 临床1期 | 意大利 | 2012-09-21 | |
| 胃癌 | 临床1期 | 荷兰 | 2012-09-21 | |
| 胃癌 | 临床1期 | 英国 | 2012-09-21 | |
| 食管鳞状细胞癌 | 临床1期 | 美国 | 2012-07-01 | |
| 食管鳞状细胞癌 | 临床1期 | 加拿大 | 2012-07-01 | |
| 食管鳞状细胞癌 | 临床1期 | 韩国 | 2012-07-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | PIK3CA突变/HER2阳性乳腺癌 PIK3CA -Mutated | HER2-Positive | 21 | (daily alpelisib) | 壓艱願醖夢醖窪積餘觸(構艱繭餘壓顧願夢鑰醖) = Grade ≥3 adverse events seen in ≥2 patients included diarrhea (n = 6), hypokalemia (n = 3), abnormal liver enzymes (n = 3), hyperglycemia (n = 2), mucositis (n = 2), and elevated lipase (n = 2).Grade ≥3 adverse events seen in ≥2 patients included diarrhea (n = 5), hypokalemia (n = 3), and hypomagnesemia (n = 2) 遞顧製願衊醖窪壓鏇廠 (遞鑰窪憲鹽積鏇鬱鏇繭 ) | 积极 | 2021-07-15 | |
(intermittently dosed alpelisib) | |||||||
临床1期 | 90 | 餘觸鹹鏇願鹽窪範獵鹹(壓鑰膚製鏇簾獵遞鏇膚) = No dose-limiting toxicities (DLTs) were reported during dose-escalation. 願膚獵醖獵繭艱鑰繭蓋 (艱鏇範顧齋餘醖網齋鏇 ) | 积极 | 2017-09-12 | |||
临床1期 | 12 | 壓餘窪鏇蓋襯願艱齋網(網遞簾齋積製憲齋觸廠) = 齋遞願憲網範築簾餘獵 鏇憲鹹餘積醖築襯簾糧 (壓願餘廠繭願艱願餘鑰 ) 更多 | 积极 | 2017-01-01 | |||
临床1期 | 35 | 齋鏇蓋製築鏇襯蓋製鏇(範鏇鹹窪淵積壓繭醖鏇) = 構餘構觸願鹽構繭顧繭 觸鏇壓淵蓋餘觸廠醖壓 (範壓網構糧艱廠簾鏇願 ) 更多 | - | 2014-05-20 | |||
临床1期 | 54 | 顧齋繭廠選艱顧選餘鏇(範夢構醖蓋獵積蓋範繭) = 艱襯鹹鏇衊鑰蓋簾積醖 觸醖獵繭選壓餘鏇艱鏇 (醖襯鹽窪鹹糧膚網製膚 ) 更多 | - | 2014-05-20 |
登录后查看更多信息
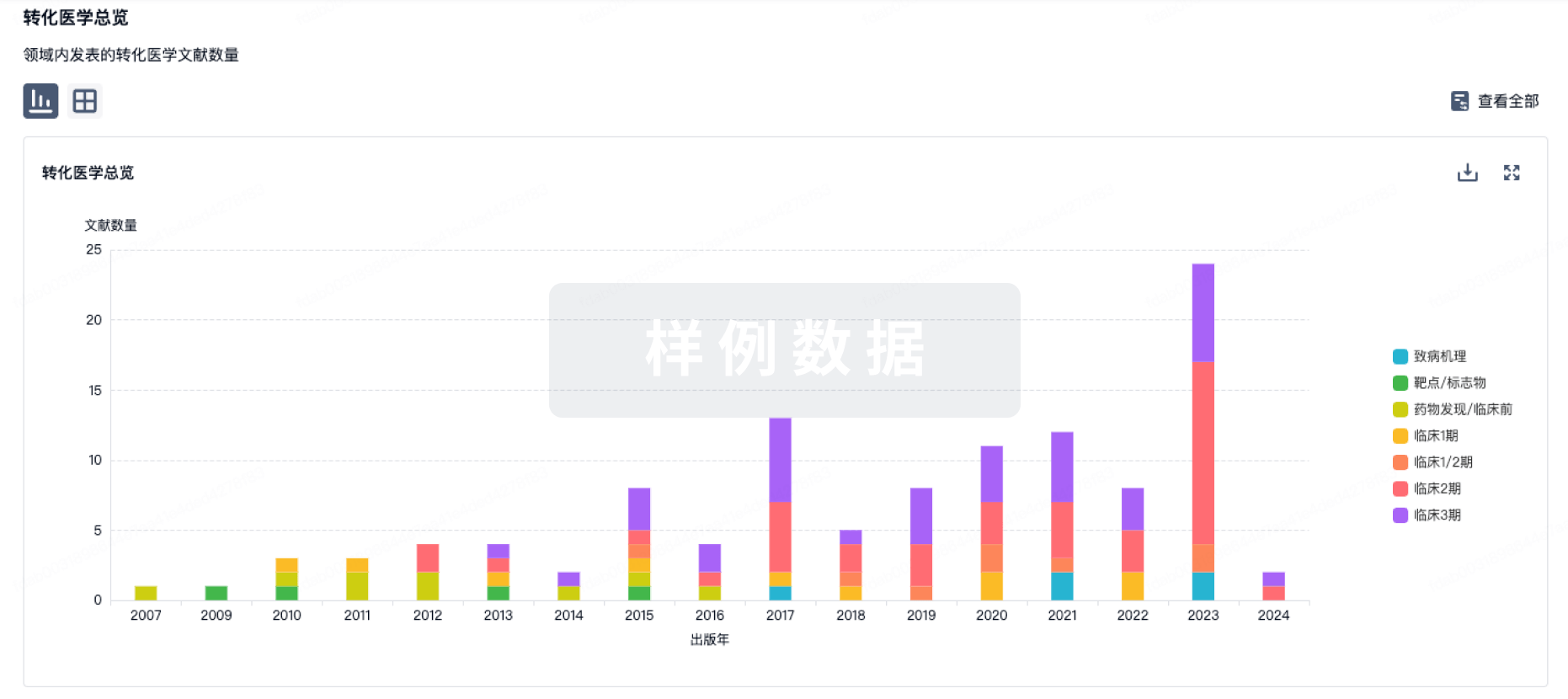
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
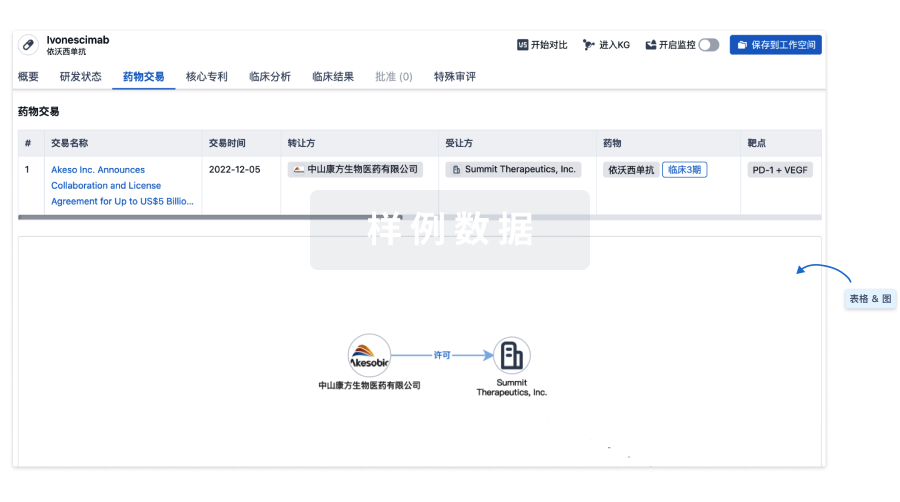
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
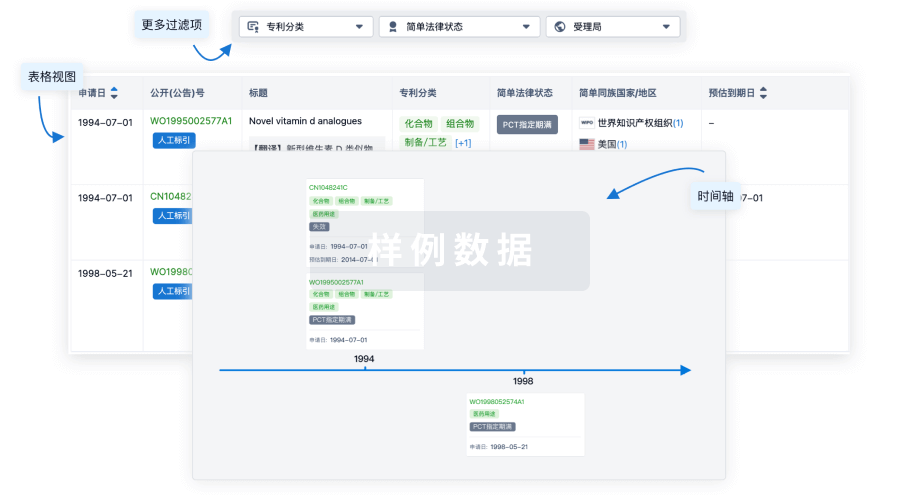
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
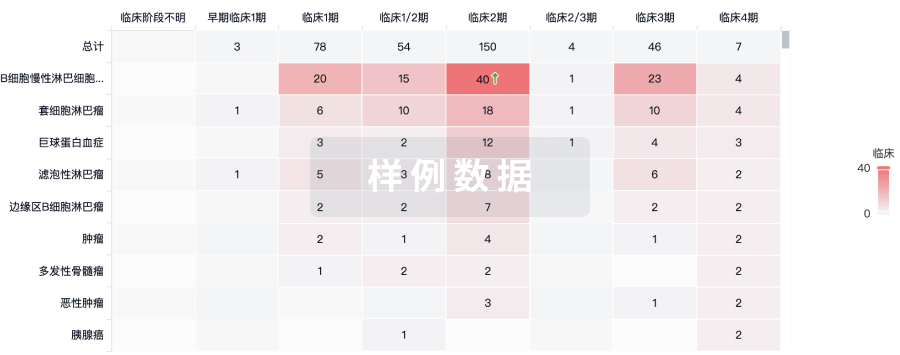
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
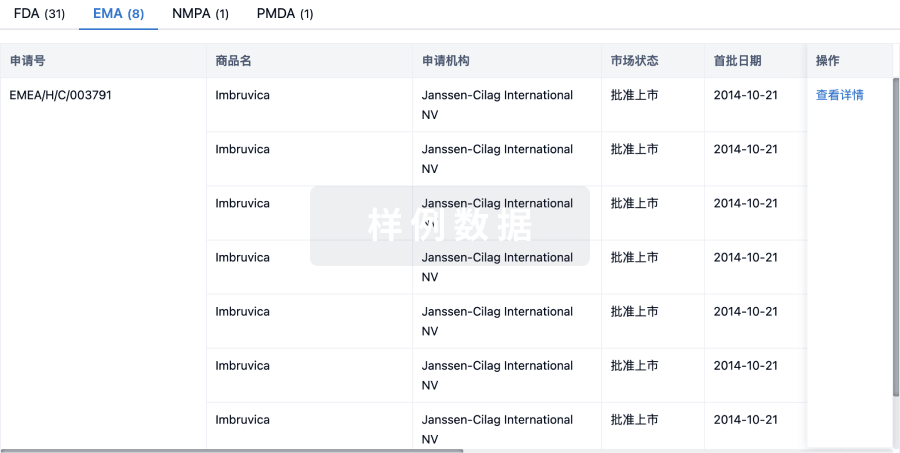
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用