BMS PD-1抑制剂纳武利尤单抗皮下注射剂首个III期临床研究数据公布,针对肾细胞癌
2024年1月27日,百时美施贵宝首次披露皮下注射PD-1纳武利尤单抗(nivolumab,Opdivo)治疗晚期或转移性透明细胞肾细胞癌(ccRCC)患者的III期CheckMate-67T研究数据。这也是BMS公布的首个纳武利尤单抗皮下注射制剂III期临床试验结果。
纳武利尤单抗(欧狄沃)是一种PD-1免疫检查点抑制剂,它通过与免疫细胞上的PD-1结合,阻止PD-1与PD-L1结合,进而重新激活患者自身免疫细胞来杀伤肿瘤。该药2014年12月获得美国食品和药物管理局(FDA)批准上市,2018年6月15日在中国获批上市,目前已在超过60个国家获批上市,适应症涵盖十余个癌种。2022年,该药全球销售额达到92.94亿美元,有望突破百亿美元销售门槛。
与静脉输注纳武利尤单抗相比,皮下注射纳武利尤单抗在28天内平均血清浓度(Cavgd28)和稳态血清低谷浓度(Cminss)指标上均表现出非劣效性,达到共同主要终点。关键次要终点客观缓解率(ORR)也显示出非劣效性。CheckMate-67T是一项随机、开放标签的III期临床研究(N=495),旨在评估皮下注射和静脉输注纳武利尤单抗在既往接受过全身治疗的ccRCC患者中的疗效。结果显示,与静脉输注(N=247)相比,皮下注射纳武利尤单抗的Cavgd28和Cminss均显示出非劣效性,几何平均比值分别为2.098(90% Cl: 2.001-2.200)、1.774 (90% CI: 1.633-1.927)。在BICR评估的关键次要终点方面,皮下注射纳武利尤单抗组患者ORR为24.2%,而静脉输注组患者的ORR为18.2%(RR=1.33;95% CI: 0.94-1.87),显示出非劣效性;皮下注射纳武利尤单抗组患者PFS为7.23个月,而后者该数值为5.65个月。安全性方面,皮下注射纳武利尤单抗与静脉输注一致。皮下注射纳武利尤单抗局部注射部位反应发生率为8.1%,且均为低等级和短暂的。
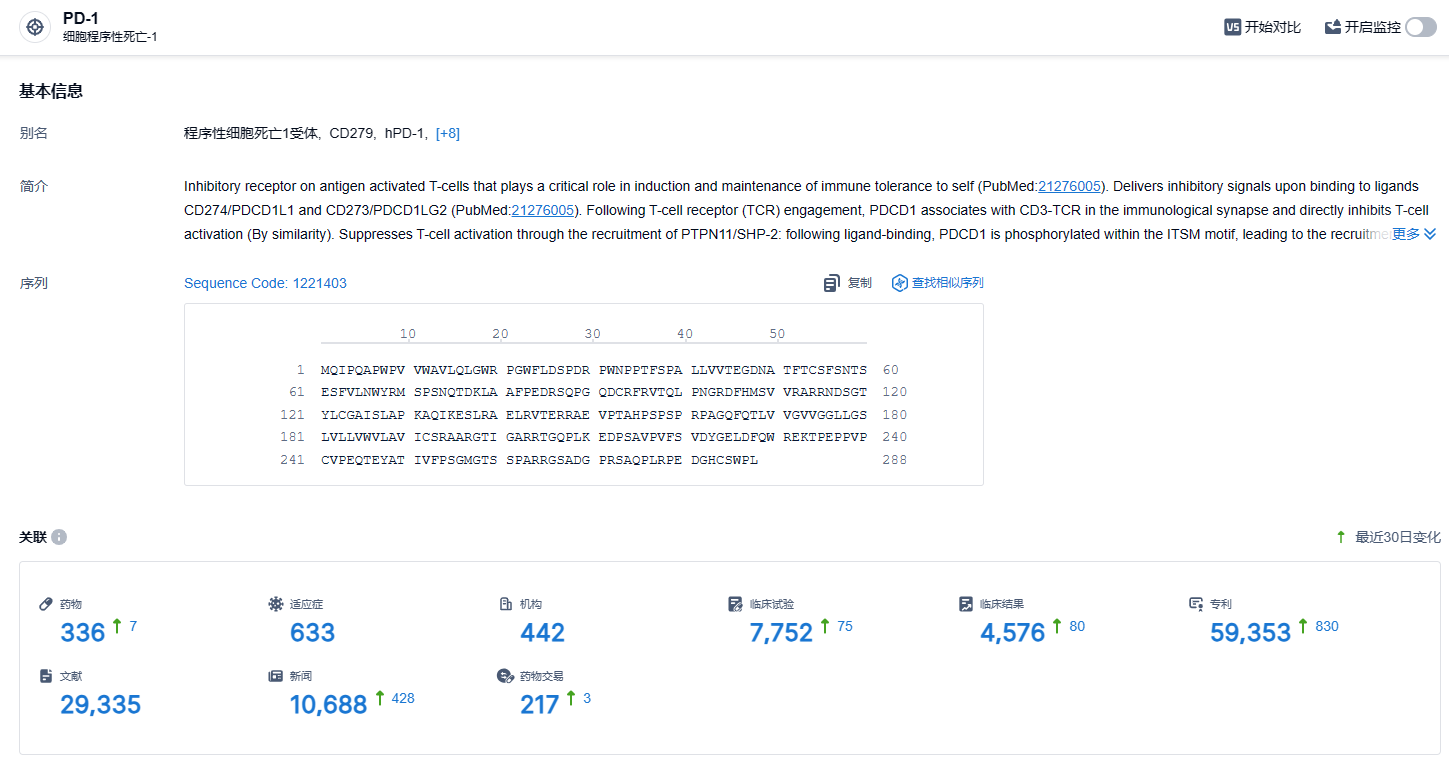
根据智慧芽新药情报库所披露的信息(点击下方卡片直达PD-1靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到2024年1月30日,PD-1靶点共有在研药物336个,包含的适应症有633种,在研机构442家,涉及相关的临床试验7752件,专利多达59353件……PD-1靶点是研发非常火热的领域,国内外均有众多企业布局,O药作为该领域的明星产品,期待该药的后续表现。