华东医药FRα ADC索米妥昔单抗注射液上市申请获受理
2023年10月25日,华东医药发布新闻稿称,其全资子公司中美华东收到中国国家药品监督管理局(NMPA)签发的《受理通知书》,由中美华东与ImmunoGen公司合作开发的索米妥昔单抗注射液(mirvetuximab soravtansine Injection,研发代码:IMGN853、HDM2002)的上市许可申请获得受理,申报适应症为:既往接受过1-3线系统性治疗的叶酸受体α(FRα)阳性的铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者。
索米妥昔单抗(HDM2002/ MIRV/ELAHERE®)是华东医药与 ImmunoGen 合作开发的全球首个针对叶酸受体 α 阳性卵巢癌 ADC 药物,该产品已于 2022 年 11 月获得美国 FDA 加速批准上市,用于治疗叶酸受体 α(FRα)阳性且既往接受过 1-3 线全身治疗方案的铂耐药卵巢上皮性癌、输卵管癌或原发腹膜癌的成年患者。2020年10月,华东医药与ImmunoGen达成协议,以4000万美元首付款和最高2.65亿美元里程碑付款以及约定比例的销售额提成费获得索米妥昔单抗在中国的开发和商业化权益,而ImmunoGen则保留该产品中国以外地区的所有权益。
该研究招募了106例铂类耐药性高级别浆液性上皮性卵巢癌、原发性腹膜癌或输卵管癌患者。结果显示,经研究者评估的客观缓解率(ORR)为32.4%,经BICR评估的ORR为31.6%。根据ImmunoGen财报,索米妥昔单抗正在逐步放量,2023Q1销售额达2950万美元。ImmunoGen还开展了另一项验证性III期MIRASOL研究,旨在将索米妥昔单抗在美国的加速批准转化为完全批准。2023年5月,MIRASOL研究传来捷报,相比化疗,索米妥昔单抗使患者的总生存期(OS)从12.75个月延长到16.46个月,死亡风险降低33%,成为首个延长FRα阳性铂耐药卵巢癌患者OS的新药;无进展生存期(PFS)从3.98个月延长到5.62个月。
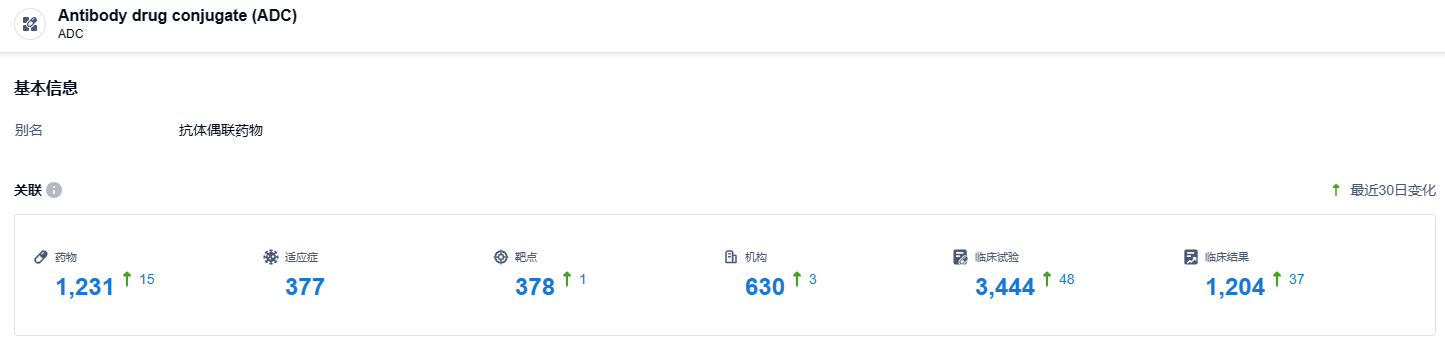
根据智慧芽新药情报库所披露的信息 (点击下方图片直达ADC药物类型注册登录后可免费获得该药物类型下的在研药物、适应症、靶点、研发机构、临床试验等详细信息),截止到 2023 年10月26日,ADC这一药物类型共有在研药物1231个,包含的适应症有377种,靶点378个,在研机构630家,涉及相关的临床试验3444件……期待索米妥昔单抗早日在国内上市,给国内患者带来新的治疗选择。