第2项!葆元医药/信达生物新一代ROS1抑制剂泰莱替尼拟纳入优先审评,针对NSCLC
2024年2月26日,中国国家药监局药品审评中心(CDE)官网公示,葆元医药申报的他雷替尼胶囊拟纳入优先审评,用于未经ROS1-TKI治疗的ROS1阳性局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的治疗。
泰莱替尼(他雷替尼,taletrectinib)最早由第一三共开发,是下一代靶向ROS1和NTRK的酪氨酸激酶抑制剂,其开发、生产和商业化权益于2018年12月被授予葆元医药。2021年6月,信达生物与葆元生物达成协议,以在大中华区合作开发和商业化泰莱替尼。葆元医药负责泰莱替尼在中国大陆地区的临床开发和注册报批以及大中华地区的临床生产和商业化生产,信达生物则有权负责泰莱替尼在中国香港、澳门和台湾地区的开发和注册报批。2023年11月22日,CDE网站显示,信达生物和葆元医药合作开发的新一代ROS1/NTRK抑制剂泰莱替尼(他雷替尼)申报上市。根据信达生物2023年H1财报,此次申报的适应症为治疗既往接受过ROS1-TKI治疗的ROS1融合阳性非小细胞肺癌(NSCLC)患者。
2023年10月,葆元医药公布了泰莱替尼治疗ROS1阳性NSCLC患者的II期TRUST-II研究的积极结果。该研究是一项全球关键性、多中心、单臂、开放标签的临床试验(n=154),其中队列1和队列2共包括53例初治ROS1阳性NSCLC患者和46例克唑替尼或恩曲替尼经治ROS1阳性NSCLC患者。结果显示,在初治患者(n=25)中,经确认的客观缓解率(cORR,标准为肿瘤体积缩小)达到了92%;在既往接受过1种ROS1-TKI抑制剂治疗的患者(n=21)中,cORR为57%。此外,泰莱替尼对存在脑转移的患者(n=8)也有效,cORR为62.5%。初治患者的无进展生存期(PFS)尚未达到,经治患者的PFS约为11.7个月。
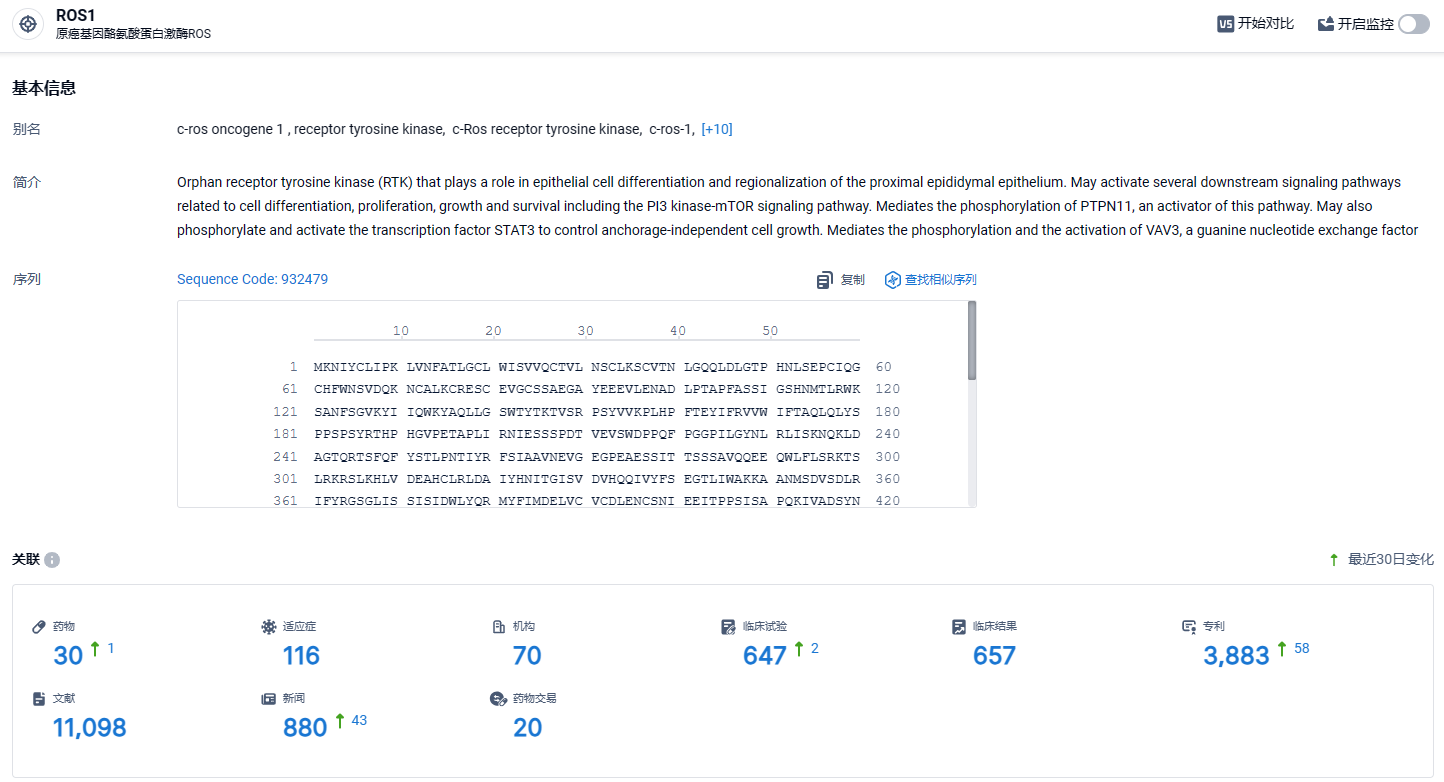
根据智慧芽新药情报库所披露的信息 (点击下方图片直达ROS1靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年2月27日,ROS1靶点共有在研药物30个,包含的适应症有116种,在研机构70家,涉及相关的临床试验647件,专利多达3883件……目前,全球已有7款针对ROS1的靶向药物获批上市,其中仅有两款可同时抑制ROS1和TRK,分别为恩曲替尼和瑞普替尼。期待泰莱替尼得后续表现。