正大天晴GLP-1受体激动剂利拉鲁肽生物类似药获批上市,针对2型糖尿病
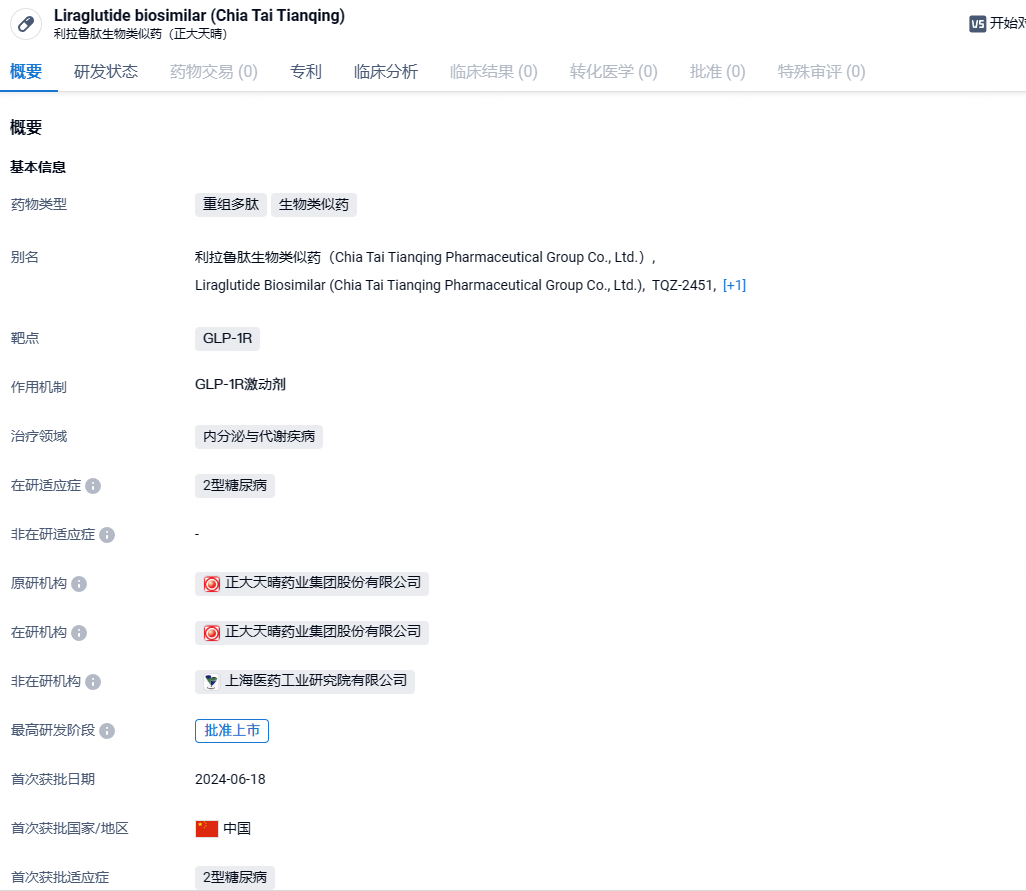
2024年6月25日,中国国家药监局(NMPA)官网最新公示,正大天晴申报的利拉鲁肽注射液生物类似药的上市申请已获得批准。公开资料显示,利拉鲁肽是一款人GLP-1R激动剂。
利拉鲁肽原研药由诺和诺德开发,分别于2009年、2010年在欧盟和美国获准上市,并在 2011年在中国上市,获国家药品监督管理局批准,用于治疗成人 2 型糖尿病。在海外,诺和诺德还有利拉鲁肽的减重适应症于2014年12月获得美国食品药品监督管理局(FDA)批准。2023年3月,华东医药全资子公司中美华东开发的利拉鲁肽注射液获批上市,用于成人2型糖尿病患者控制血糖,成为首款在国内上市的利拉鲁肽注射液仿制药,今年7月,进一步获批肥胖或超重适应症。此次大天晴申报的利拉鲁肽注射液生物类似药(TQZ-2451)的上市申请已获得批准,属于国产第3款。
目前,利拉鲁肽已被纳入《美国糖尿病学会(ADA)糖尿病诊疗标准(2024版)》、《中国2型糖尿病防治指南(2020年版)》、《中国成人2型糖尿病合并心肾疾病患者降糖药物临床应用专家共识》等多个指南。
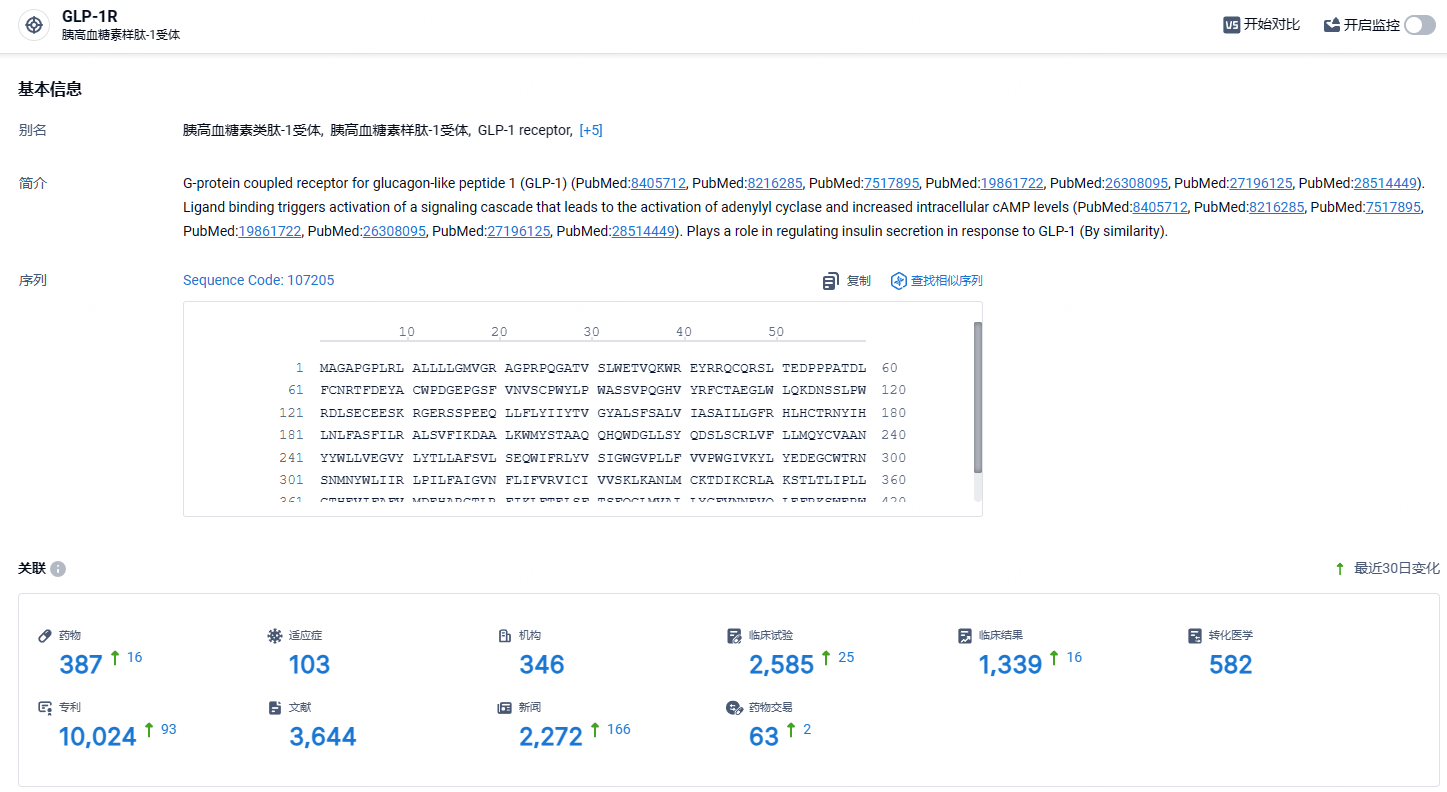
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 GLP-1R靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年6月26日,GLP-1R靶点共有在研药物387个,包含的适应症有103种,在研机构346家,涉及相关的临床试验2585件,专利多达10024件……GLP-1是当前全球最热门的降糖和减重靶点,在这一领域,除利拉鲁肽外,正大天晴司美格鲁肽注射液正在进行III期临床试验,有望为患者带来更多治疗选择。目前,国内已有三款利拉鲁肽生物类似药获批上市,分别来自华东医药、通化东宝和正大天晴。此外,联邦制药、健元医药、翰宇药业和圣诺生物的利拉鲁肽生物类似药已申报上市,东阳光药、万邦医药、双鹭药业、宸安生物/派金生物的利拉鲁肽生物类似药正在开展III期临床试验。