维亚臻生物siRNA新药VSA003注射液拟纳入突破性治疗品种,针对高胆固醇血症
2024年1月18日,中国国家药监局药品审评中心(CDE)官网公示,维亚臻生物申报的VSA003注射液拟纳入突破性治疗品种,针对适应症为成人纯合子型家族性高胆固醇血症(HoFH),可用于在饮食疗法和其他降脂治疗基础上且需要进一步降低LDL-C的HoFH患者,或其他降脂治疗无效、或不耐受其他降脂治疗的HoFH患者。
VSA003是一款治疗脂质代谢紊乱的肝脏靶向小干扰RNA(siRNA)药物,通过靶向降解血管生成素样蛋白3(ANGPTL3)信使RNA(mRNA),增加对低密度脂蛋白胆固醇(LDL-C)和甘油三酯(TG)等的清除。因此具有针对高胆固醇血症、高甘油三酯血症、纯合子型家族性高胆固醇血症(HoFH)等心血管领域未满足医疗需求的治疗潜力。
2023年7月,维亚臻生物宣布,其在研1类新药VSA003注射液(以下简称VSA003)在中国医学科学院北京协和医院顺利完成首例受试者给药。
HoFH是由低密度脂蛋白胆固醇(LDL-C)分解代谢的关键基因发生突变所引起的常染色体显性遗传性疾病,因极为罕见已被纳入国家《第一批罕见病目录》。由于HoFH患者出生时就处于极高的LDL-C水平暴露状态,患者发生动脉粥样硬化性心血管疾病的风险明显增高,全身动脉粥样硬化病变发生早且进展快,可在儿童及青年期发生心绞痛或心肌梗死,并于20至30岁之前死亡。靶向ANGPTL3的小核酸药物,有望通过非LDLR依赖的降脂机制,成为HoFH患者的更佳药物治疗选择。
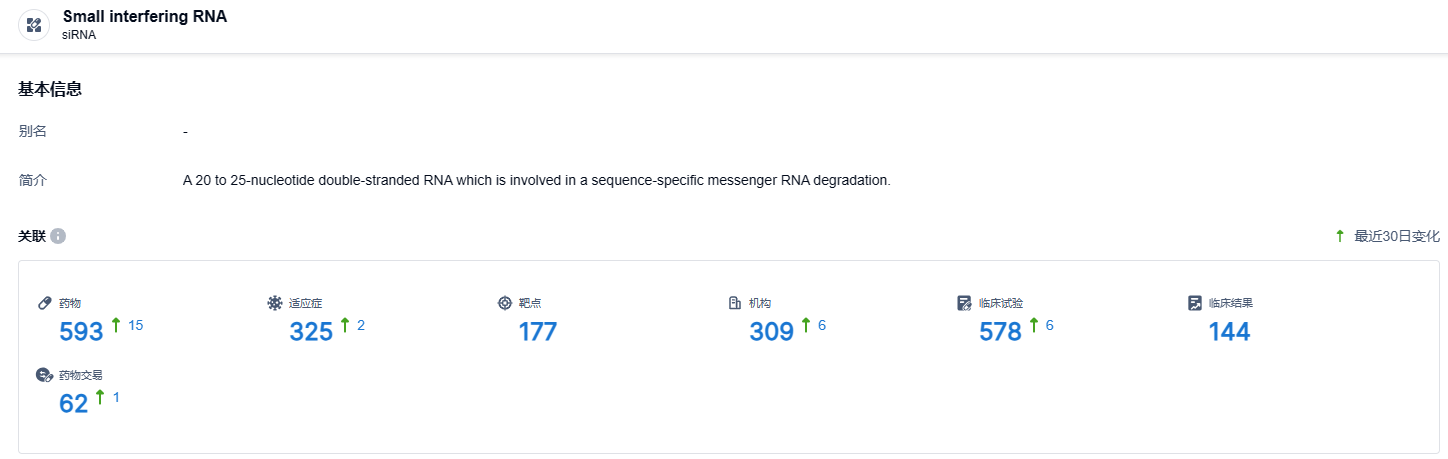
根据智慧芽新药情报库所披露的信息 (点击下方图片直达siRNA药物类型注册登录后可免费获得该药物类型下的在研药物、适应症、靶点、研发机构、临床试验等详细信息),截止到 2024 年1月19日,siRNA这一药物类型共有在研药物593个,包含的适应症有325种,靶点177个,在研机构309家,涉及相关的临床试验578件……目前维亚臻生物产品管线拥有三款处于临床研发阶段、针对心血管及代谢领域的siRNA药物。本次也是维亚臻生物第二款产品被拟纳入突破性治疗品种。此前,该公司靶向APOC3的siRNA药物VSA001注射液已经被纳入突破性治疗品种,拟开发用于降低家族性乳糜微粒血症综合征(FCS)成人患者的甘油三酯水平。期待维亚臻生物在siRNA领域大展身手。





