STING药物靶点研发进展
cGAS-STING信号通路是一种胞质DNA传感通路,在先天免疫反应中扮演关键角色。了解该信号通路对于研究药物靶点和治疗策略至关重要。当肿瘤DNA被胞质中的cGAS感知时,cGAS催化连接核苷酸形成CDNs,进而与STING结合并激活它。这一过程触发了一系列的免疫反应,包括激活干扰素通路和调动其他重要信号通路。激活的STING会向细胞内不同位置转运,招募其他关键分子,如TBK1和IRF3,进一步激活干扰素通路和其他重要的免疫反应通路。这些反应有助于机体抵御病毒和肿瘤等病原体的侵袭。除了肿瘤DNA,STING还能感知细菌产生的环二核苷类天然配体,进而激活下游信号通路。这揭示了cGAS-STING通路在机体免疫监视中的重要作用。
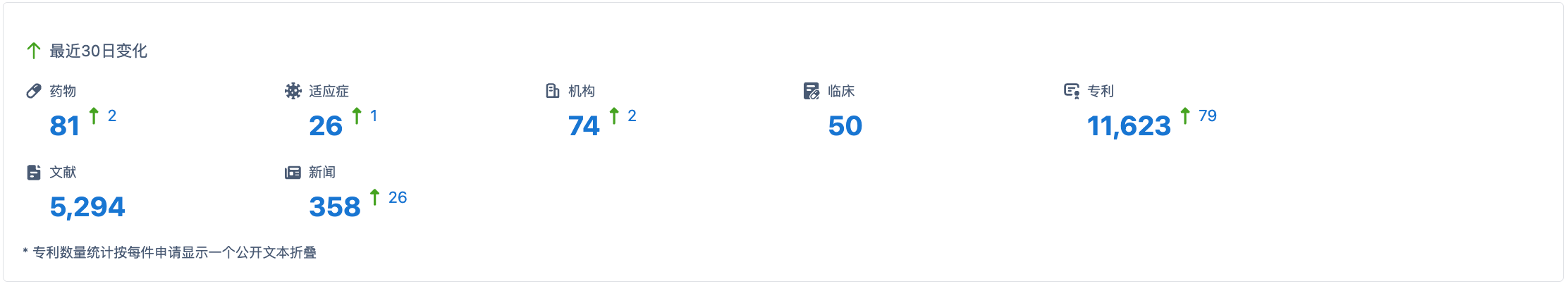
截至目前,已有81种以STING为靶点的药物被发现,并涵盖了26个不同的适应症。研发这些药物的机构达到74家,与临床试验相关的数据显示,已有50项临床试验结果与STING靶点药物相关。同时,STING靶点药物的研发也受到了广泛的关注和保护,目前已有11647项专利申请与STING靶点药物相关。为了支撑STING靶点药物研究的进展,已有5294篇文献发表。这反映了该领域的科学活跃度和知识积累。
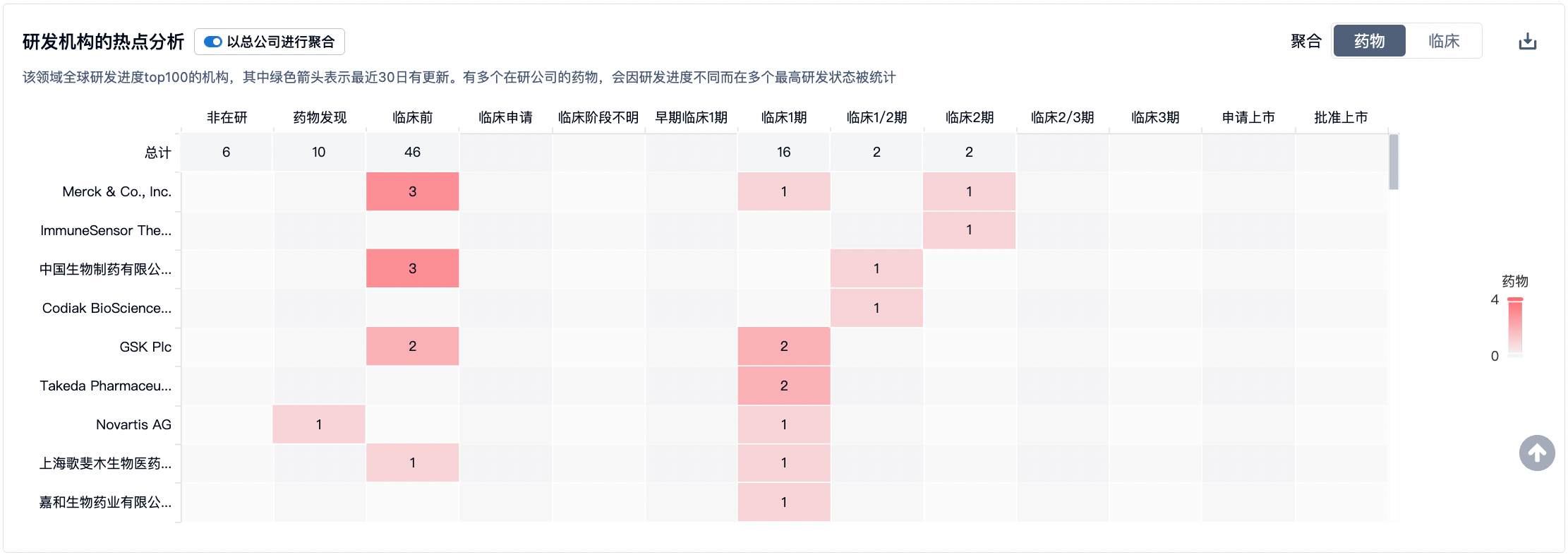
竞争格局
默克的MK-1454和ImmuneSensor的IMSA-101在STING靶点药物研发领域处于领先位置,已达临床2期。中国生物制药、GSK和CS-Bay等机构也展现出强烈的竞争热度,它们分别开发了4种与STING靶点相关的药物。
重点药物
第一代STING激动剂是CDNs的衍生物,由于在体内被迅速清除、膜通透性较差,并且只能通过瘤内给药方式使用,因此其作用范围受到限制。为了解决这些问题,新一代STING激动剂的研发方向是实现系统给药,提高药物在肿瘤中的分布浓度,从而提高药物治疗窗口。
F-star Therapeutics的SB11285是新一代STING激动剂,它能够特异性地靶向难以触及的肿瘤细胞,并促使激活的免疫细胞从外周迁移到肿瘤病灶。在与PD-L1抗体阿替利珠单抗(商品名:Tecentriq)联用或单药治疗晚期实体瘤的I期临床试验中,SB11285表现出良好的耐受性和疗效。
默沙东的MSA-2是一种稳定型STING激动剂,以非共价二聚体形式结合STING,并诱导其处于封闭构象。疗效研究显示,在结直肠癌小鼠模型中,通过瘤内、皮下或口服给药,MSA-2表现出良好的耐受性,可使80%至100%接受治疗的小鼠肿瘤完全消退。此外,MSA-2只有在形成二聚体的情况下才能与STING结合,而肿瘤微环境的酸性条件更有利于MSA-2的二聚化。因此,尽管MSA-2是全身性给药,但具有潜在的肿瘤特异性,表现出较好的安全性和耐受性。
武田的TAK-676是一种新型合成STING激动剂,与肿瘤内注射的STING激动剂相比,TAK-676经过最佳设计以降低血清降解并增强渗透性,可通过全身性静脉给药途径使用。此外,在放疗后加入TAK-676可通过增加STING介导的IFN抑制剂释放来增强免疫应答,并进一步刺激T细胞介导的抗肿瘤免疫反应。目前正在进行的研究旨在评估放疗后TAK-676联合帕博利珠单抗的安全性和初步抗肿瘤活性。
卫材的E7766是一种大环桥联STING激动剂。在肝脏肿瘤小鼠模型中,单次注射E7766能够使90%的肿瘤消退,并且在8个月以上没有复发。目前,E7766正在进行I/Ib期临床试验,旨在评估E7766作为单一疗法对晚期实体瘤和淋巴瘤患者的疗效。
Scripps研究所的SR-717是一种可口服或系统性给药的非核苷酸小分子STING激动剂。在侵袭性黑色素瘤动物模型中,SR-717显著抑制了肿瘤的生长和转移,并促使肿瘤分子呈现给免疫系统,从而大幅度提高了肿瘤周围CD8+ T细胞和自然杀伤(NK)细胞的水平。
GSK的GSK37417是一种含有二聚氨基苯并咪唑支架的非CDN小分子STING激动剂。目前正在进行I期剂量递增研究,研究中将GSK37417作为单一疗法或与多司他利单抗(商品名:Jemperli)联用治疗复发/难治性实体瘤患者。GSK37417通过静脉注射给药,预计研究将于2025年完成。
Synlogic公司的SYNB1891是一种表达dacA蛋白的大肠杆菌,它能催化2个ATP分子生成环状的AMP二聚体,从而激活STING蛋白,进而产生1型干扰素反应,并促进肿瘤特异性T细胞的反应。罗氏与Synlogic公司合作探索其PD-L1抑制剂阿替利珠单抗与SYNB1891联用治疗晚期实体瘤患者的效果。