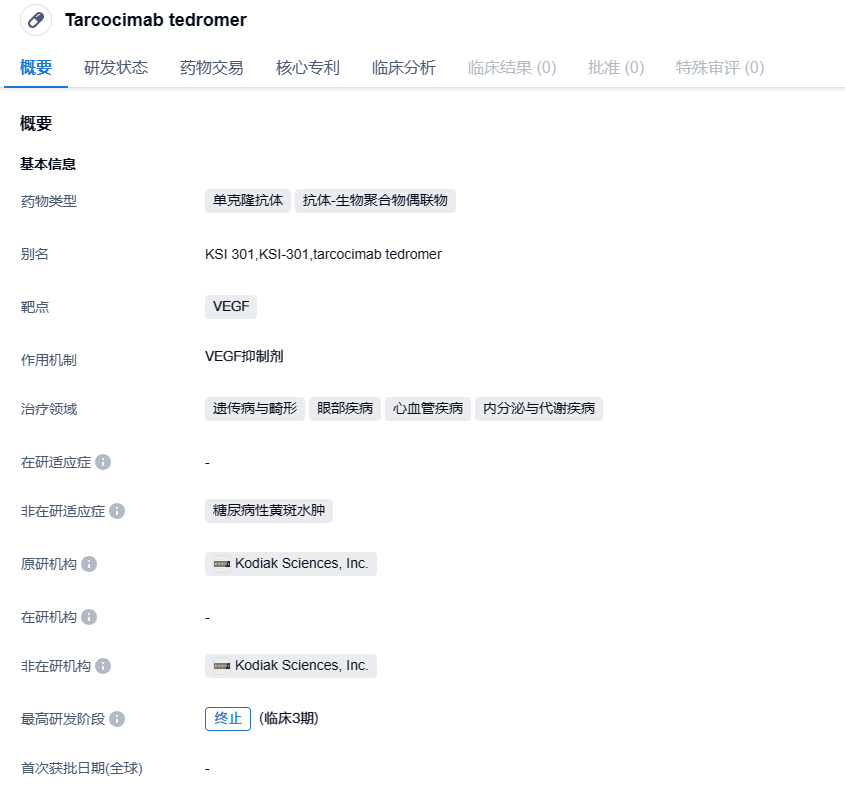
Kodiak创新疗法tarcocimab tedromer 3期试验达主要终点,治疗糖尿病视网膜病变
近日,Kodiak Sciences宣布,评估5 mg剂量的抗体偶联生物聚合物(ABC)疗法tarcocimab tedromer治疗中重度非增殖性糖尿病视网膜病变(NPDR)患者的3期GLOW优效研究达到了其一年期的主要终点。经过每6个月一次的治疗后,NPDR患者的视力和视网膜解剖结构得到了改善并保持稳定。
tarcocimab tedromer(KSI-301)是Kodiak基于其专有的ABC平台研发的长效抗血管内皮生长因子(VEGF)疗法,将VEGF抗体偶联到高度疏水的磷脂胆碱多聚物上,可特异性结合VEGF下调VEGF水平,并且能够极大程度上延长VEGF抗体在玻璃体内的半衰期,从而实现更长时间的有效性,减少给药频率。体外试验结果已表明,KSI-301与雷珠单抗和阿柏西普相比“最大抑制”(Maximal Inhibition)提高,其抑制HRMVEC细胞增生的作用优于单抗类药物。
分析显示,GLOW研究达到主要终点,即糖尿病视网膜病变严重程度量表(DRSS)评分至少改善2级的患者比例。使用tarcocimab治疗的患者中,41.1%的可评估患者的病情至少改善了2级,而假性治疗对照组中只有1.4%的可评估患者的病情显示出改善(P<0.0001),应答率比提高了29倍。在延长给药间隔时间后,使用tarcocimab治疗患者的视力和视网膜解剖结构得到了改善并保持稳定。GLOW研究同样达到了所有关键的次要终点,包括发生危及视力的并发症(如糖尿病性黄斑水肿和增殖性糖尿病视网膜病变)患者比例较对照组有了更大的降低,风险降低了89%,达到21.0%对比2.3%(P<0.0001)。与对照组相比,发生糖尿病性黄斑水肿的风险降低了95%,其中对照组为13.7%,而tarcocimab组为0.7%。与对照组相比,tarcocimab在防止糖尿病性黄斑水肿(DME)发生上也表现出95%的风险减少,其中,对照组的发病率为13.7%,而tarcocimab组为0.7%。两组受试者发生严重眼部不良事件和眼内炎症的比例相似。
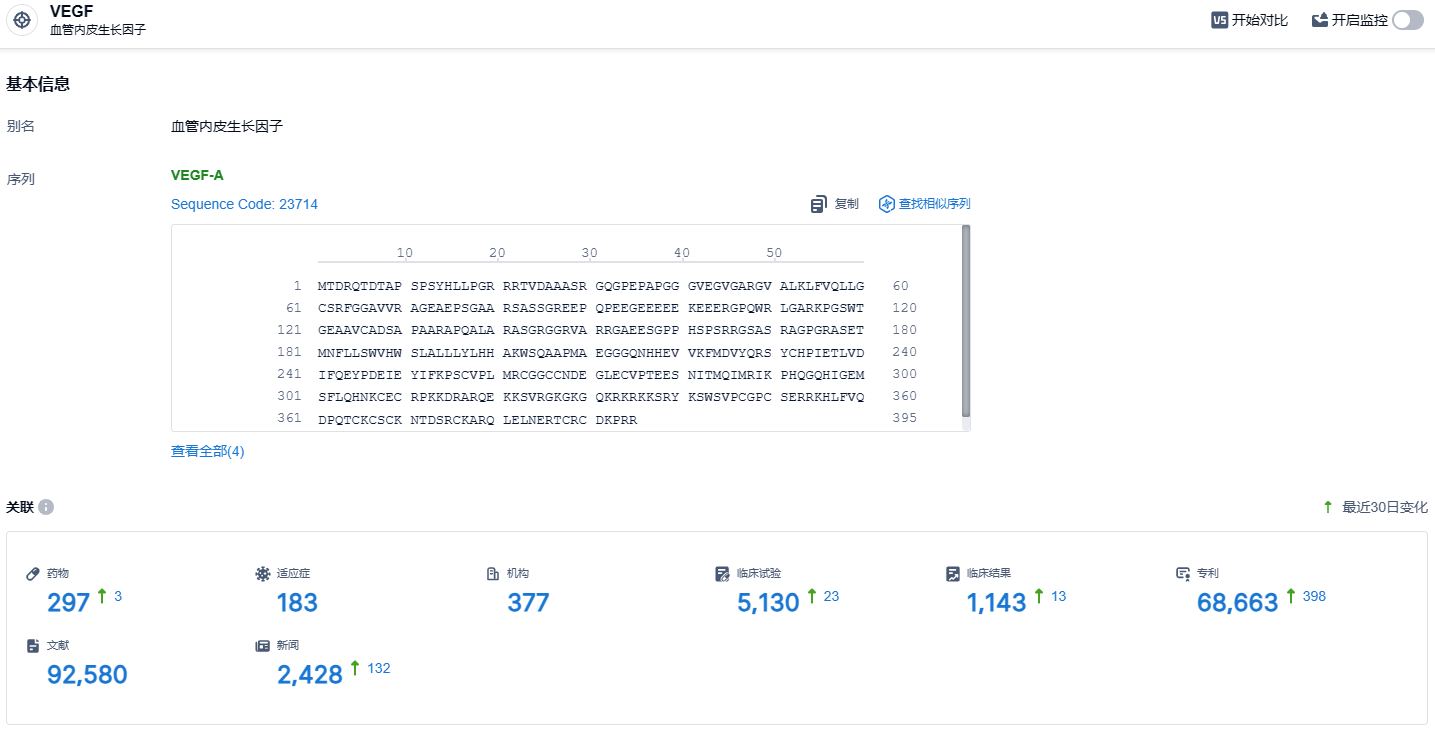
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达VEGF靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年11月9日,VEGF靶点共有在研药物297个,包含的适应症有183种,在研机构377家,涉及相关的临床试验5130件,专利多达68663件……2023年7月24日,Kodiak Sciences公布tarcocimab tedromer治疗AMD、DME三项三期临床的最新数据,三项三期临床均未达到主要终点,引发股价大跌。此次治疗中重度非增殖性糖尿病视网膜病变(NPDR)患者的3期GLOW优效研究达到了其一年期的主要终点,能够让其逆风翻盘,拭目以待。