强生潜在重磅FcRn单抗尼卡利单抗Ⅱ/Ⅲ期研究取得积极结果,针对重症肌无力
10月15日, 强生宣布尼卡利单抗(Nipocalimab)在治疗患有全身性重症肌无力 (gMG) 的抗AChRa阳性青少年(12-17岁)患者的2/3期研究中取得积极结果。接受尼卡利单抗加标准治疗 (SOC) 治疗的患者实现了持续的疾病控制。
Nipocalimab是一款潜在“best-in-class”、靶向新生儿Fc受体的抗体疗法。它通过与FcRn结合,让被单核细胞和内皮细胞摄入的自身抗体不会被重新释放到血液中,而是在细胞内被降解。已有研究显示,它可以将血液循环中包括致病自身抗体在内的IgG水平降低超过75%。这款抗体疗法有望治疗多种自身抗体介导的免疫疾病。FDA曾授予该疗法突破性疗法认定,用于治疗有高风险出现严重新生儿溶血病(HDFN)的孕妇,以及授予其快速通道资格用以治疗HDFN、gMG、温抗体型自身免疫性溶血性贫血(wAIHA)、胎儿新生儿同种免疫性血小板减少症(FNAIT)。。2020 年8 月,强生以65 亿美元收购生物技术公司Momenta,获得3期药物nipocalimab,加强自身免疫病管线的布局。这项2/3期研究结果为首次公布,与尼卡利单抗治疗gMG成人患者的关键研究结果一致。今年8月和9月,强生已分别向FDA、EMA提交尼卡利单抗的上市申请,用于治疗成人gMG患者。
此前上市申请是基于三期临床Vivacity-MG3的数据。在三期临床Vivacity-MG3中,经过24周治疗,Nipocalimab+标准治疗、安慰剂+标准治疗组,重症肌无力日常生活量表(MG-ADL)分别下降4.70、3.25,差值Wie2.45,p值为0.002。重症肌无力量表(QMG)分别下降4.86、2.05,差值为2.81,p值小于0.001。该研究还达到了多个关键的次要终点:在第22周和第24周,通过QMG测量不同肌肉群的力量和功能的改善情况,Nipocalimab+SOC组与安慰剂+SOC组相比,显著改善(P<0.001);在第22、23和24周,与安慰剂+SOC相比,Nipocalimab+SOC的MG-ADL反应(比基线改善≥2点)显著更高(P=0.021),进一步强调了Nipocalimab减轻gMG对患者日常生活影响的潜力。
此次的Ⅱ/Ⅲ期Vibrance-MG研究旨在评估尼卡利单抗对儿科gMG患者的疗效。研究的主要终点是24周内IgG从基线水平的减少情况,次要终点包括MG-ADLb和QMGc评分的改善。结果显示,尼卡利单抗联合SOC治疗达到了研究的主要终点,总血清IgG减少了69%,并同时达到了两个次要终点,即MG-ADL和QMG评分的改善。此外,五名患者中有四名在治疗结束时症状表现达到最低水平(MG-ADL评分0-1)。尼卡利单抗在六个月期间耐受性良好,与成人患者的研究结果相似,未发生严重不良事件,也没有因不良事件而停药。
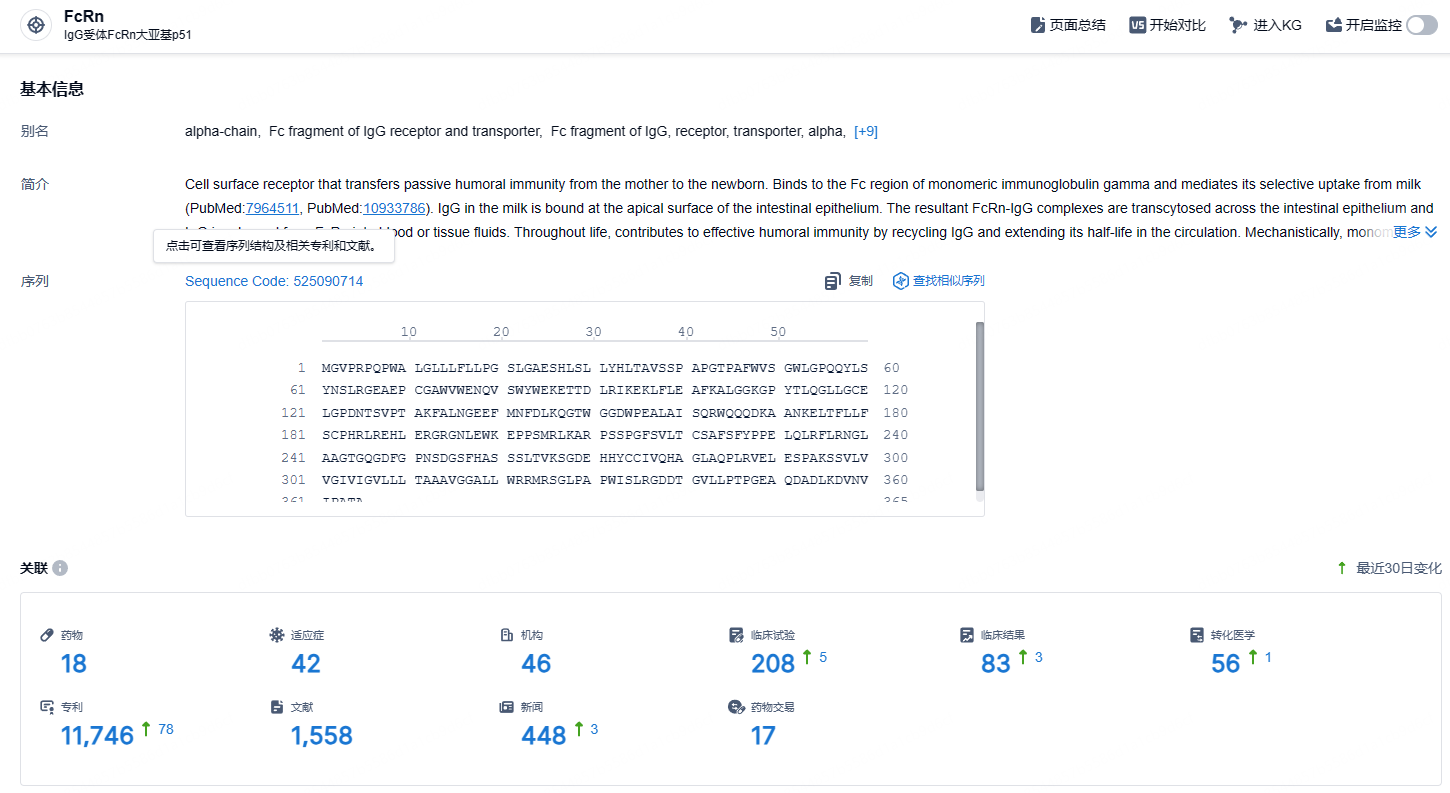
根据智慧芽新药情报库所披露的信息 (点击下方图片直达FcRn靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年10月17日,FcRn靶点共有在研药物18个,包含的适应症有42种,在研机构46家,涉及相关的临床试验208件,专利多达11746件……研究表明,FcRn 广泛表达于各个组织的细胞中,其中包括与血管壁对齐的内皮细胞,肠上皮细胞、气道上皮细胞、胎盘合胞体滋养细胞、肝细胞、内皮细胞、髓样细胞以及支气管导管细胞等;此外,在造血细胞如B 细胞、巨噬细胞以及树突状细胞中也収现了高水平表达的FcRn,理论上可导致七八十种自身免疫性疾病。期待强生这款FcRn单抗早日上市。