信达生物降脂新药PCSK9抑制剂托莱西单抗获批上市,国产首个!
2023年8月16日,信达生物自主研发的PCSK9抑制剂托莱西单抗注射液(研发代号:IBI306)获得国家药品监督管理局(NMPA)批准上市,治疗原发性高胆固醇血症(包括杂合子型家族性和非家族性高胆固醇血症)和混合型血脂异常。作为中国首个获批的本土自主研发PCSK9抑制剂,信必乐®(托莱西单抗注射液)是信达生物布局心血管疾病领域的首款产品,也是信达生物成立12年来的第十款产品。
信必乐@ (托莱西单抗注射液) 是信达生物制药自主研发的创新生物药,lgG2全人源单克隆抗体,能特异性结合PCSK9 (前蛋白转化酶枯草杆菌蛋白酶/ kexin 9 型)分子,通过减少PCSK-9介导的低密度脂蛋白受体(LDLR)内吞来增加LDLR水平,进而促进LDL-C在肝脏内的降解,降低血浆中LDL-C,治疗高脂血症,降低心血管疾病风险。之前,国内已有两款PCSK-9抑制剂获批上市,分别是赛诺菲的阿利西尤单抗和安进的依洛尤单抗,随着托莱西单抗注射液的上市,该领域竞争也变得越发激烈。
此次批准是基于托莱西单抗三项III期临床试验(CREDIT-1、CREDIT-2和CREDIT-4)的研究结果:与安慰剂相比,托莱西单抗可降低LDL-C水平约57%~65%,且可维持长期治疗疗效;此外,托莱西单抗还可明显降低总胆固醇、非高密度脂蛋白胆固醇、载脂蛋白B及脂蛋白a水平。托莱西单抗的降脂达标率高,可长间隔给药(每6周一次),整体安全性良好,有望成为原发性高胆固醇血症和混合型血脂患者的强效治疗手段。托莱西单抗的疗效和安全性也得到了学术界的认可。CREDIT-1研究的主要结果以大会壁报的形式发表于2022年美国心脏协会年会 (AHA),研究论文近期将会在同行评议的学术期刊发表。CREDIT-2研究的主要结果以大会壁报的形式发表于2022年美国心脏病学会年会 (ACC) ,研究论文发表于BMC Medicine。CREDIT-4研究论文已于2023年7月在线发表于JACC: Asia。
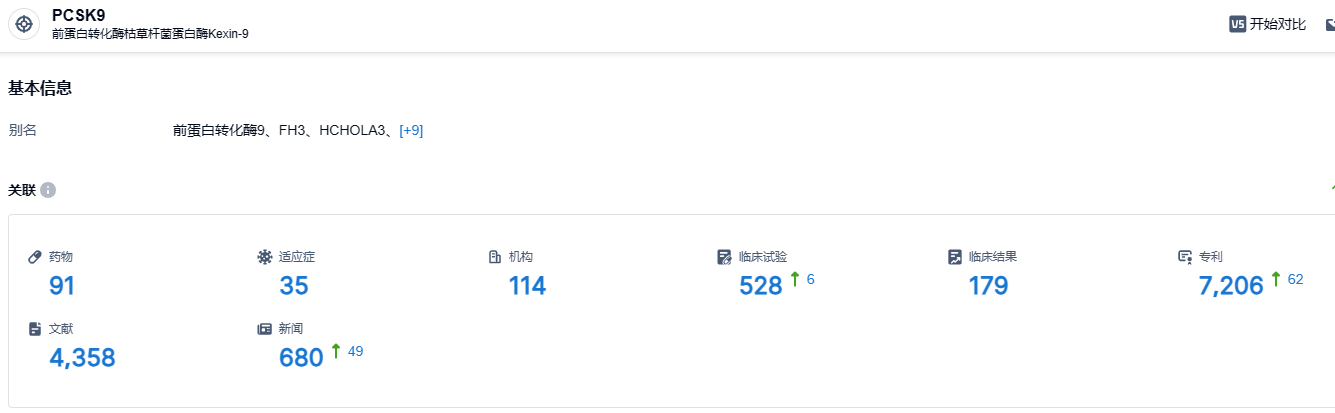
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 PCSK9 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年7月17日,PCSK9靶点共有在研药物91个,包含的适应症有35种,在研机构114家,涉及相关的临床试验528件,专利多达7206件……PCSK9靶点在降血脂领域有着非常大的治疗潜力,恒瑞、君实和康方生物等企业开发的PCSK9抑制剂已进入申报上市阶段,红海市场初现。