恒瑞医药CDK4/6抑制剂达尔西利新适应症获批临床,治疗前列腺癌
2023年9月10日,恒瑞医药公告,恒瑞医药及子公司成都盛迪医药收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,同意开展羟乙磺酸达尔西利片联合醋酸阿比特龙片(I)和泼尼松片(AA-P)对比安慰剂联合AA-P治疗高瘤负荷的转移性激素敏感性前列腺癌(mHSPC)的多中心、随机、双盲的Ⅰb/Ⅲ期临床研究。
达尔西利是首个国产原研CDK4/6抑制剂,由恒瑞医药开发。它能够选择性地抑制CDK4/6激酶活性,进而阻断CDK4/6-Rb信号通路,诱导细胞G1期的阻滞并选择性地抑制Rb高表达肿瘤细胞的增殖,从而达到抗肿瘤的作用。此外,该产品通过经典电子等排体替换引入哌啶结构,从而避免了潜在的肝脏毒性。2022年1月,达尔西利首次在中国获批上市,联合氟维司群用于治疗HR阳性、HER2阴性、经内分泌治疗后进展的复发或转移性乳腺癌。2023年6月26日,恒瑞医药的CDK4/6抑制剂达尔西利的新适应症获批,适应症为:联合芳香化酶抑制剂作为初始治疗,适用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性局部晚期或转移性乳腺癌患者。
前列腺癌是全球男性发病率排第2、死亡率排第5的恶性肿瘤。根据GLOBOCAN2020报告,2020年全球约有141万例新发前列腺癌病例(占男性所有新发恶性肿瘤病例的14.1%,仅次于肺癌的14.3%)以及约38万例死亡病例(占男性所有恶性肿瘤死亡病例的6.8%)。根据国家癌症中心2022年2月数据,2016年我国新发前列腺癌病例约为7.8万例(居男性恶性肿瘤发病率第6位),死亡病例约3.4万例(居男性恶性肿瘤死亡率第8位);同时我国初诊前列腺癌患者中的转移性患者比例远高于西方国家,既往流行病学研究显示我国初诊患者中约50%已处于转移性疾病阶段,而在西方国家该比例不到10%。前列腺癌细胞的生长特征性地依赖于雄激素受体(AR)通路的激活,因此雄激素剥夺治疗(ADT,即去势治疗,包括双侧睾丸切除和促性腺激素释放激素类似物[GnRHa]药物治疗)联合或不联合新型内分泌治疗(NHT)拮抗剂(如阿比特龙,恩扎鲁胺)是目前转移性前列腺癌的标准一线治疗,随着新型内分泌治疗药物的普遍应用,临床医生对转移性激素敏感性前列腺癌(mHSPC)患者生存的预期逐步提高。高瘤负荷与mHSPC患者预后差密切相关,目前高瘤负荷mHSPC临床一线治疗方案存在局限性,因此,开发新型有效NHT的联合治疗方案已成为高瘤负荷mHSPC患者的迫切临床需要。羟乙磺酸达尔西利片联合醋酸阿比特龙片(I)和泼尼松片(AA-P)有望给前列腺癌患者带来新的治疗选择。
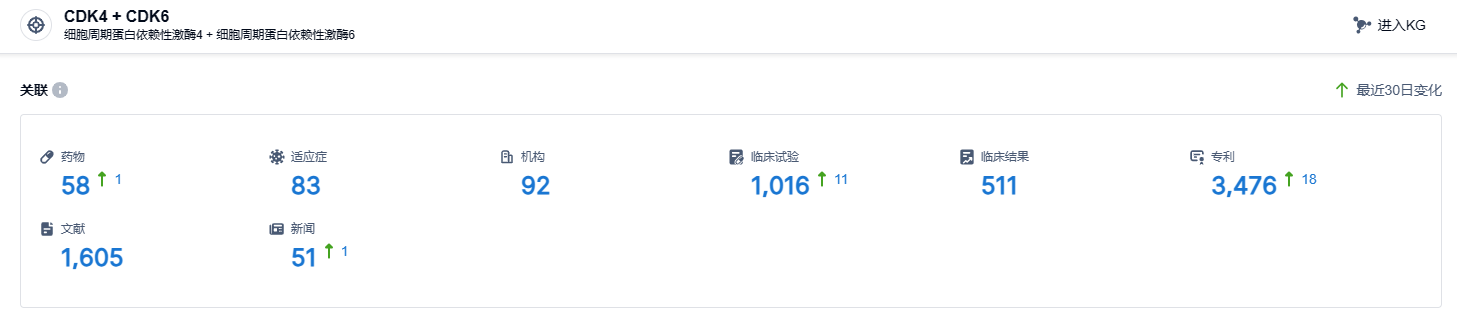
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 CDK4/6靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年9月12日,CDK4/6靶点共有在研药物58个,包含的适应症有83种,在研机构92家,涉及相关的临床试验1016件,专利多达3476件……恒瑞的达尔西利作为当前唯一获批上市的国产 CDK4/6 抑制剂,本身具备国产优势,各大适应症的研发进度在国产CDK4/6抑制剂中遥遥领先,期待该药的后续表现。