亘喜生物口头报告FasTCAR-T疗法GC012F最新临床数据,ORR达100%!
2023年12月12日,亘喜生物宣布在第65届美国血液学会(ASH)年会上以口头报告形式公布了一项GC012F治疗多发性骨髓瘤新确诊(NDMM)患者的由研究者发起的临床试验(IIT)最新研究结果。
GC012F是一款基于亘喜生物的FasTCAR技术平台开发的BCMA + CD19双靶点自体CAR-T细胞疗法,有望为癌症和自身免疫性疾病带来新的治疗选择,并具备差异化的安全性优势。目前,亘喜生物正在开展FasTCAR-T GC012F的多项临床研究,适应症覆盖多种血液肿瘤和自身免疫性疾病。临床数据显示,该药物在临床研究中展现出了良好的有效性和安全性。亘喜生物已在美国启动了一项评估 GC012F治疗复发/难治性多发性骨髓瘤(RRMM)的1b/2期IND临床试验,在中国也即将启动同适应症的1/2期IND临床试验。此外,美国FDA已经批准了GC012F针对难治性系统性红斑狼疮(rSLE)的IND申请,同时,一项针对同适应症的由研究者发起的临床试验也已启动。2023年11月27日,亘喜生物宣布其CD19/BCMA双靶点自体FasTCAR-T细胞疗法GC012F的又一项新药临床试验(IND)申请获得美国FDA批准,将在美国启动治疗难治性系统性红斑狼疮(rSLE)的1/2期临床试验。
截至2023年10月1日数据截止日,22例符合移植条件的高危NDMM患者在接受了GC012F治疗后,展现出100%的总体应答率(ORR)和95%的微小残留病灶阴性(MRD-)严格完全缓解(sCR)率。其中,16例为既往随访患者,2022年ASH年会期间已发表过首次临床数据;另外6例为新入组接受治疗的患者。在本针对前线治疗的临床试验中,数据显示GC012F耐受性良好,未观察到新的安全性信号。
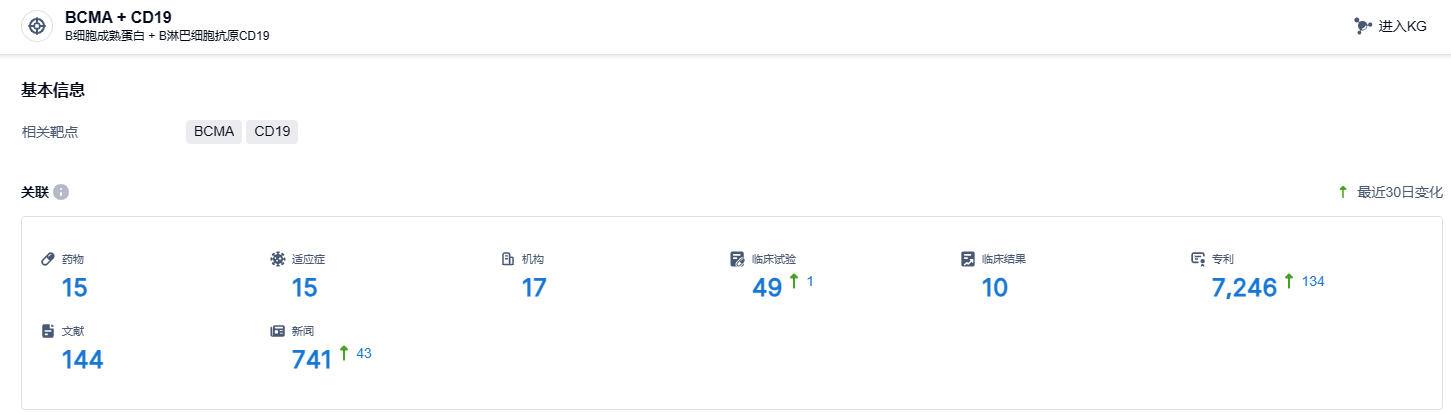
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达BCMA + CD19靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年12月13日,BCMA + CD19靶点共有在研药物15个,包含的适应症有15种,在研机构17家,涉及相关的临床试验49件,专利多达7246件……FasTCAR-T GC012F目前正处于一系列临床试验中,以探索其针对多发性骨髓瘤、B细胞非霍奇金淋巴瘤以及系统性红斑狼疮的治疗效果。目前这些疾病仍有大量的临床需求尚未被满足,期待GC012F能够给患者带来新的治疗选择。