首个!Ascidian体内RNA外显子编辑疗法ACDN-01挺进临床,针对Stargardt病
2024年1月30日,Ascidian Therapeutics宣布在研RNA外显子编辑疗法ACDN-01的IND申请已经获得美国FDA的许可,并被授予快速通道资格。
ACDN-01是一种由单个载体递送的体内 RNA 外显子编辑器,在非人灵长类动物视网膜中展示了高效、持久的体内 RNA 外显子编辑,在人类视网膜外植体中展示了离体 RNA 外显子编辑。Ascidian 的反式剪接前 mRNA 外显子编辑技术,包含目标外显子的合成 RNA 序列以及分子线索(包括供体和受体位点),目标是在前 mRNA 处理过程中将正确的 RNA 序列包含在新出现的 mRNA 转录物中剪接体;编辑成分首先被编码在重组 DNA 分子中,该分子可以通过 AAV 载体或脂质纳米颗粒递送至靶细胞。ACDN-01是首个获美国FDA许可进入临床试验的RNA外显子编辑疗法,并且是首款专门针对Stargardt病遗传起源的临床期治疗方法。Ascidian预计在2024年上半年开始招募参与ACDN-01针对Stargardt病及其他ABCA4相关视网膜病变的1/2期临床试验STELLAR的患者。
Stargardt病是一种原发于视网膜色素上皮层的常染色体隐性遗传病, ABCA4基因突变是引发Stargardt病的原因之一,该突变导致进行性视网膜变性和视力丧失,通常始于儿童期及青少年时期。根据领先的医疗保健市场研究和商业咨询公司DelveInsight估计,Stargardt病的患病率估计为1 / 8,000~10,000,全球约有80万人受此病影响,仅在美国就影响了 30,000 多人。Stargardt病是遗传性黄斑变性的最常见形式。
受限于ABCA4基因个体较大的原因,它仍然无法通过 AAV 和 CRISPR 疗法解决。针对该疾病,Ascidian的RNA外显子编辑疗法优势突出:1)RNA 层面编辑理论上是可逆的,比在 DNA 层面编辑做出的永久性改变风险低很多;2)通过替换突变的外显子,Ascidian 的技术能够针对大基因和具有高突变变异的基因进行治疗,同时保持天然基因表达模式和水平。3)由于 Ascidian 技术不引入外源酶,因此降低了不良免疫反应的风险。
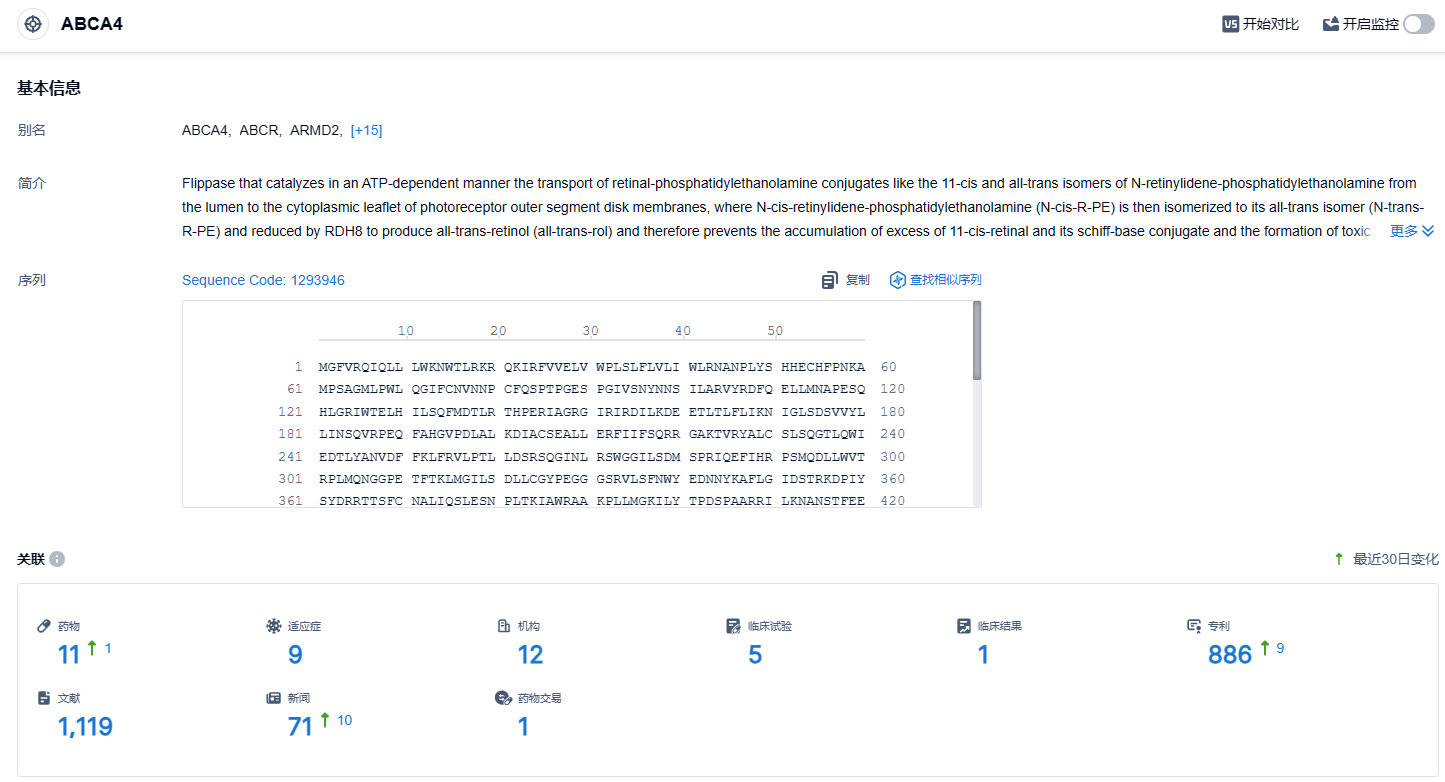
根据智慧芽新药情报库所披露的信息 (点击下方图片直达ABCA4靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年1月31日,ABCA4靶点共有在研药物11个,包含的适应症有9种,在研机构12家,涉及相关的临床试验5件,专利多达886件……目前全球针对ABCA4基因突变的在研药物有十余款,ACDN-01成为唯一针对Stargardt病遗传原因的临床阶段治疗药物。基于该RNA外显子编辑技术,当前Ascidian官网展示了其在几大治疗领域的研究现状,包括视网膜病变、神经和神经肌肉领域等。其中ABCA4先导项目为该公司的核心项目。Ascidian的方法有可能用一剂RNA外显子编辑疗法治疗患者,为亟待突破的疾病开辟新的治疗可能性。