Deciphera公布vimseltinib关键3期试验积极顶线结果,治疗腱鞘巨细胞瘤
2023年10月31日,Deciphera Pharmaceutical宣布其在研药品vimseltinib在治疗腱鞘巨细胞瘤(TGCT)患者的MOTION关键3期试验的积极顶线结果,这些患者不适合进行手术治疗。分析显示,该试验达主要终点,vimseltinib治疗组患者的客观缓解率(ORR)达统计学显著并具临床意义的改善。
vimseltinib(DCC-3014)是Deciphera Pharmaceutical开发的一款强效、具高选择性的口服CSF-1R激酶抑制剂,通过利用调节激酶构象激活的开关控制区的独特特征来选择性和有效地抑制CSF-1R,用于治疗腱鞘巨细胞瘤(3期)、色素沉着的绒毛结节性滑膜炎(3期)和实体瘤(2期)等。临床前研究显示,vimseltinib在体外和体内持久地抑制CSF-1R活性,消耗巨噬细胞和其他依赖CSF-1R的细胞,并导致在小鼠癌症模型中抑制肿瘤生长和骨退化。在一项I期临床研究中,vimseltinib治疗可调节CSF-1R抑制的生物标志物,并降低TGCT患者的肿瘤负担。
MOTION关键性3期试验是一项两部分、随机双盲、安慰剂对照研究,旨在评估vimseltinib在既往未接受过抗CSF1/CSF1R治疗、无法进行手术的TGCT患者中的疗效和安全性。分析显示,该研究在意向治疗(ITT)人群中达到主要终点,根据RECIST 1.1的盲法独立放射学审评(IRR)结果显示,在第25周时,与安慰剂相比,vimseltinib组患者具有统计学显著和临床意义的ORR改善。在ITT人群中,vimseltinib组在第25周时的ORR为40%(95% CI:29%-51%),安慰剂组为0%(95% CI:0%-9%),两组的缓解差异为40%(95% CI:29%-51%,p<0.0001)。
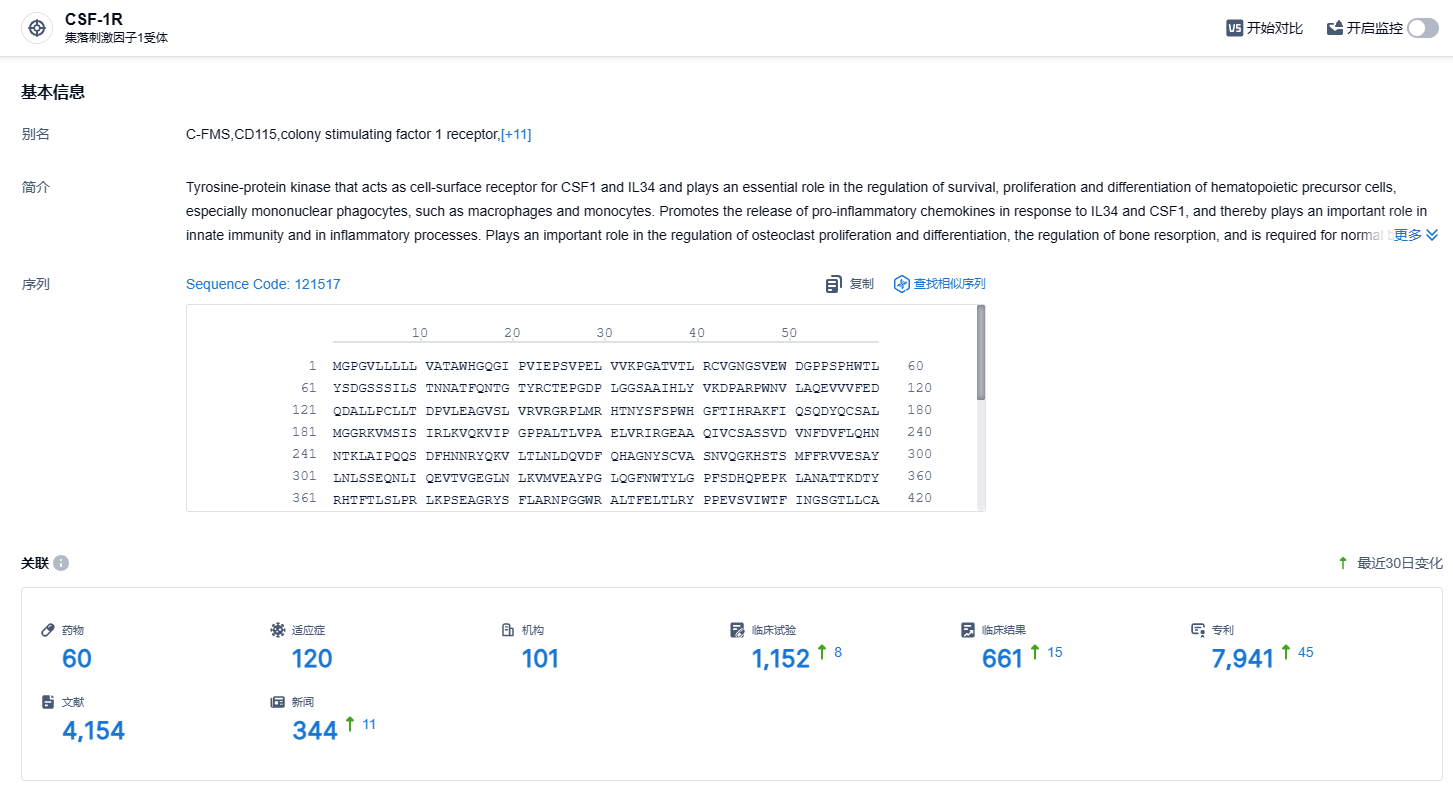
根据智慧芽新药情报库所披露的信息 (点击下方图片直达CSF-1R靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年11月1日,CSF-1R靶点共有在研药物60个,包含的适应症有120种,在研机构101家,涉及相关的临床试验1152件,专利多达7941件……CSF-1R是细胞因子CSF-1受体,同时是受体酪氨酸激酶中的重要一员,该靶点与炎症的发生、发展紧密相关。在肿瘤微环境(TME)中,CSF-1R与其配体CSF-1的信号可以传导诱导肿瘤相关巨噬细胞(TAM)的分化和存活,进而促进肿瘤细胞生长。据统计,目前获批的CSF-1R抑制剂有7款,包含第一三共的pexidartinib、诺华的尼洛替尼,和黄医药的索凡替尼等品种。期待vimseltinib能够早日获批上市。