预约演示
更新于:2025-06-30

Suzhou VAC
更新于:2025-06-30
概览
标签
感染
其他疾病
神经系统疾病
预防性疫苗
联合疫苗
结合疫苗
关联
7
项与 苏州微超生物科技有限公司 相关的药物靶点- |
作用机制 免疫刺激剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制 免疫刺激剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制 免疫刺激剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
4
项与 苏州微超生物科技有限公司 相关的临床试验CTR20231563
评价冻干ACYW135群脑膜炎球菌结合疫苗接种3月龄至6周岁健康婴幼儿后免疫原性与安全性的随机、盲法、同类疫苗对照III期临床试验
主要目的:
(1)评价3月龄受试者完成3剂基础免疫、1剂加强免疫后的免疫原性和安全性。
(2)评价6-11月龄和12-23月龄(2剂组)受试者完成2剂基础免疫、2-6周岁受试者完成1剂基础免疫后的免疫原性和安全性。
次要目的:
(1)评价6-11月龄试验组受试者加强免疫1剂后的免疫原性和安全性。
探索性目的:
(1)评价12-23月龄(1剂组)受试者完成1剂基础免疫后的免疫原性和安全性。
(2)评价3月龄试验组受试者完成1剂加强免疫后12个月和24个月的免疫持久性。
(3)评价6-11月龄试验组受试者完成加强免疫后12个月和18个月的免疫持久性。
(4)评价12-23月龄试验组受试者完成基础免疫后12个月的免疫持久性。
(5)评价2-6周岁受试者完成基础免疫后12个月、24个月和36个月的免疫持久性。
开始日期2023-05-29 |
申办/合作机构 |
CTR20230951
评价20价肺炎球菌结合疫苗接种2月龄(最小6周龄)至55周岁健康人群后安全性与初步免疫原性的随机、盲法、 阳性疫苗对照I期临床试验
初步观察20价肺炎球菌结合疫苗在2月龄(最小6周龄)至55周岁健康人群中接种的安全性和免疫原性。
开始日期2023-04-07 |
申办/合作机构  苏州微超生物科技有限公司 苏州微超生物科技有限公司 [+1] |
CTR20220680
评价13价肺炎球菌结合疫苗接种2月龄(最小6周龄)至49周岁健康人群后安全性与免疫原性的随机、盲法、阳性疫苗对照Ⅰ期临床试验
初步观察13价肺炎球菌结合疫苗在2月龄(最小6周龄)至49周岁健康人群中接种的安全性和免疫原性。
开始日期2022-03-23 |
申办/合作机构 |
100 项与 苏州微超生物科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 苏州微超生物科技有限公司 相关的专利(医药)
登录后查看更多信息
10
项与 苏州微超生物科技有限公司 相关的新闻(医药)2025-03-04
·药时空
2025年3月4日,国家药品监督管理局药品审评中心(CDE)已对苏州聚微生物提交的6价B族链球菌结合疫苗临床试验申请(IND)正式受理,注册分类1.1类,受理号:CXSL2500190。
同时2月28号,苏州聚微生物的24价肺炎球菌结合疫苗新药临床试验申请(IND)正式获得CDE受理,受理号:CXSL2500183。
据了解,本次受理的6价B族链球菌结合疫苗预测是该款:JW002。脑膜炎奈瑟球菌(Neisseria meningitidis)是一种定植在人上呼吸道的病原菌,不仅可以引起败血症和脑脊髓炎,还能通过呼吸、咽喉分泌物传播。苏州聚微生物利用重组DNA技术研制的蛋白疫苗用于预防B群脑膜炎球菌引起的疾病,填补国产疫苗空白。
值得注意的是,苏州聚微生物已布局多款肺炎和脑膜炎球菌疫苗:1)2023年5月26日,在河南省开封市祥符区黄河迎宾馆,苏州聚微/微超生物科技有限公司研制的“冻干ACYW135群脑膜炎球菌结合疫苗”III期临床试验启动会暨培训会如期召开。2)2023年3月30日,苏州聚微生物/微超生物科技有限公司20价肺炎球菌结合疫苗I期临床试验启动会暨培训会,在河南省濮阳县疾病预防控制中心召开。
苏州聚微产品管线以儿童用13价肺炎球菌结合疫苗和冻干ACYW135群脑膜炎球菌结合疫苗为基础的主流产品,20价肺炎球菌结合疫苗应用于老年人预防社区获得性肺炎及侵袭性肺炎的主力产品,该公司长期致力于开发多种技术平台应用于预防性疫苗及治疗性疫苗领域。
关于聚微生物
苏州聚微生物科技有限公司,2021年11月于苏州市吴中经济开发区注册成立,坐落于吴中生物医药产业园,致力于成为行业领先的集研发、临床及商业化生产和销售于一体的生物制药型企业,主要从事人用疫苗的研究和商业化生产,以研发生产创新疫苗和高质量疫苗为企业目标。
识别微信二维码,可添加药时空小编
请注明:姓名+研究方向!
疫苗临床3期临床1期临床申请微生物疗法
2024-09-25
肺炎是一种肺部炎症性疾病,通常由细菌、病毒、真菌或其他微生物感染而引起,细菌性肺炎占人体感染的肺炎的80%,其中肺炎链球菌是重要的病原体。早在2008年,WHO就已将肺炎球菌疾病列为需“极高度优先”使用疫苗预防的疾病。
在我国,肺炎球菌疫苗尚未被纳入我国国家免疫规划,属于自费接种疫苗。从市场规模看,据观研天下数据显示,到2026年,中国肺炎球菌疫苗市场规模将突破200亿元,年复合增长率达到18.24%。基于此,本文统计梳理了国内17家布局肺炎球菌疫苗的企业,供大家参考。以下为企业及管线详情,如有遗漏,欢迎留言补充。
相关阅读:
盘点 | 中国24家人用狂犬病疫苗企业及管线最新进展
盘点 | 中国20家流感疫苗企业及管线最新进展
盘点 | 中国12家RSV mRNA疫苗企业及管线最新进展
1、成都生物制品研究所
成都生物制品研究所有限公司成立于1958年,坐落于四川省成都市锦江区,是中国医药集团有限公司所属中国生物技术股份有限公司的全资子公司,国家高新技术企业。公司长期致力于医学微生物学、免疫学和基因工程的研究,研发与生产各类预防和治疗用生物制品、诊断制品、基因重组药物等,为国家扩大免疫规划(EPI)提供安全有效的疫苗,为预防传染性疾病做出了重要贡献。
在疫苗方面,成都所上市的产品包括杰益维(乙型脑炎减毒活疫苗)、惠益康(23价肺炎球菌多糖疫苗)、山联泰(吸附无细胞百白破联合疫苗)、皮内注射用卡介苗等。另外,在肺炎球菌疫苗上,成都所目前正在进行一项13价肺炎球菌多糖结合疫苗的I期临床试验(登记号:CTR20230671),已入组285人。
2、康泰生物/民海生物
北京民海生物科技有限公司成立于2004年6月,主营业务为人用疫苗类产品的研发、生产和销售。2008年与深圳康泰生物制品股份有限公司(股票代码:300601)实施战略重组,成为其全资子公司。公司通过自主科技创新建立了“结合疫苗技术平台”、“联合疫苗技术平台”、“基因工程疫苗技术平台”、“口服疫苗技术平台”、“疫苗质量评价平台”、“细胞无血清培养基适应和大规模培养技术平台”、“mRNA疫苗研发平台”、 “VSV载体疫苗平台”等多个现代化的新型疫苗研发技术平台。公司先后开发了近30个具有自主知识产权、国内外技术领先的创新疫苗品种。
在肺炎疫苗方面,公司上市了2款产品——13价肺炎球菌多糖结合疫苗(破伤风类毒素/白喉类毒素)和23价肺炎球菌多糖疫苗,其中“13价肺炎球菌多糖结合疫苗(破伤风类毒素/白喉类毒素)”是全球重磅品种,且第一家采用双载体蛋白结合技术,国际创新。另外,公司还布局20价肺炎球菌多糖结合疫苗,以填补国内空白,目前该疫苗已取得临床试验批件;其还在研究23价肺炎球菌多糖疫苗(新工艺)。
3、坤力生物
江苏坤力生物制药有限责任公司于2018年在苏州高新区成立,聚焦于新型细菌疫苗的研发和商业化,致力于肺炎链球菌、金黄色葡萄球菌、大肠杆菌、奈瑟氏菌、沙门氏菌、鲍特氏菌等细菌所导致感染性疾病负担的减轻与消除。
公司拥有多款在研肺炎球菌疫苗,包括13价肺炎球菌多糖结合疫苗、20价肺炎球菌多糖结合均处于临床Ⅰ期,24价肺炎球菌多糖结合疫苗处于临床Ⅰ/Ⅱ期,此外,公司还在研究PCV系列迭代疫苗。
4、科兴生物
科兴控股生物技术有限公司(SINOVAC科兴)是一家总部位于北京的生物高新技术企业,目前在美国纳斯达克全球精选市场(Nasdaq-GS:SVA)上市。公司通过全资子公司科兴控股(香港)有限公司拥有北京科兴生物制品有限公司、北京科兴中维生物技术有限公司、科兴(大连)疫苗技术有限公司等多家企业,在北京海淀、昌平、大兴及辽宁大连拥有四个产业基地,并在海外多国推进生物医药产品研发和产业化合作。
SINOVAC科兴以“为人类消除疾病提供疫苗”为使命,致力于人用疫苗及其相关产品的研究、开发、生产和销售,为疾病预防控制提供服务。公司上市产品主要包括新型冠状病毒灭活疫苗(克尔来福®)、肠道病毒71型灭活疫苗(益尔来福®)、中国第一支甲型肝炎灭活疫苗(孩尔来福®)、三价流感病毒裂解疫苗(安尔来福®)和四价流感病毒裂解疫苗、水痘减毒活疫苗、腮腺炎减毒活疫苗、23价肺炎球菌多糖疫苗、Sabin株脊髓灰质炎灭活疫苗等。
其中,23价肺炎球菌多糖疫苗是科兴首个细菌类疫苗产品,于2020年12月2日获批上市。另外,在肺炎疫苗方面,据药物临床试验登记与信息公示平台显示,科兴正在进行多项关于13价肺炎球菌多糖结合疫苗以及24价肺炎球菌多糖结合疫苗的临床试验,大多处于临床I期。值得注意的是,其中有2项针对13价肺炎球菌疫苗的临床试验主动暂停了。
5、沃森生物
沃森生物成立于2001年,并于2010年在深交所创业板上市。经过20余年的发展,公司现已成为国内专业从事人用疫苗等生物技术药物集研发、生产、销售于一体的现代高技术生物制药企业。目前,公司自主研发并生产上市的疫苗产品已达 8个品种共12个品规,涵盖肺炎疫苗系列、脑膜炎疫苗系列、HPV 疫苗、Hib疫苗和百白破疫苗,全面覆盖 6 周龄以上全年龄段人群。
其中,肺炎球菌疫苗上市产品包括13价肺炎结合疫苗(西林瓶型和预灌封型)和23价肺炎多糖疫苗(西林瓶型和预灌封型)。公司是中国首家、全球第二家自主研发并成功上市13价肺炎结合疫苗的企业,该产品自2021年至今持续保持中国市场份额第一,打破了国际巨头在婴幼儿肺炎疫苗领域20年的垄断。
6、智飞生物/智飞绿竹
重庆智飞生物制品股份有限公司成立于2002年,是一家集疫苗、生物制品研发、生产、销售、推广、配送及进出口为一体的国际化、全产业链生物高科技企业。公司于2010年9月在深交所挂牌上市,为第一家在创业板上市的民营疫苗企业,旗下五家全资子公司及两家参股公司,其中北京智飞绿竹生物制药有限公司及安徽智飞龙科马生物制药有限公司为高新技术企业。
目前,公司共有13种产品上市在售,1种产品附条件上市,包括预防流脑、宫颈癌、肺炎、轮状病毒、带状疱疹等传染病的疫苗产品,也涵盖提供结核感染诊断、预防、治疗有效解决方案的药品,覆盖人群包括婴幼儿、青少年、成人;自主研发项目共计32项(不含新冠系列项目),其中处于临床试验及申请注册阶段的项目18项。
在肺炎球菌疫苗产品方面,智飞绿竹研发的23价肺炎球菌多糖疫苗于2023年8月29日获批上市,15价肺炎球菌结合疫苗处于III期临床试验,26价肺炎球菌结合疫苗处于I/II期临床试验。值得注意的是,公司的26价肺炎球菌结合疫苗是目前国内已获批临床试验的最高价次的同类产品。
7、康希诺
康希诺生物股份公司成立于2009年,致力于在世界范围内提供预防和治疗感染类疾病的解决方案。公司现有病毒载体疫苗技术、合成疫苗技术、蛋白结构设计和VLP组装技术、mRNA技术、制剂及给药技术五大创新疫苗平台技术。目前,康希诺生物已建立覆盖10余种适应症的多款创新疫苗产品,包括亚洲首款四价流脑结合疫苗曼海欣®、二价流脑结合疫苗美奈喜®、获得世卫组织认可的新冠疫苗克威莎®、全球首款吸入用新冠疫苗克威莎®雾优®以及亚洲首个重组埃博拉病毒病疫苗。
在肺炎球菌疫苗方面,公司共有3款在研产品:
PCV13i(CRM197/TT双载体),目前处于上市申请获受理阶段。PCV13i采用多糖抗原与蛋白载体共价结合的方式,多糖抗原连接载体蛋白后,多糖可以转化为T细胞依赖性抗原,不仅可以在2岁以下婴幼儿体内诱导出很高的特异性抗体水平,还可以产生记忆性B细胞,产生免疫记忆。同时,公司采用双载体技术,可减少与其他疫苗共注射时对免疫原性造成的免疫抑制。在生产工艺上,公司采用了更加安全的生产工艺,发酵培养基采用无动物来源培养基,降低了动物源生物因子造成的风险,且避免了传统纯化工艺采用苯酚方法带来的毒性残留。
PBPV-重组肺炎球菌蛋白疫苗,目前处于临床Ib期。PBPV是全球创新的在研肺炎疫苗,其主要采用基于肺炎球菌表面蛋白A(PspA,一种几乎所有肺炎球菌表达的高度保守蛋白)的抗原,相较于目前上市的PPV23、PCV13,PBPV具有更高血清覆盖率(至少98%的肺炎球菌株覆盖率)。在高覆盖率保护下,可以有效防止“血清型替代”的产生。同时该产品相较多糖疫苗和结合疫苗,生产工艺更为简便,易于放大和质量控制。
公司的PBPV已获得Ⅰ期临床积极初步结果:Ⅰa期及Ⅰb期临床研究结果表明,PBPV 在成人及老年人群中具有良好的安全性,未观察到3级不良反应和特殊的安全性风险;同时,单剂接种即可诱导显著的结合抗体,以及针对跨家族/亚类肺炎链球菌的功能性杀菌抗体应答,进一步证明了该候选疫苗的广谱性和潜在公共卫生价值。公司将基于Ⅰ期临床试验中获得的初步结果,进行下一阶段PBPV研发工作的评估和规划。
CS-2028多价肺炎结合疫苗,目前处于临床前研究。
8、艾美疫苗
艾美疫苗成立于2011年,并于2022年在港交所上市。其是中国大型全产业链民营疫苗集团,业务涵盖从研发到制造、再到商业化的整个行业价值链。目前全资控股4家持证疫苗生产企业,分别为艾美诚信、艾美行动、艾美坚持及艾美荣誉。控股3家研究院,其中2018年建成的研发中心——艾美探索者,专注于对各家工厂研发部门的早期及尖端研究提供技术支持。艾美于2021年并购了珠海丽凡达生物技术有限公司,该公司是国内最早获得mRNA新冠疫苗临床试验批件的3家企业之一,拥有自主mRNA生产和药物递送技术平台。
目前,公司拥有针对6个疾病领域的8款商业化疫苗,以及针对13个疾病领域的21种在研创新型疫苗。其中,在肺炎球菌疫苗方面,公司开发了一系列迭代升级的产品:
13价肺炎结合疫苗已经完成了上市预申请,药品注册前置检验结果符合质量标准,已完成基础阶段揭盲统计,正在加速推进上市注册工作。
23价肺炎多糖疫苗已完成III期临床试验现场工作,处于锁库前的准备阶段,即将揭盲进行统计分析,计划提交上市注册预申请。
20价肺炎结合疫苗已提交临床试验预申请。
全球同步首研的24价肺炎结合疫苗已完成临床前研究工作。
9、普大生物
普大生物科技(泰州)有限公司于2022年成立,位于泰州中国医药城,是一家专注于创新型人用疫苗的研发、生产和商业化的高科技企业。由多位国外著名研究院及疫苗公司从事疫苗产品研发及生产的博士团队组成。公司已建立多项疫苗开发技术平台,包括合成技术主要开发多糖蛋白结合类疫苗,纳米颗粒重组蛋白技术主要开发病毒类疫苗,脂蛋白重组蛋白技术主要开发细菌类疫苗,基因编辑技术致力于开发填补世界空白疫苗产品。
公司产品目标是以AI赋能,开发能够取代或更新市场上现有的产品,并且具有巨大市场潜力的产品,如通用性流感纳米颗粒重组蛋白疫苗、肺炎-脑膜炎联合疫苗等。公司目前已形成三个核心技术平台:(1)CDAP-TEC技术平台:开发多价肺炎多糖结合疫苗,及相关技术系列产品;(2)Nano-P技术平台:RSV重组蛋白疫苗,VZV重组蛋白疫苗,及相关技术产品系列产品;(3)Dual-VLP技术平台:开发同时预防两种疾病的VLP疫苗。公司产品管线主要为新型及覆盖型疫苗,包括进入IND生产的多价肺炎多糖结合疫苗、呼吸合胞病毒重组蛋白疫苗、带状疱疹重组蛋白疫苗,及临床前研究的其它疫苗产品。
10、复星安特金
复星安特金(成都)生物制药有限公司是覆盖疫苗研发及生产全产业链能力的领先疫苗企业,于2021年10月26日加入上海复星医药(集团)股份有限公司,成为疫苗事业部核心成员企业。公司坚持以创新研发为核心驱动因素,拥有全球首创、具有自主知识产权的多价结合体疫苗技术;拥有国内领先的无弹状病毒SF9昆虫细胞系、无诺达病毒Hi5昆虫细胞系疫苗技术;减毒/灭活疫苗技术;初步布局mRNA技术及多联多价疫苗技术。
在肺炎球菌疫苗方面,公司的13价肺炎球菌结合疫苗(多价结合体)处于临床Ⅲ期,据复星医药此前的会议交流纪要,公司预期该产品有望在2026年上市并实现销售;23价肺炎球菌多糖疫苗已获临床试验默示许可;此外还有一款24价肺炎球菌结合疫苗。
11、瑞宙生物
上海瑞宙生物科技有限公司于2017年9月由资深归国专家创办,是一家注重自主研发的高新生物技术制药企业,专注于国际先进的创新生物制品的研发和产业化。公司的研发中心位于上海张江科学城。公司建有完整的创新生物制品研发技术平台,一个严格的质量管理体系,培养了一支专业敬业团队,可以开展从基因工程、发酵、纯化、偶联、免疫、临床医学、质量分析等方面的研发工作,有效推进新型疫苗、抗体及重组蛋白类药物的发现、临床前研发、及工艺放大。
4月17日,瑞宙生物自主研发的24价肺炎球菌多糖结合疫苗在江苏省邳州市启动II期临床试验。此次开展的临床II期试验将在18岁及以上成年人、老年人群中免疫接种一针,进一步研究24价肺炎球菌多糖结合疫苗的安全性及免疫效果。
12、微超生物
苏州微超生物科技有限公司成立于2017年5月,以“引领疫苗科技,助力健康中国“为宗旨,致力于高质量人用疫苗及治疗产品的开发,是一家以人用疫苗研发、生产和销售为一体的生物技术企业。
目前公司已建设形成细菌高密度发酵培养、细菌多糖纯化、细菌蛋白质纯化、结合疫苗制备、疫苗制剂、疫苗佐剂、分子生物学技术和免疫学技术平台,为相关产品研发和生产奠定了技术基础。在此基础上,公司立项研发的疫苗产品有4价脑膜炎球菌结合疫苗、13价和20价肺炎球菌结合疫苗、第一代和第二代新型DTaP疫苗及其联合疫苗、基因重组B群脑膜炎球菌疫苗和疫苗佐剂等产品课题,并积极布局预防病毒性疾病的相关疫苗。其中,13价和20价肺炎球菌结合疫苗均处于临床Ⅰ期。
13、华安科创
北京华安科创生物技术有限公司专注于生物制药的科技公司,致力于治疗性及预防性生物制品的临床前研究及自主研发。该公司建立了完整的细菌疫苗与重组蛋白研发平台。
2017年11月21日,华安科创申报的23价肺炎球菌多糖疫苗获得国家食品药品监督管理总局的《药物临床试验批件》。该产品由康希诺生物转让予华安科创,并在产品开发及生产过程中持续提供技术支持。据药物临床试验登记与信息公示平台显示,华安科创已于2023年4月27日完成了23价肺炎球菌多糖疫苗的Ⅰ期临床试验,目前暂未查询到该产品进一步的进展。
14、博沃生物
武汉博沃生物科技有限公司成立于2012年,是一家专业从事高端人用疫苗研发、制造与市场销售的“国家级高新技术企业”。公司致力于新型新冠疫苗、人用多价轮状病毒疫苗、新型肺炎球菌结合疫苗、广谱HPV疫苗、重组带状疱疹疫苗等重量级产品的开发与产业化。
在肺炎球菌疫苗方面,博沃生物与辽宁成大合作研发的13价肺炎球菌结合疫苗目前处于临床Ⅰ期;另外,公司还布局了下一代肺炎球菌结合疫苗——利用公司已有成熟的13价肺炎球菌结合疫苗的工艺基础以及结合疫苗研发的实际经验,进一步开发13价以上肺炎球菌结合疫苗的研究,可极大缩短研发周期。
15、成大生物
辽宁成大生物股份有限公司成立于2002年,专注人用疫苗的研发、生产与销售,并于2021年10月28日在上交所科创板上市。公司主要上市产品为人用狂犬病疫苗(Vero细胞)、人用乙脑灭活疫苗(Vero细胞);主要在研产品包括人用二倍体狂苗、四价/三价流感疫苗、15价HPV疫苗、13价和20价肺炎疫苗、重组带状疱疹疫苗、B群流脑疫苗、多价手足口疫苗、狂犬病单抗等。
在肺炎球菌疫苗研发方面,公司的13价肺炎疫苗处于Ⅰ期临床试验阶段,并已完成I期临床基础免疫;20价肺炎结合疫苗处于临床前研究中。
16、金迪克生物
江苏金迪克生物技术股份有限公司成立于2008年12月,是一家集人用疫苗科研、生产、经营、服务为一体的生物高科技企业,于2021年在上海证券交易所科创板上市。公司已形成四大核心平台技术,产品管线已实现了对流行性感冒、狂犬病、水痘、带状疱疹和肺炎疾病等5种重要传染性疾病预防的覆盖。其中已上市销售的产品1个,为四价流感病毒裂解疫苗。
在肺炎球菌疫苗研发方面,公司的23价肺炎球菌多糖疫苗、13价肺炎球菌多糖结合疫苗均处于临床前研究阶段。
17、荣盛生物
上海荣盛生物药业股份有限公司历史可追溯至1988年成立的荣盛试剂厂,一家专注于疫苗和体外诊断试剂研发生产销售的现代生物医药企业,三十多年来一直秉承“质量放心、朋友诚心、员工安心”的三心价值观,成长为我国生物医药领域的长青品牌。公司目前拥有包括已授权以及在申请的专利近50项,除水痘疫苗产品外,公司还拥有免疫及生化诊断试剂近60项产品。
目前,公司有8项疫苗在研项目,分别为细胞工厂工艺水痘减毒活疫苗研制及临床研究、新建年产1,000万人份水痘减毒活疫苗生产线及工艺开发和可比性研究、13岁及以上人群水痘减毒活疫苗、冻干人用狂犬病疫苗(Vero细胞)、冻干人用狂犬病疫苗(人二倍体细胞)、水痘-带状疱疹疫苗、四价流感病毒裂解疫苗(MDCK细胞)和16价肺炎球菌多糖结合疫苗等。其中,16价肺炎球菌多糖结合疫苗处于临床前研究阶段。
参考资料:
[1]突然降价三成!又一领域开打“价格战”.21世纪经济报道.2024年09月05日.
[2]下降近3成!肺炎疫苗打响降价第一枪.界面新闻.2024年09月04日.
[3]国家药品监督管理局药品审评中心,药物临床试验登记与信息公示平台,各公司官网、官微、财报等.
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
疫苗信使RNA临床1期
2024-08-11
随着全球人口老龄化和疾病模式的变化,对创新药物的需求不断增加。患者和医疗保健提供者正在寻求更有效、更安全、更个性化的治疗方案,这推动了对创新药的强烈需求。不同国家和地区的监管机构,对创新药物的审评审批标准和流程有着不同的要求。国际人用药品注册技术协调会(ICH)制定了一系列关于药品研发、生产和监管的国际指南,被广泛认为是创新药物研发和临床质量控制的国际标准。
近年来为了更快与国际市场接轨,增强患者多样性,增加公司收入来源的多元化,中国的生物技术公司纷纷寻求产品“出海”之路。为此,国际创新药临床质量需要适应这些多样化的监管环境,确保药物在全球范围内的合规性和可接受性。
8月29日(周四)下午,佰傲谷BioValley联合赛默飞世尔科技,举办创新药临床试验国际化策略私享沙龙—苏州站,以期帮助更多新药蛟龙入海,走向世界。
活动信息
活动时间:2024年8月29日 13:30-20:00
活动地点:苏州工业园区星湖街218号B2栋一楼—生物医药产业综合服务中心
活动规模:40位药企研发及管理人员(闭门会,需审核)
主办单位:赛默飞世尔科技、佰傲谷BioValley
拟邀参会:博瑞生物、盛禾生物、丹诺医药、清普生物、迈诺威医药、宁丹新药、海融医药、勤浩医药、润佳医药、星锐医药、映恩生物、拜恩泰科、苏州玉森新药开发有限公司、新元素医药、奥赛康药业、开拓药业、征祥医药、韬略生物、鑫康合生物医药、苏州信诺维医药、微超生物、浦合医药、康宁杰瑞、中科健康、南京泛太化工医药研究所、坤力生物、峻德生物、亚虹医药、吴中医药、润新生物、江苏威凯尔、阿思科力、亚盛医药、康乃德生物医药、兴盟生物、典晶生物、宜联生物等企业高级经理及以上……
扫码报名(需审核)
日程安排
创新药临床试验国际化策略私享沙龙·苏州站
2024年8月29日(周四)下午
13:30-14:00
活动签到
14:00-14:10
主持开场
14:10-14:40
主题演讲1:2024年医药投资趋势---中国创新药出海机遇与挑战
王海蛟 高特佳 副总经理
14:40-15:10
主题演讲2:生物药的临床质量控制原则与经验分享(拟)
顾明洋 昂科免疫 QA总监&总经理助理
15:10-15:40
主题演讲3:自体细胞治疗产品海外落地初探分享
刘超 禾沐基因 CEO
15:40-16:00
茶歇、休息交流
16:00-16:30
主题演讲4:以国际经验深耕中国,助力生物医药研发创新和国际化
神秘大咖
16:30-17:00
主题演讲5:多国家多地区临床试验中的操作和项目管理趋势及亮点
施维维 赛默飞Patheon制药服务 临床供应链中国质量负责人
17:00-17:40
圆桌讨论:创新药出海的底层逻辑探讨
讨论嘉宾:
王海蛟 高特佳 副总经理
顾明洋 昂科免疫 QA总监&总经理助理
刘 超 禾沐基因 CEO
施维维 赛默飞Patheon制药服务 临床供应链中国质量负责人
其它嘉宾邀请中....
17:40-17:50
总结、合影
17:50-20:00
冷餐会
联系我们
本次活动为报名审核制,请仔细填写报名信息临床、研发部门优先录取。截止目前,20位药企管理人员已加盟~
扫码下方二维码报名
审核成功后将以短信和邮件通知
审核未通过者不予参加活动
如您有任何问题,欢迎联系小助手:Abby Jiang 18217659261
点击此处“阅读全文”查看更多内容
细胞疗法ASH会议临床研究申请上市医药出海
100 项与 苏州微超生物科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 苏州微超生物科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年09月02日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床前
2
2
临床1期
临床3期
1
2
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
ACYW135群脑膜炎球菌结合疫苗(苏州微超生物科技) | 脑膜炎 更多 | 临床3期 |
20价肺炎球菌结合疫苗(苏州微超生物) | 肺炎球菌感染 更多 | 临床1期 |
13价肺炎球菌结合疫苗 (苏州超微) | 肺炎球菌感染 更多 | 临床1期 |
新型DTap组分疫苗(苏州微超生物科技) | 百日咳 更多 | 临床阶段不明 |
B群流脑结合疫苗(苏州微超生物科技) | 脑膜炎 更多 | 临床阶段不明 |
登录后查看更多信息
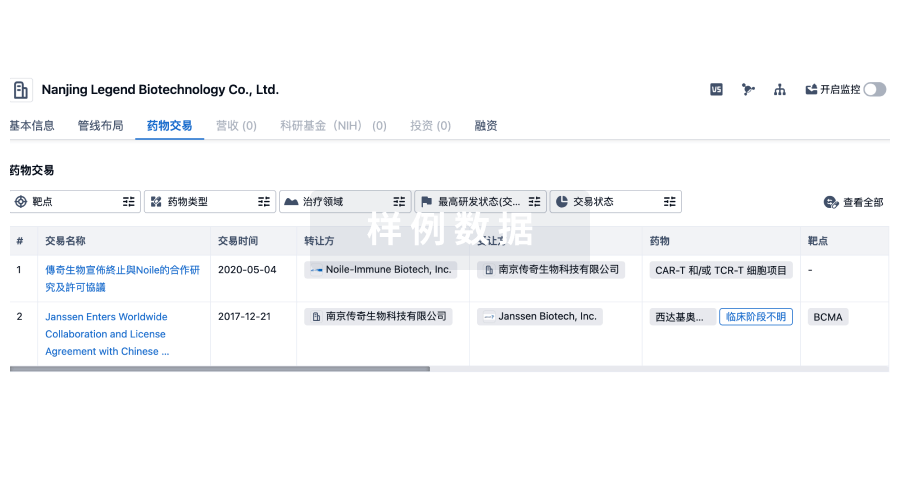
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
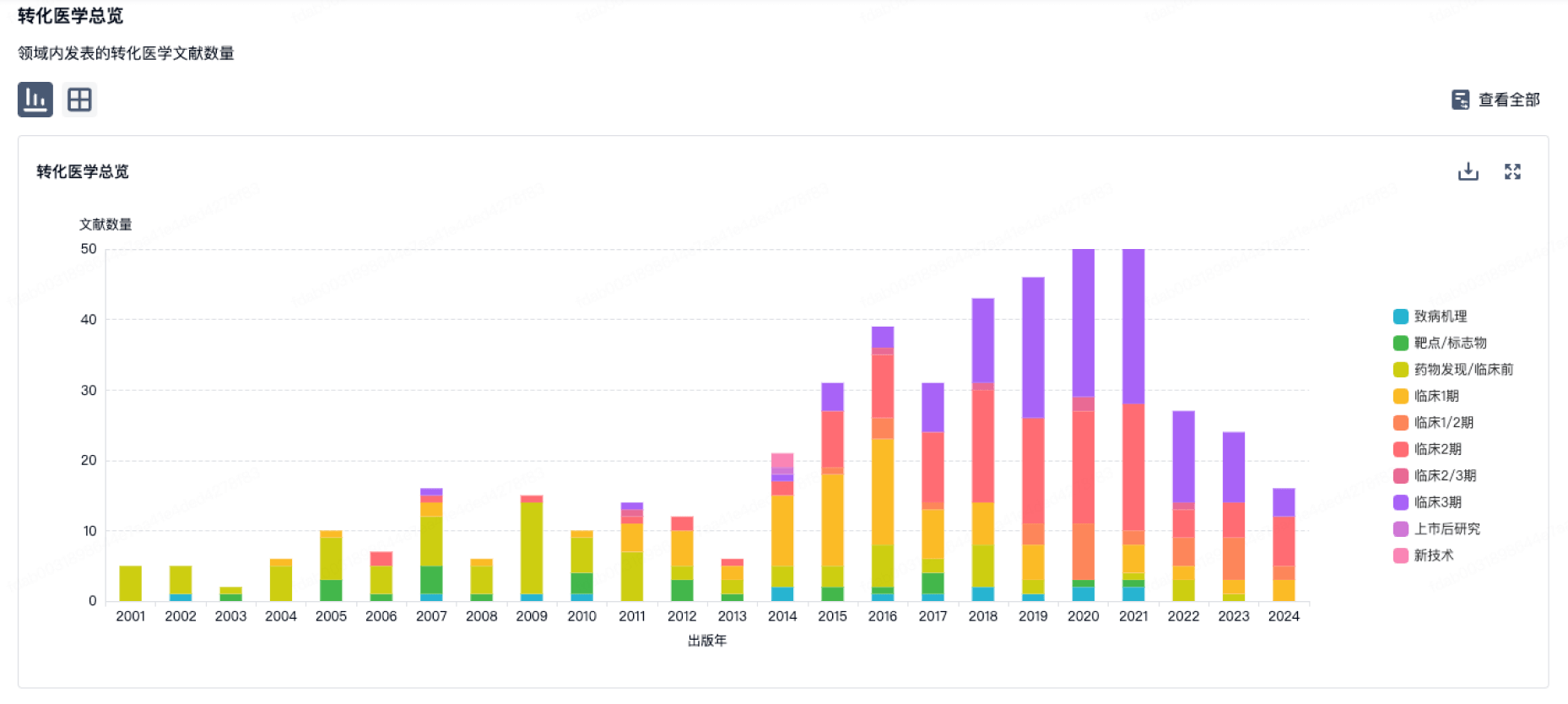
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
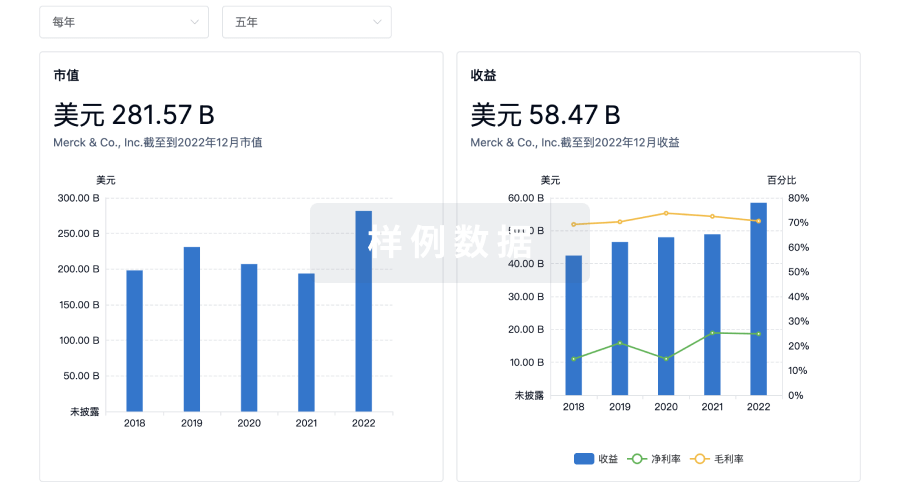
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
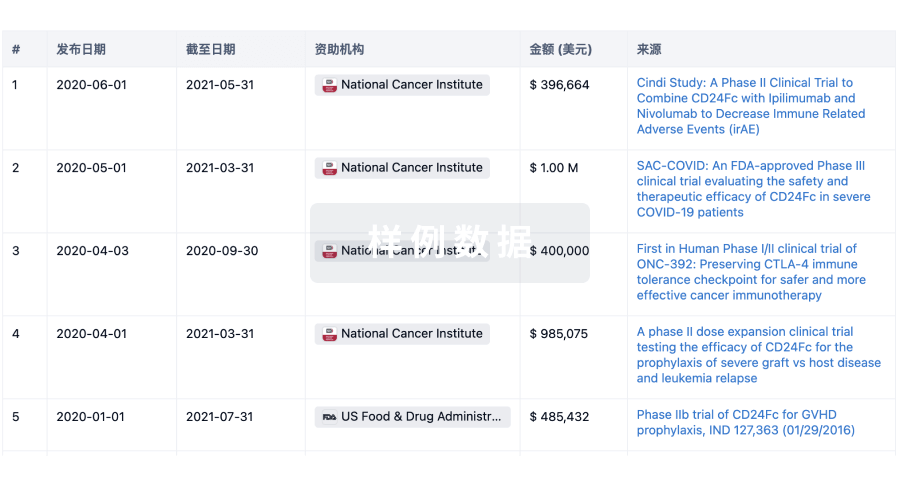
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
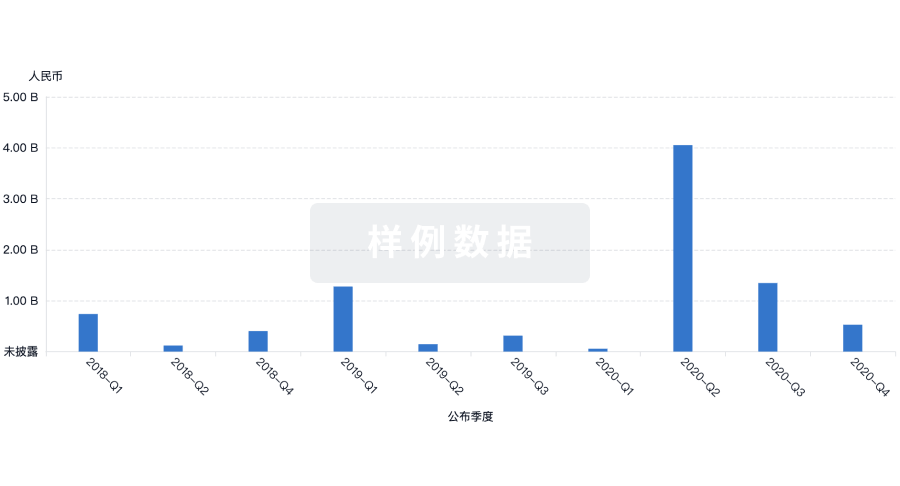
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
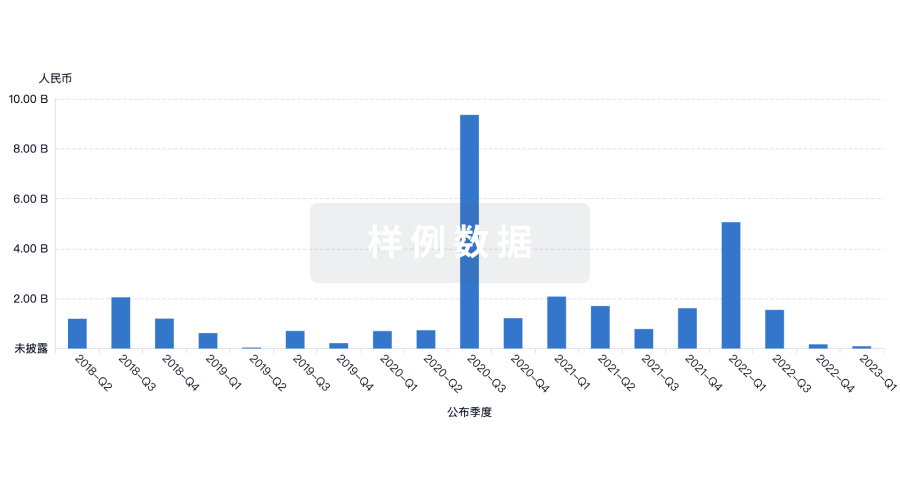
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用