预约演示
更新于:2025-05-07

Chengdu Weisk Biopharmaceutical Co., Ltd.
更新于:2025-05-07
概览
标签
感染
肿瘤
消化系统疾病
mRNA疫苗
预防性疫苗
疫苗
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| mRNA疫苗 | 18 |
| 预防性疫苗 | 16 |
| 疫苗 | 16 |
| 治疗性疫苗 | 13 |
| 重组亚单位疫苗 | 4 |
关联
67
项与 成都威斯克生物医药有限公司 相关的药物作用机制 SARS-CoV-2 S protein抑制剂 |
在研适应症 |
非在研适应症- |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2022-12-05 |
作用机制 SARS-CoV-2 S protein抑制剂 [+1] |
在研机构 |
原研机构 |
在研适应症- |
非在研适应症 |
最高研发阶段申请上市 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制 免疫刺激剂 |
在研机构 |
原研机构 |
在研适应症- |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
12
项与 成都威斯克生物医药有限公司 相关的临床试验NCT05911061
A Multicenter, Randomized, Double-Blind, Controlled, Phase Ⅲ Clinical Trial of Recombinant COVID-19 Trivalent (XBB+BA.5+Delta) Protein Vaccine (Sf9 Cell) in Booster Vaccination to Evaluate Efficacy, Safety and Immunogenicity in Population Aged 18 Years Old and Above
A Phase Ⅲ Clinical Trial of Recombinant COVID-19 Trivalent (XBB+BA.5+Delta) Protein Vaccine (Sf9 Cell) in Booster Vaccination to Evaluate Efficacy, Safety and Immunogenicity
开始日期2024-12-30 |
申办/合作机构 |
NCT05911048
A Clinical Trial to Evaluate the Safety and Immunogenicity of Recombinant COVID-19 Bivalent (XBB+Prototype) Protein Vaccine (Sf9 Cell) (WSK-V101C) in Booster Vaccination in Healthy Population 18 Years Old of Age and Above
A Clinical Trial of Recombinant COVID-19 Bivalent (XBB+Prototype) Protein Vaccine (Sf9 Cell) in Booster Vaccination to evaluate safety and immunogenicity in healthy population aged 18 years old and above.
开始日期2024-12-30 |
申办/合作机构 |
NCT05013983
Single-center, Randomized, Double-blind, Placebo-controlled Phase I/II Clinical Trial to Evaluate the Safety, Tolerability and Immunogenicity of Recombinant COVID-19 Vaccine (Sf9 Cells) in Healthy People Aged 6-17 Years
This is a phase Ⅰ/Ⅱ, single-center, randomized, double-blind, placebo-controlled study, to evaluate the safety, tolerability and immunogenicity of the recombinant COVID-19 vaccine (Sf9 cells) in the subjects from healthy aged 6-17 years with immunization procedures 0, 21, 42 days and doses (10μg/20μg/40μg).
开始日期2024-07-01 |
申办/合作机构  成都威斯克生物医药有限公司 成都威斯克生物医药有限公司 [+1] |
100 项与 成都威斯克生物医药有限公司 相关的临床结果
登录后查看更多信息
0 项与 成都威斯克生物医药有限公司 相关的专利(医药)
登录后查看更多信息
1
项与 成都威斯克生物医药有限公司 相关的文献(医药)2025-05-01·International Journal of Biological Macromolecules
Molecular basis of two broad-spectrum antibodies neutralizing rabies virus and other phylogroup-I lyssaviruses by blocking structural transition between the pleckstrin-homology and fusion domains in the glycoprotein
Article
作者: Lin, Sheng ; Yu, Yueru ; Wang, Wei ; Ye, Fei ; Yang, Jing ; Yang, Fanli ; He, Bin ; Yin, Keqing ; Lu, Guangwen ; Cao, Yu ; Zhai, Lili ; Ye, Haoyu ; Gao, Jian ; Chen, Zimin ; Shu, Siqi ; Guo, Liyan
213
项与 成都威斯克生物医药有限公司 相关的新闻(医药)2025-05-03
21 年 8 月,沃森市值还在 1500 亿,如今却只剩下不到 200 亿。为了重回巅峰,沃森一方面不断加大研发投入(去年研发支出占总营收 25%),一方面计划贷款 28 亿元,在未来 2 年内,启动对疫苗主业资产的整合并购。目前,沃森账面上差不多还有 30 多亿,加上贷款,能用于并购的资金还是很充裕的。那么,国内哪些疫苗公司有可能被沃森收购呢?据统计,目前,国内大大小小的疫苗公司(疫苗项目占比在 80% 以上)有 200 多家,已经上市的有十几家,包括智飞生物、艾美疫苗、康泰生物、康希诺、华兰疫苗、欧林生物、瑞科生物、康乐卫士等等。来源:Insight 数据库以沃森生物手里的资金量来说,康乐卫士、瑞科生物(市值在 50 亿元内)虽然在承受范围内,但这几个公司核心管线(HPV 疫苗)重叠程度太高了,代价也比较大,不大可能被收购。反而是那些还未上市的初创 Biotech,可能性更大。企业并购要么是为了强化优势市场,要么是为了补齐管线缺口。沃森主要专注于细菌性疫苗、重组蛋白疫苗、mRNA 疫苗和重组腺病毒疫苗 4 个方向,其中 mRNA 是它最看中的领域,未来很有可能继续在这个方面发力。国内威斯津生物、蓝鹊生物、艾博生物、启辰生物、深信生物、瑞吉生物、嘉晨西海等,都有着较为丰富的 mRNA 疫苗管线。其中,蓝鹊、艾博还跟沃森有过合作,虽然最后没什么结果,但有合作基础总归是好一些。而且蓝鹊又在沃森预算内,被收购可能性还是很大的。不过,最终沃森会对哪个公司出手,还得交给时间来验证。封面来源:企业logo免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。编辑:月牙PR 稿对接:微信 insightxb投稿:微信 insightxb;邮箱 insight@dxy.cn
疫苗信使RNA并购
2025-04-19
·同写意
以“医药健康产业的变革与新生”为主题,汇聚行业领袖,聚焦创新药械和消费医疗,探讨产业变革,交流商业保险与AI技术带来的机遇,助力行业新生。火热报名中属于mRNA技术的春风,眼看着再度吹起。大洋彼岸,曾在大流行中风头无两的Moderna,近期宣布2027年有望推出首款肿瘤mRNA疫苗;海的这边,Biotech云顶新耀则透露,其个性化肿瘤疫苗已完成首例给药,通用型肿瘤疫苗申报FDA IND。后COVID-19时代,mRNA领域亟需一场伟大的全面胜利,为自己接下来的前景证明。而肿瘤疫苗这个曾几度受挫的大药市场,显然成为不少玩家的优选项。随着探索推进,产品商业化节点近在眼前。但想要从中分一杯羹,仍需厘清一些关键问题。1新的叙事有目共睹,是COVID-19将mRNA疫苗技术从概念推向大规模市场应用,催生了一大批“新神”。例如,被辉瑞相中的BioNTech,后来确实让它赚得盆满钵满。2022年,凭借COVID-19 mRNA疫苗,辉瑞揽获高达378亿美元的营收。Moderna也不例外,在其产品的推动下,同期录得184亿美元销售额。问题在于,COVID-19终究是过去了。2020年以来,行业见证了太多棋差一招、满盘皆输的案例。就连辉瑞、Moderna这些抢滩成功者,也不得不在瘟疫之后,在财报和股价的压力下,考虑巨轮的转向。尽管Biotech陆续出清,一批被高高捧起的明星公司迅速销声匿迹,但这大概并非mRNA技术的问题。事实上,2024年,Moderna就成功推出了RSV mRNA疫苗,为自己打开了第二条销售增长线。只不过,比起COVID-19来说,RSV能给到Moderna的空间还是太小了,mRNA产品也仍需更多的突破,例如在抗肿瘤市场。mRNA灵活高效的模式,更容易应对肿瘤的抑制性和个体的差异化,在其他技术手段无法介入下形成的天然空窗,mRNA肿瘤疫苗顺其自然成为企业的着力点。有专家学者指出,mRNA技术是进一步补充肿瘤治疗武器库的后备力量。肿瘤免疫治疗近年来非常火热,CAR-T细胞疗法、PD-1已经走入公众视野,但它们只对一部分肿瘤有效,例如CAR-T目前主要治疗血液瘤, PD-1对肺癌仅有20%左右的疗效。如果想进一步扩充肿瘤治疗的武器库,需要肿瘤疫苗等新技术,“目前有很多肿瘤疫苗已经进入临床试验阶段,前景还是很好的”。尽管暂时无法和巨人比肩,纵观国产mRNA肿瘤疫苗赛道,亦是一派百舸争流。年初至今,国产mRNA疫苗企业相继迎来里程碑事件:• 1月,北京启辰生生物首款治疗原发性脑胶质母细胞瘤的mRNA-DC肿瘤疫苗正式启动I期临床试验的患者入组工作;• 3月6日,云顶新耀个性化肿瘤疫苗EVM16完成首例给药;• 3月10日,新合生物依托AI技术研发的个性化新抗原治疗性mRNA疫苗XH001临床试验申请获CDE受理:• 3月下旬,星锐医药个性化肿瘤疫苗STR-V005完成首例患者给药;3月24日,云顶新耀通用型现货肿瘤治疗性疫苗EVM14获FDA IND批准。国内mRNA肿瘤疫苗主要在研企业(数据来源:公开资料)国产mRNA肿瘤疫苗已经拉开竞跑序幕,如何实现从跟跑到领跑,更考验企业的底层技术。2技术为王可以确定的是,mRNA疫苗相较于传统癌症疫苗有着显著优势,包括高效诱导保护性免疫反应、副作用较低且生产成本更低。但mRNA疫苗成药,面临着两个关键性问题:稳定性差、体内递送困难。首先,mRNA作为长的单链核苷酸,序列非常不稳定,容易发生断裂,在质量控制和生产上难度颇高。其次,因为它的不稳定性,极易被人体内和空气中的RNA酶降解,如何稳定地将其递送至靶细胞成为另一难点。新合生物自主研发的核心平台NeoCura AI ALPINE通过整合肿瘤基因组学、转录组学及蛋白质组学数据,结合干湿实验闭环验证,将新抗原预测能力提升至行业领先水平,为个性化治疗奠定了技术基础。并依托AI与RNA技术深度融合的创新模式,成功攻克了新抗原预测精度、mRNA递送系统稳定性及规模化生产等关键挑战。攻克底层技术,并转化为自己的专利,正在成为行业共识。靶向递送系统是mRNA技术产业化的关键一环,也是该领域新药研发中最容易出现的“短板”之一。为打破LNP递送系统的国际专利壁垒,威斯津生物首创新一代mRNA递送系统。威斯津生物联合创始人宋相容称,新一代mRNA递送系统通过多氮可电离脂质替代已上市的LNP中的单氮可电离脂质,结合中心组合设计策略,进而提高LNP的靶向性、体内安全性和贮存稳定性,开创出mRNA药物递送的全新技术。该技术于2023年8月获得美国专利授权;2024年,多氮可电离脂质再获中国发明专利授权。站在中国生物医药的DeepSeek时刻,AI理所当然成为兵家必争之地。mRNA技术背后所涉及的巨量蛋白、基因、转录和代谢组学数据,天然地和AI做一个强有力的结合。AI辅助抗原设计和序列优化对疫苗的蛋白表达量、细胞免疫、体液免疫水平,疫苗的有效性、稳定性、成药性、专利保护性,以至于最后的临床数据,和真实世界保护效力和安全性,起到至关重要的作用。有业内专家直言,对于小分子研发来说,AI是个可选项,但对mRNA尤其是肿瘤疫苗,AI是个必选项。这也体现在新合生物不久前获批临床的XH001注射液。该疫苗通过高通量测序技术对患者样本进行深度突变谱分析,再运用自主研发的NeoCura AI ALPINE肿瘤新抗原预测平台筛选高免疫原性新抗原序列也正是在AI技术加持下,云顶新耀突破mRNA序列设计优化、高效递送系统构建等关键技术瓶颈,推动mRNA肿瘤疫苗进入临床阶段。公开资料显示,云顶新耀自主研发的“妙算”系统(EVER-NEO-1)已迭代至第三代。通过深度学习优化mRNA序列设计,将传统18个月的研发周期压缩至数月。其新抗原预测准确率甚至超越国际顶尖机构,在临床前模型中免疫原性捕获率高达79.3%。3路径之辩在支付体系与商业化的双重枷锁下,mRNA企业天然要面对肿瘤治疗的个体化需求与高昂的成本之间的矛盾。个体化和通用型两种策略,便成为商业化博弈下不同的路径体现。个性化定制和通用型设计是目前mRNA肿瘤疫苗开发比较主流的思路。具体而言,个体化肿瘤疫苗针对单个的病人,确定新生抗原后使用mRNA技术进行编码,最后回输到病人体内达到治疗的目的。而个体化肿瘤疫苗制备过程长,且成本过高,所以产生另一种思路,即通用型肿瘤疫苗。个性化新抗原肿瘤mRNA疫苗因精准靶向个体肿瘤特异性抗原,成为精准医学的候选者,但在实际应用中面临新抗原鉴定的复杂性和资源消耗,从而限制其广泛应用。基于此,通用型疫苗开发策略为癌症免疫,提供了一种广泛适用的潜在治疗框架——不仅能够省去冗长的抗原鉴定筛选过程,进一步缩短治疗周期,还有望通过选择临床常见的病原体抗原,惠及更广泛的癌症患者。但是,个体化和通用型二者并不割裂。Pivotal bioVenture管理合伙人柳丹认为,几乎没有企业可以从头完全避开对个体化肿瘤疫苗的探索,只有积累足够多的样本数据才能为通用型肿瘤疫苗做准备,通用型肿瘤疫苗是未来的主流趋势。他从产业逻辑角度分析,个体化肿瘤疫苗因为个体肿瘤抗原免疫特性的区别,潜在市场较为有限,且研发成本过高会影响其商业化后的可及性。通用型肿瘤疫苗潜在市场更为广阔,但在广谱抗原的选择上需要研发者做“数学题”,如何选择药物覆盖的抗原表达。“从个体化走向通用型是趋势,这需要一个过程。”柳丹表示,在这个过程中,现货型肿瘤疫苗或许是个不错的探索,“现货型主要强调的是常规药物的逻辑,患者来了就能打,不需要等待生产时间。通用型一般对应的是个性化,前者是对某群肿瘤类型或者携带某些个突变的患者都可以使用的,后者针对个人定制。” 从理论上讲,现货型肿瘤疫苗靶向多种肿瘤相关抗原,适用范围更广,可以针对多个癌种且适用于不同阶段的癌症患者,而由于批量生产成本也会低很多,甚至可能低于单抗药物,因此颇具竞争力。由于识别肿瘤特异性突变并预测个别HLA等位基因对应新表位的高难度,全球现货型mRNA肿瘤疫苗研发仍处于早期阶段。Moderna、BioNTech等巨头多处于I/II研究阶段,进展缓慢,国产进展也均处于早期阶段。不过,另一方面,这意味着国产企业几乎与海外巨头站在同一起跑线。正如宋相容所言,“follow只会让别人抢占先机,只有自己做First-in-Class、做全球首创,才有机会获得话语权并构建核心竞争优势。市场上尚未出现肿瘤mRNA疫苗,业内共识是,这属于时间问题。在第二届国际生物科技创新与投资大会上,mRNA企业创始人回爱民接受同写意论坛发起人程增江的现场访谈时表示,“整体来说,我觉得有个四五年时间,mRNA肿瘤疫苗会实现上市突破。”— 结语 — 当一把万能钥匙出现时,没人会拒绝它的诱惑。肿瘤mRNA疫苗的研发是一场漫长的马拉松,也是一场接力赛,赛道里奔跑的选手们远没有撞线。在生物医药周期冷热交替中,mRNA企业更应锻造前瞻的战略眼光和强大的执行落地能力,在工具革命与思维跃迁双重共振下,迎接属于自己的春暖花开。
信使RNA财报疫苗免疫疗法细胞疗法
2025-04-16
·药智网
2020年底,美国FDA紧急批准了两种mRNA疫苗(辉瑞/BioNTech联合研发的BNT162b2和Moderna公司的mRNA-1273),为新冠疫情防控提供了革命性工具。这两款疫苗的巨大成功,开启了mRNA技术的新纪元,也促进了mRNA疫苗在肿瘤等更多疾病领域的研发和应用。1mRNA疗法:癌症治疗新希望疫苗是人类在医学领域里最伟大的发明之一,每当一款疫苗被研发出来,就意味着某些疾病将被击败,甚至永久性地从人类生活中消失。而针对癌症的疫苗也被人们寄予了厚望。癌症疫苗是指药物进入机体后,其中的肿瘤相关抗原(tumor-associated antigen,TAA)或肿瘤特异性抗原(tumor-specific antigen,TSA)通过主要组织相容性复合体Ⅰ/Ⅱ提呈作用,激活细胞毒性T淋巴细胞、辅助T细胞等免疫细胞,增强人体免疫系统特异性识别抗原的能力,从而抑制肿瘤的生长、转移。图片来源:参考资料1事实上,癌症疫苗的研究已经历很多阶段,利用许多的技术和方法推动肿瘤疫苗的研发。目前用于肿瘤治疗的疫苗平台有以下四种:全细胞疫苗、多肽疫苗、病毒载体疫苗、DNA/mRNA疫苗。但此前,除了HPV疫苗等少数预防性癌症疫苗,治疗性癌症疫苗发展并不顺利,虽有获批上市,但应用有限。相比较而言,近期崛起的mRNA肿瘤疫苗具有众多优势:①与病毒疫苗类似,mRNA肿瘤疫苗能够同时递送多种抗原,引发体液免疫和细胞免疫,增加了肿瘤细胞根除的可能性。②与多肽疫苗相比,mRNA的分子量更小,并且mRNA疫苗可以将多种抗原同时编码进mRNA序列当中,并在细胞内翻译产生大量相关抗原。③与DNA疫苗相比,mRNA疫苗是转录后的产物,是一条单链,不需要在细胞核中再进行转录,可以直接利用细胞中的原料,提高抗原产生效率,同时也避免外来信息整合进入宿主的DNA中。④开发快速且灵活性高。mRNA疫苗的设计和生产过程相对简单,能够快速响应肿瘤抗原的变化。mRNA疫苗可以根据不同患者的肿瘤抗原进行快速设计和合成,具有个性化治疗的潜力。⑤与其他疗法的协同作用。mRNA疫苗可以与免疫检查点抑制剂(如PD-1/PD-L1抑制剂)、化疗和放疗等传统疗法联合使用,进一步增强抗肿瘤效果。mRNA肿瘤疫苗具有的这些优势,使其成为未来肿瘤免疫治疗的重要方向之一。2首个上市在即药智数据显示,目前全球已有数十个mRNA肿瘤疫苗正在开发中,虽无上市产品,但Moderna与默沙东联合开发的mRNA-4157已进入临床3期,预计将在2027年上市,有望成为首款上市的mRNA肿瘤疫苗。此外,德国生物技术公司BioNTech、国内瑞宏迪医药、云顶新耀、康方生物、思路迪医药等公司也有mRNA肿瘤疫苗管线在研。表1 全球在研mRNA肿瘤疫苗管线(部分)数据来源:药智数据Moderna和BioNTech两家生物技术公司在领跑mRNA新冠疫苗之后,继续领跑mRNA肿瘤疫苗。mRNA-4157是Moderna公司开发的一款个体化mRNA肿瘤疫苗,其抗原为包含编码最多34种新抗原的单一合成mRNA分子,佐剂为脂质纳米颗粒(lipid nanoparticle,LNP)。该药目前已启动三项Ⅲ期研究,分别为一项针对黑色素瘤和两项针对非小细胞肺癌的研究。图片来源:Moderna公司在2024年ASCO年会上,Moderna公布了mRNA-4157联合Keytruda(帕博利珠单抗,pembrolizumab)治疗已切除黑色素瘤的Ⅱb期临床试验3年随访数据。结果显示,中位随访时间约34.9个月,与单独使用帕博利珠单抗相比,mRNA-4157与帕博利珠单抗联用可使黑色素瘤患者复发和死亡风险降低49%,远处转移的风险降低了62%。且与单独使用帕博利珠单抗相比,mRNA-4157联合帕博利珠单抗的总生存(overall survival,OS)时间的探索性终点更有利,2.5年OS率分别为96.0%和90.2%,其RFS时间显著延长,RFS率提高了19.2%。值得一提的是,此前Moderna与默沙东就mRNA-4157已达成协议,共同开发和商业化mRNA-4157。Moderna预计2026年可能会公布mRNA-4157的关键数据,并有望拿下首款基于mRNA的个性化癌症疫苗。除了mRNA-4157,Moderna公司的mRNA-4359也已进入临床Ⅱ期。BioNTech公司则开发了两个mRNA癌症疫苗技术平台:个体化新抗原特异性免疫治疗平台iNeST和针对特定适应症的“现货”mRNA癌症疫苗平台FixVac。图片来源:BioNTech公司基于iNeST技术,BioNTech开发了BNT122(autogene cevumeran)。这是一种针对多种实体瘤的个体化癌症候选疫苗,编码多达20种患者特异性肿瘤新抗原,诱导针对患者个体肿瘤的免疫反应。其治疗胰腺癌的I期临床研究显示,50%(8/16)的患者检测显示诱导出新抗原特异性T细胞。在中位随访时间为18个月时,获得新抗原特异性免疫反应患者的无复发生存期(RFS)显著长于无疫苗激发免疫反应的患者。BNT122目前正在各种实体瘤适应症中进行评估,包括肌层浸润性尿路上皮癌、结直肠癌、胰腺导管腺癌、黑色素瘤等。基于FixVac技术,BioNTech开发了BNT111、BNT113、BNT116三款癌症疫苗,分别针对黑色素瘤、头颈鳞状细胞癌和非小细胞肺癌,目前皆已进入临床研究阶段。3国内多家Biotech已布局目前国内mRNA肿瘤疫苗也已有多个产品处于临床及临床前研究阶段,如云顶新耀的EVM16、上海瑞宏迪医药的HRXG-K-1939、成都威斯津生物的WGc-043、北京臻知医学的IPM514、合肥阿法纳生物的AFN18等。EVM16是云顶新耀通过AI辅助研发的首款新型mRNA个性化肿瘤治疗性疫苗。临床前研究显示,EVM16在小鼠模型中显著抑制了肿瘤生长,同时展现出良好的安全性。而且EVM16与PD-1抗体联用后具有协同抗肿瘤效果。目前该药已在北京大学肿瘤医院顺利完成首例患者给药。另外,云顶新耀的通用型的现货肿瘤治疗性疫苗EVM14也已成功获得美国FDA IND批准,拟用于非小细胞肺癌、头颈癌等多种癌症的治疗。HRXG-K-1939是上海瑞宏迪医药自主研发的个性化新抗原mRNA肿瘤疫苗,已在复旦大学附属肿瘤医院和中国人民解放军总医院分别开展实体瘤和胰腺癌的IIT研究。WGc-043是成都威斯津生物研发的一款EB病毒阳性肿瘤mRNA疫苗,已先后获得美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)IND许可,获准在两地开展临床试验,这也是全球首款针对EB病毒相关肿瘤获得IND批件的治疗性mRNA肿瘤疫苗。IPM514是北京臻知医学研发的一种基于mRNA-LNP的现货通用型肿瘤治疗性疫苗候选药物,可通过肌肉注射递送一套经优化设计编码近20个食管鳞癌(ESCC)肿瘤相关抗原表位序列的纳米脂质体药物。目前一项开放、多中心、评估IPM514治疗食管鳞状细胞癌的安全性、耐受性、药代动力学和初步有效性的临床研究正在开展中。AFN18是合肥阿法纳生物开发的一款个体化肿瘤新生抗原mRNA疫苗,已在肿瘤癌前病变和实体瘤两大领域分别获得国家药监局的两项临床批件。此外,康方生物于近期注册了个体化mRNA疫苗单药或联合PD-1/CTLA-4双抗、PD-1/VEGF双抗辅助治疗胰腺癌的IIT临床试验。思路迪医药基于mRNA-LNP平台开发的首个mRNA肿瘤疫苗3D124计划在今年向FDA及CDE递交IND申请。4结语近年来,mRNA肿瘤疫苗在癌症治疗领域方面展现出巨大潜力,并取得了显著进展,但仍然面临递送、免疫反应调控、规模化生产等许多挑战,距离全面用于临床治疗仍需大量研究和系统性验证。不过,随着基础研究的深入和相关技术的进步,mRNA肿瘤疗法有望在未来几年取得更多突破,成为下一个肿瘤治疗爆发领域。参考资料:1.https://link-cnki-net.libproxy1.nus.edu.sg/urlid/11.1784.N.20240402.1658.0282.DOI:10.3969/j.issn.1672-4992.2024.09.0293.DOI:10.12206/j.issn.2097-2024.2024100344.医药领袖:后疫情时代BioNTech生存法则:进军mRNA癌症疫苗5.阿法纳生物:阿法纳生物个体化肿瘤mRNA疫苗临床研究启动会顺利召开6.医药笔记:康方生物:个体化mRNA疫苗启动胰腺癌IIT临床研究7.云顶新耀:云顶新耀宣布通用型的现货肿瘤治疗性疫苗EVM14注射液的新药临床试验申请获美国FDA批准权威榜单定义行业标杆,赋能企业品牌价值!识别二维码,解锁年度惊喜!声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智网立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请联系maxuelian@yaozh.com。责任编辑 | 小月石合作、投稿、转载开白 | 马老师 18323856316(同微信) 阅读原文,是受欢迎的文章哦
信使RNA疫苗临床3期免疫疗法上市批准
100 项与 成都威斯克生物医药有限公司 相关的药物交易
登录后查看更多信息
100 项与 成都威斯克生物医药有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年08月21日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
9
34
临床前
临床申请
3
1
临床申请批准
临床1期
3
3
临床2期
临床3期
4
1
申请上市
批准上市
1
8
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
重组变异新型冠状病毒疫苗(Sf9细胞) ( SARS-CoV-2 S protein ) | 新型冠状病毒感染 更多 | 批准上市 |
WSK-V101 ( SARS-CoV-2 S protein ) | - | 申请上市 |
重组三价新冠病毒三聚体蛋白疫苗 (Sf9细胞) ( SARS-CoV-2 S protein ) | 新型冠状病毒感染 更多 | 临床3期 |
WSK-IM02 | - | 临床3期 |
WSK-V102 | - | 临床3期 |
登录后查看更多信息
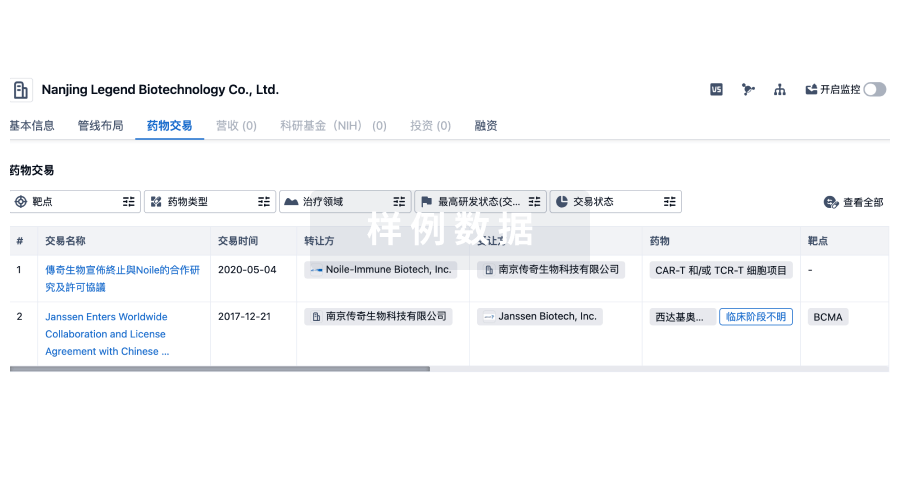
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
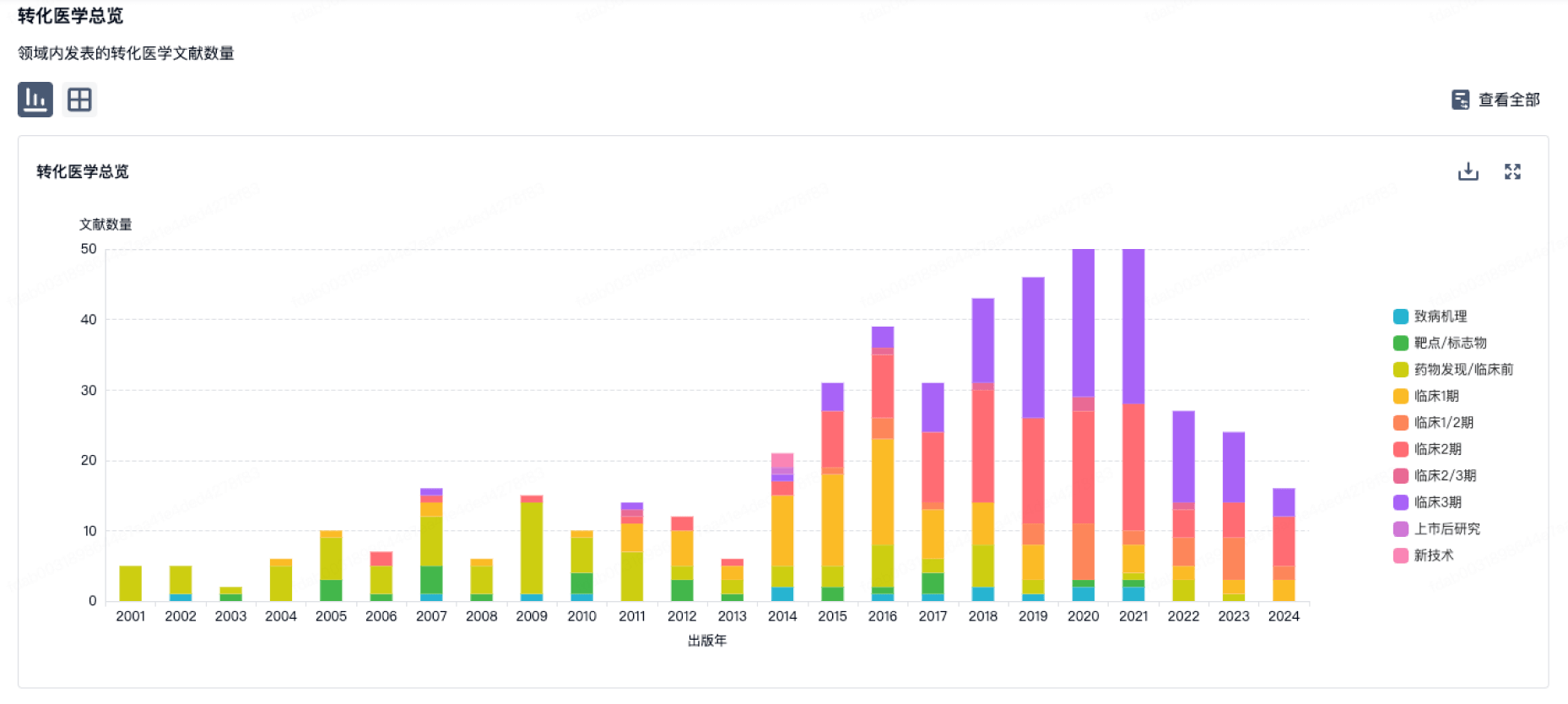
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
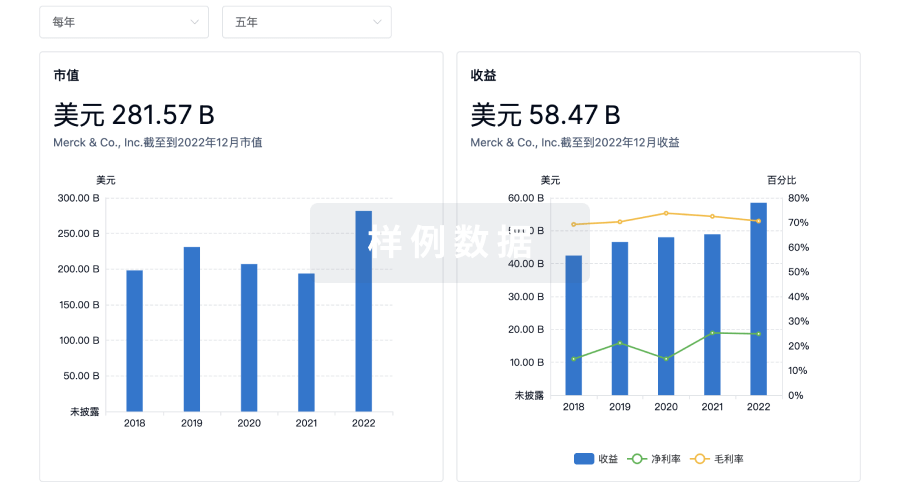
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
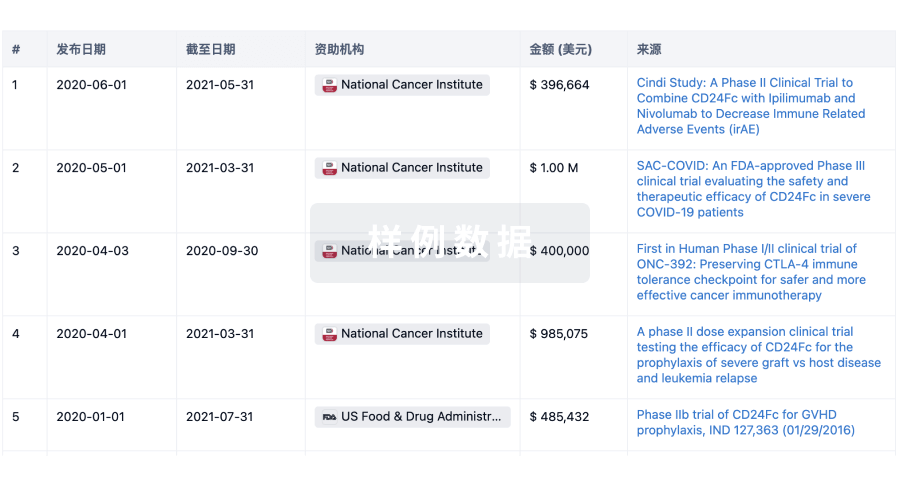
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
