预约演示
更新于:2025-08-29

Beijing Zhitai Biomedical Technology Co., Ltd.
更新于:2025-08-29
概览
标签
内分泌与代谢疾病
消化系统疾病
神经系统疾病
重组多肽
合成多肽
生物类似药
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 重组多肽 | 2 |
| 融合蛋白 | 2 |
| 重组蛋白 | 1 |
| 合成多肽 | 1 |
| 生物类似药 | 1 |
| 排名前五的靶点 | 数量 |
|---|---|
| GLP-1R(胰高血糖素样肽-1受体) | 3 |
| FGF21R x GLP-1R | 1 |
| GDF15 x GLP-1R | 1 |
关联
6
项与 北京质肽生物医药科技有限公司 相关的药物靶点 |
作用机制 GLP-1R激动剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床2期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 GLP-1R调节剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
作用机制 FGF21R激动剂 [+1] |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床申请批准 |
首次获批国家/地区- |
首次获批日期- |
11
项与 北京质肽生物医药科技有限公司 相关的临床试验NCT07020884
A Randomized, Double-Blind, Placebo-Controlled Phase II Clinical Study to Evaluate the Efficacy, Safety, and Pharmacokinetic Characteristics of ZT002 Injection in Subjects With Overweight or Obesity
This study will evaluate the percentage change from baseline in weight after 24 weeks of treatment with ZT002 Injection in subjects with overweight/obesity.
开始日期2024-08-14 |
申办/合作机构 |
CTR20240709
在二甲双胍治疗后血糖控制不佳的2型糖尿病患者中比较 ZT001注射液与诺和泰®皮下注射治疗的疗效和安全性:一项多中心、随机、开放、平行对照Ⅲ期临床试验
主要目的:评价ZT001注射液与诺和泰®在二甲双胍治疗后血糖控制不佳的T2DM患者中皮下注射治疗的疗效。次要目的:以诺和泰®为对照,评价ZT001注射液在二甲双胍治疗后血糖控制不佳的T2DM患者中皮下注射治疗的安全性;评价ZT001注射液在成年T2DM患者中的群体药代动力学(PopPK);评价ZT001注射液在成年T2DM患者中的免疫原性。
开始日期2024-07-18 |
申办/合作机构 |
NCT07065032
A Single-center, Randomized, Double-blind, Placebo-controlled, Multiple-ascending-dose Phase Id/IIa Study Evaluating the Safety, Tolerability, and Pharmacokinetics of ZT002 Injection in Adult Chinese Subjects With Type 2 Diabetes Mellitus (T2DM)
This study will comprise a randomized, double blind, placebo controlled, multiple ascending dose, safety, tolerability and pharmacokinetic study of ZT002 in subjects with type 2 diabetes mellitus (T2DM).
开始日期2024-02-19 |
申办/合作机构 |
100 项与 北京质肽生物医药科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 北京质肽生物医药科技有限公司 相关的专利(医药)
登录后查看更多信息
84
项与 北京质肽生物医药科技有限公司 相关的新闻(医药)2025-08-22
·创鉴汇
近日,南京安吉生物宣布达成三款多肽新药(涵盖眼科与抗肿瘤治疗领域)的对外授权合作,协议结构中包括75万美元前期付款与525万美元首付款,高达4.53亿美元的潜在交易总额,再度印证了中国肽类创新药公司正在通过“License‑out”模式获得认可。
与此同时,2025年以来,中国肽类创新药领域投融资活跃,公开资料显示至少发生20起融资事件,融资总额突破120亿元人民币,其中12起属于亿元级及以上,涵盖Pre‑A至IPO多个阶段。充分说明资本不仅关注早期创新研发,也认可成熟公司商业化进展与预期获益。地域分布上,江苏、上海与广东是肽类创新药公司与资本活跃集中的主要区域,依托本地研发平台、产业生态和资本支持,这些区域公司在融资表现上尤为突出。总体而言,肽类创新药正成为创新药研发的重要赛道,未来有望在肿瘤、眼科、代谢疾病(如GLP‑1类适应症拓展)等方向实现更多突破。
*本文肽类创新药公司泛指研发管线包含肽类药物的公司。
维昇药业:内分泌疾病药物研发公司
3月21日,维昇药业在港交所IPO,募资约6.72亿港元。
维昇药业成立于2018年11月,是一家处于研发后期、产品接近商业化的生物医药公司,专注于在中国为患者提供特定内分泌疾病的治疗方案。该公司目前拥有一款核心产品及两款其他在研候选药物,核心产品每周一次的长效生长激素隆培促生长素已经于2024年3月向中国国家药监局(NMPA)递交上市申请。
隆培促生长素(lonapegsomatropin)是一款每周一次的长效生长激素替代疗法,用于治疗儿童生长激素缺乏症(一种生长激素不足导致的18岁以下患者中常见的矮小症)。此外,关键候选药物之一那韦培肽(navepegritide)是一款C型利钠肽的长效前药,每周一次给药,拟开发用于治疗2至10岁软骨发育不全(一种短肢型矮小症,可导致严重的骨骼并发症及合并症)。另一款关键候选药物帕罗培特立帕肽(palopegteriparatide)是一款每日一次的甲状旁腺激素替代疗法,拟开发用于治疗慢性甲状旁腺功能减退症(一种由甲状旁腺激素分泌减少或功能缺陷所引起的钙磷代谢异常综合症)。
派格生物:慢病新药研发生物技术公司
5月27日,派格生物(Pegbio)完成约2.32亿港元IPO融资。该公司成立于2008年,专注于自主研究及开发慢性病创新疗法,重点关注内分泌代谢领域。通过自主开发的HECTORTM技术平台设计和筛选具有新靶标、新位点、新机制的分子实体。
派格生物聚焦糖尿病、肥胖等代谢疾病,建立了多肽药物、蛋白质药物及小分子药物为主的研发管线体系。其核心产品PB-119为自主开发、接近商业化阶段的长效胰高血糖素样肽-1(GLP-1)受体激动剂。PB-119主要用于二型糖尿病(T2DM)及肥胖症一线治疗。凭借聚乙二醇化技术,可实现一周一次给药。PB-119在中国用于治疗T2DM的新药上市申请(NDA)于2023年9月获药监局受理。派格生物预计于2025年获得NDA批准并在中国商业化推出用于治疗T2DM的PB119。
麦科奥特:多肽药物研发公司
7月3日,麦科奥特宣布完成超亿元D轮融资交割。所募集资金将重点用于推动核心管线研发、制剂产业化基地建设等方面,进一步提升麦科奥特在多肽创新药领域的研发能力。
麦科奥特于2007年成立,专注于双功能和多功能特异性多肽药物研发,聚焦于心脑血管、代谢类疾病领域。新闻稿介绍,该公司已有7个创新药管线进入临床研发,包括1个临床3期阶段,3个临床2期阶段和3个临床1期阶段。根据官网,该公司进展较快的MT1013为双功能双靶点多肽药物,其双特异性靶标可以:抑制甲状旁腺激素(PTH)分泌;成骨生长肽作用于成骨细胞,骨髓间充质干细胞,肾小管上皮细胞,肠道细胞:改善骨皮质骨质疏松,治疗肾性骨病;促进钙吸收,调节血钙,防治低钙血症。拟用于治疗继发性甲状旁腺功能亢进、慢性肾病合并甲状旁腺功能亢进性骨质疏松症。
质肽生物:蛋白质药物开发公司
2月17日消息,质肽生物获亿元融资。质肽生物成立于2018年9月,专注用大肠杆菌生产重组蛋白质药物,致力于开发治疗慢性代谢性疾病(如糖尿病、肥胖、非酒精性脂肪性肝炎等)创新生物药。
目前质肽生物管线中有10个在研重组蛋白创新药和生物类似物品种,包括司美格鲁肽注射液生物类似药ZT001,以及有望实现仅需每月注射1次的新型超长效GLP-1R激动剂ZT002等,口服GLP-1类多肽药物ZT006片等。2024年11月,ZT006片获得临床试验默示许可,拟开发用于成人2型糖尿病患者的血糖控制。ZT006是新一代口服蛋白药品种,主要治疗糖尿病和肥胖症。经过优化的ZT006具有较高的生物利用度,有希望成为继口服司美格鲁肽之后的新一代口服GLP-1品种。口服给药是公认的、可以显著提高慢性病患者依从性的一种给药方式。
星联肽:蛋白偶联药物研发公司
1月16日,星联肽宣布完成1亿元Pre-A+轮融资,本轮融资将为星联肽的产品研发提供重要资金支持,以推进核心产品的临床试验和新产品开发,加速创新性XDC药物的临床转化。
星联肽聚焦于小型化偶联药物的研发,包括多肽偶联药物(PDC)和纳米抗体偶联药物(NDC)等。该公司目前已有两款产品处于临床开发阶段,首款产品SC-101(靶向Nectin-4的PDC)分别于2024年初和年中获得中国NMPA和美国FDA的临床默示许可,目前处于1期临床阶段,已初步显示出抗肿瘤效果及良好的安全性。星联肽的第二款产品SC-102(靶向EphA2的PDC)在2024年底进入临床阶段,已完成首例受试者的入组和给药工作。此外,星联肽研发的首个NDC项目有望在今年完成PCC提名。
读者们请星标⭐创鉴汇,第一时间收到推送
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「创鉴汇」微信公众号留言联系我们。
更多数据内容推荐
点击“在看”,分享创鉴汇健康新动态
IPO引进/卖出
2025-06-30
·药时空
近期,北京质肽生物医药科技有限公司自主研发的创新性GLP-1/FGF21双重激动剂-ZT003注射液,正式获得美国食品药品监督管理局(FDA)新药临床试验批准,其适应症为代谢功能障碍相关脂肪性肝炎(MASH)的治疗,ZT003即将在国外开展I期临床试验。摩熵医药数据ZT003是一种新型的单分子GLP-1/FGF21双激动融合蛋白。临床试验结果已显示GLP-1受体激动剂可以显著缓解MASH患者代谢功能障碍,促进体重减轻,显示出在肝脏脂肪、炎症和纤维化方面的改善;FGF21可通过不同机制降低MASH患者肝脏甘油三酯和胆固醇水平,增强肝脏交感神经活动,减少肝脏新生脂肪生成和纤维化,在临床试验中已显示出逆转MASH肝硬化患者纤维化的巨大潜力。ZT003独特的分子设计,实现了GLP-1和FGF21双靶点的协同与互补效应(如图),在临床前MASH动物模型中展现出显著的改善肝脏脂肪、炎症和纤维化水平的能力,有望成为MASH治疗领域最具潜力的疗法。GLP-1/FGF21双靶点协同互补治疗MASH机制示意图参考资料:药融圈info,质肽生物。识别微信二维码,可添加药时空小编请注明:姓名+研究方向!
临床1期
2025-06-25
·创鉴汇
内分泌与代谢疾病因患者基数庞大且临床需求持续增长,成为创新药研发的重要方向。据公开数据统计,2025年至今,该领域至少发生25起创新药公司融资事件,已披露融资总额超125亿元。融资覆盖糖尿病、肥胖、高脂血症等疾病,涉及小分子药物、多肽、蛋白质药物及细胞疗法等技术路径。从IPO公司到新锐技术平台,资本正加速涌入这一充满潜力的治疗领域。融资亮点聚焦多肽与蛋白质药物主导代谢性疾病疗法创新:近半数获融资公司重点布局多肽与蛋白质药物。如维昇药业推进甲状旁腺功能减退症多肽疗法,派格生物开发GLP-1类多肽药物治疗肥胖,质肽生物则聚焦长效重组蛋白治疗糖尿病。此类药物因靶向性强、半衰期可控,在代谢调节领域临床优势显著。干细胞疗法剑指糖尿病治疗瓶颈:至少4家公司聚焦干细胞疗法治疗糖尿病及其并发症。星赛瑞真开发多能干细胞(iPSC)衍生胰岛细胞疗法CRG-002动物试验结果积极;睿健医药开发iPSC来源眼科通用型细胞治疗产品,有潜力拓展至糖尿病性视网膜病变等与代谢疾病相关的视网膜病变;中盛溯源则推进iPSC来源肾脏修复细胞产品治疗糖尿病肾病等。该领域融资集中于B+轮及以前,反映资本正加速早期技术转化。AI、新分子实体创新技术引领大额融资:11家公司获得亿元及以上融资。其中,英矽智能凭借其端到端AI平台,推动包括代谢紊乱和肥胖在内的管线进展,获得1.23亿美元E轮融资。达歌生物利用其独特的GlueXplorer分子胶平台开发新型蛋白降解疗法,珂阑医药聚焦胆固醇代谢新靶点,均获得亿元以上融资,体现了源头创新技术平台的高认可度。维昇药业:内分泌疾病药物研发公司3月21日,维昇药业在港交所IPO,募资约6.72亿港元。维昇药业成立于2018年11月,是一家处于研发后期、产品接近商业化的生物医药公司,专注于在中国为患者提供特定内分泌疾病的治疗方案。该公司目前拥有一款核心产品及两款其他在研候选药物,核心产品每周一次的长效生长激素隆培促生长素已经于2024年3月向中国国家药监局(NMPA)递交上市申请。隆培促生长素(lonapegsomatropin)是一款每周一次的长效生长激素替代疗法,用于治疗儿童生长激素缺乏症(PGHD,一种生长激素不足导致的18岁以下患者中常见的矮小症)。与每日一次人生长激素相比,隆培促生长素提供了方便的给药方案,注射频率为每周一次,这可能会提高儿童患者在日常生活中给药的依从性。此外,该公司研发管线中:那韦培肽(navepegritide)是一款C型利钠肽的长效前药,每周一次给药,拟开发用于治疗2至10岁软骨发育不全。帕罗培特立帕肽(palopegteriparatide)是一款每日一次的甲状旁腺激素替代疗法,拟开发用于治疗慢性甲状旁腺功能减退症。派格生物:慢病新药研发生物技术公司5月27日,派格生物(Pegbio)完成约2.32亿港元IPO融资。该公司成立于2008年,专注于自主研究及开发慢性病创新疗法,重点关注内分泌代谢领域。通过自主开发的HECTORTM技术平台设计和筛选具有新靶标、新位点、新机制的分子实体。派格生物聚焦糖尿病、肥胖等代谢疾病,建立了多肽药物、蛋白质药物及小分子药物为主的研发管线体系。其核心产品PB-119为自主开发、接近商业化阶段的长效胰高血糖素样肽-1(GLP-1)受体激动剂。PB-119主要用于二型糖尿病(T2DM)及肥胖症一线治疗。凭借聚乙二醇化技术,可实现一周一次给药。PB-119在中国用于治疗T2DM的新药上市申请(NDA)于2023年9月获药监局受理。派格生物预计于2025年获得NDA批准并在中国商业化推出用于治疗T2DM的PB119。珂阑医药:胆固醇代谢创新药研发公司2月21日消息,珂阑医药完成超亿元人民币A+轮融资。此次融资资金将主要用于加速推进多个核心管线进入临床申报和开发,以及研发平台和团队的拓展。珂阑医药立足于糖脂代谢领域的前沿科研,聚焦胆固醇代谢通路中成药性高的创新性靶点,开展针对代谢性疾病(高脂血症、肥胖症、糖尿病、动脉粥样硬化症以及MASH)等重大疾病的创新药研发工作。原研项目转化来自宋保亮院士实验室,致力于“健康代谢,健康心血管,健康生活”的理念,力争为代谢疾病患者治疗提供可选方案。针对代谢性疾病和肿瘤,珂阑医药整合了新药研发中基于靶标调控机理的报告基因筛选系统,蛋白质小分子互作系统、基于靶标功能的体外药效测试系统,构建生化与细胞测试自主研发平台,全方位进行药物优化,高效推动药物研发深入与开展。质肽生物:蛋白质药物开发公司2月17日消息,质肽生物获亿元融资。质肽生物成立于2018年9月,专注用大肠杆菌生产重组蛋白质药物,致力于开发治疗慢性代谢性疾病(如糖尿病、肥胖、非酒精性脂肪性肝炎等)创新生物药。目前质肽生物管线中有10个在研重组蛋白创新药和生物类似物品种,包括司美格鲁肽注射液生物类似药ZT001,以及有望实现仅需每月注射1次的新型超长效GLP-1R激动剂ZT002等,口服GLP-1类多肽药物ZT006片等。2024年11月,ZT006片获得临床试验默示许可,拟开发用于成人2型糖尿病患者的血糖控制。ZT006是新一代口服蛋白药品种,主要治疗糖尿病和肥胖症。经过优化的ZT006具有较高的生物利用度,有希望成为继口服司美格鲁肽之后的新一代口服GLP-1品种。口服给药是公认的、可以显著提高慢性病患者依从性的一种给药方式。星赛瑞真:干细胞疗法研发公司3月17日,星赛瑞真宣布完成近亿元人民币天使+轮融资。这是星赛瑞真自2024年6月获得复健资本及创瑞投资的天使轮投资以来,在半年时间内再次获得天使轮老股东的追加投资。本次融资资金将用于推进具有差异化的iPSC衍生的胰岛细胞管线(CRG-002)和iPSC衍生的角膜内皮细胞产品(CRG-101)进入临床研究阶段,以及用于公司其它早研管线的研发布局。星赛瑞真成立于2022年,聚焦细胞治疗和再生医学转化,构建了iPSC快速重编程技术、基于CRISPR/Cas12b的iPSC基因编辑平台以及生物信息学指导下的不同胚层分化技术平台。在代谢疾病领域,星赛瑞真主要开发胰岛替代疗法用于1型糖尿病治疗。其在研管线CRG-002管线为iPSC衍生胰岛细胞,已经动物试验验证,有望满足糖尿病患者巨大临床需求。读者们请星标⭐创鉴汇,第一时间收到推送免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「创鉴汇」微信公众号留言联系我们。更多数据内容推荐点击“在看”,分享创鉴汇健康新动态
IPO细胞疗法
100 项与 北京质肽生物医药科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 北京质肽生物医药科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年09月03日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床前
2
1
临床申请批准
临床1期
1
1
临床2期
临床3期
1
2
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
司美格鲁肽生物类似药 (质肽生物) ( GLP-1R ) | 肥胖 更多 | 临床3期 |
佐维格鲁肽 ( GLP-1R ) | 阿尔茨海默症 更多 | 临床1期 |
ZT-006 ( GLP-1R ) | 肥胖 更多 | 临床1期 |
ZT-003 ( FGF21R x GLP-1R ) | 非酒精性脂肪性肝炎 更多 | 临床申请批准 |
RP-005 | 糖尿病 更多 | 临床前 |
登录后查看更多信息
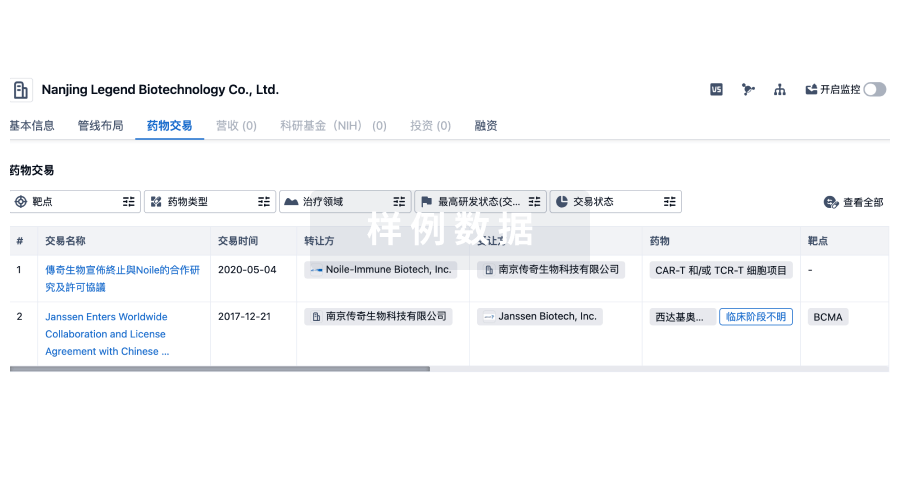
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
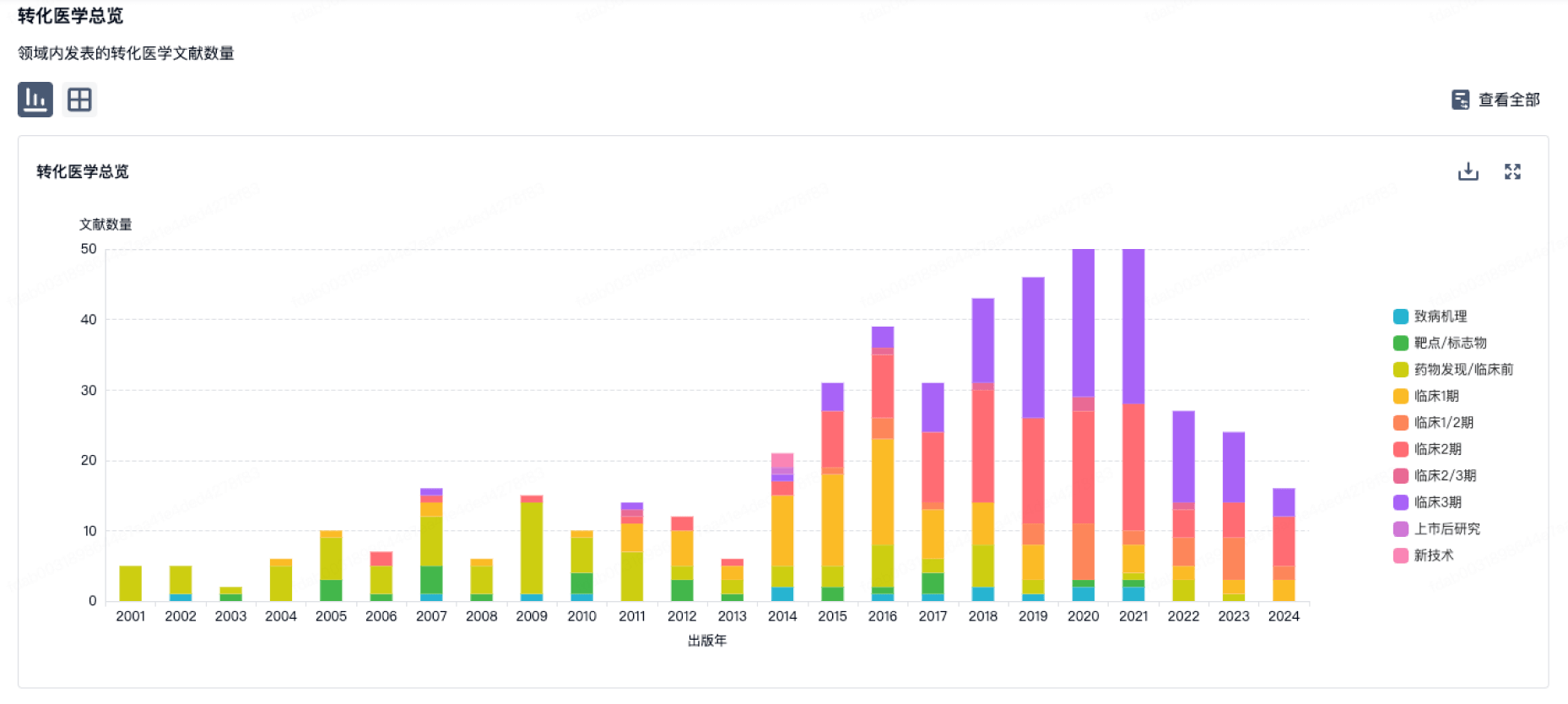
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
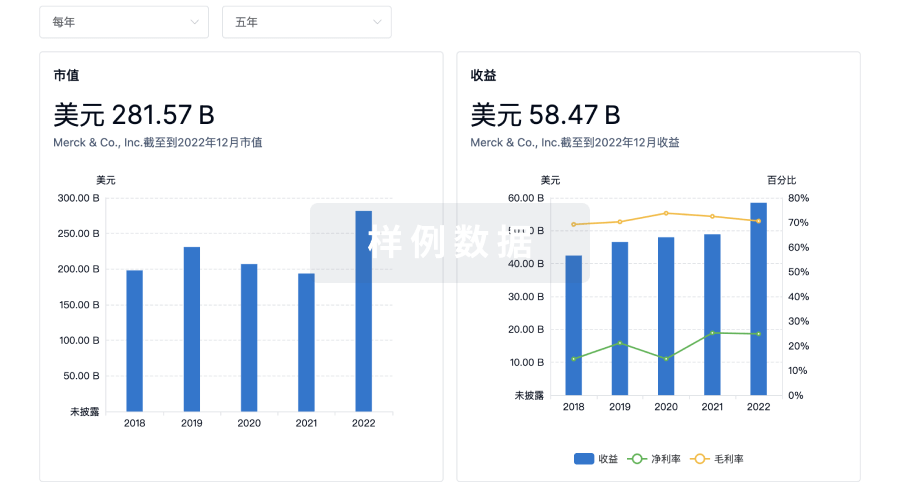
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
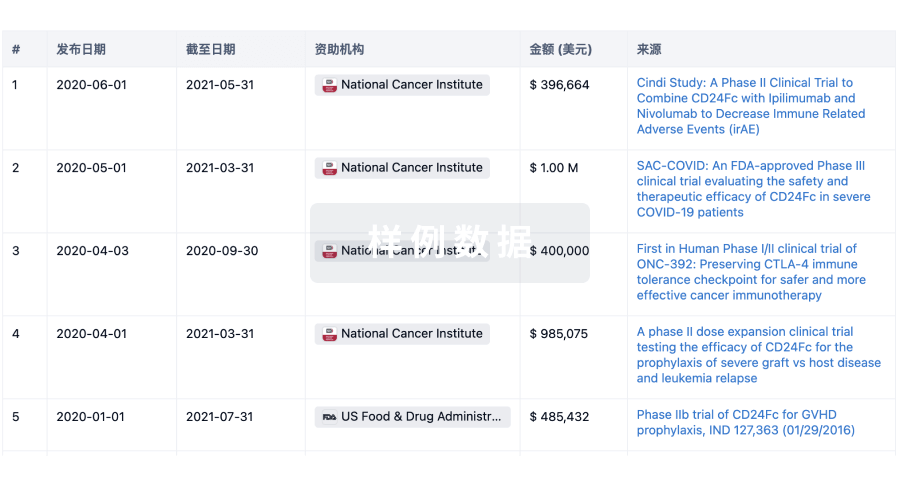
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
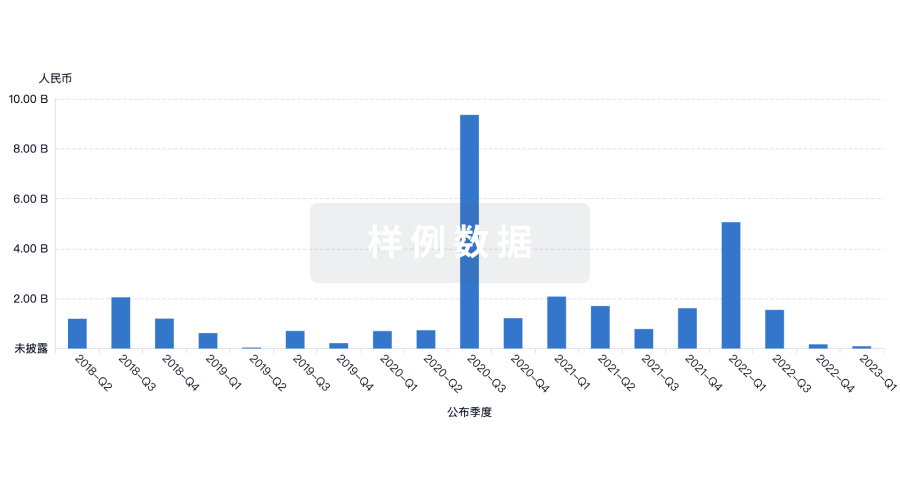
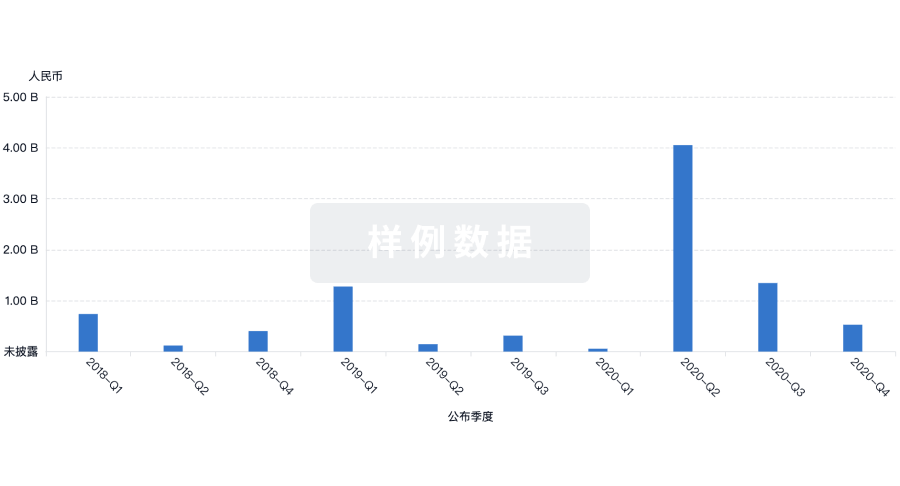
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用