《科学·转化医学》:最毒乳腺癌“黑化”未成熟自然杀伤细胞!
2023-04-03
免疫疗法细胞疗法
三阴性乳腺癌(TNBC)占所有乳腺癌的10-15%,是侵袭性最强的亚型之一,特征为缺乏雌激素和孕激素受体(ER/PR)以及人表皮生长因子受体(HER2)[1-2]。
好消息是,清除NK细胞或阻断Wnt信号通路与免疫治疗等方法联合,可以改善患者预后。这一研究结果发表在Science Translational Medicine上[10]。

Preview
来源: 生物谷
文章封面
视频号" role="option">
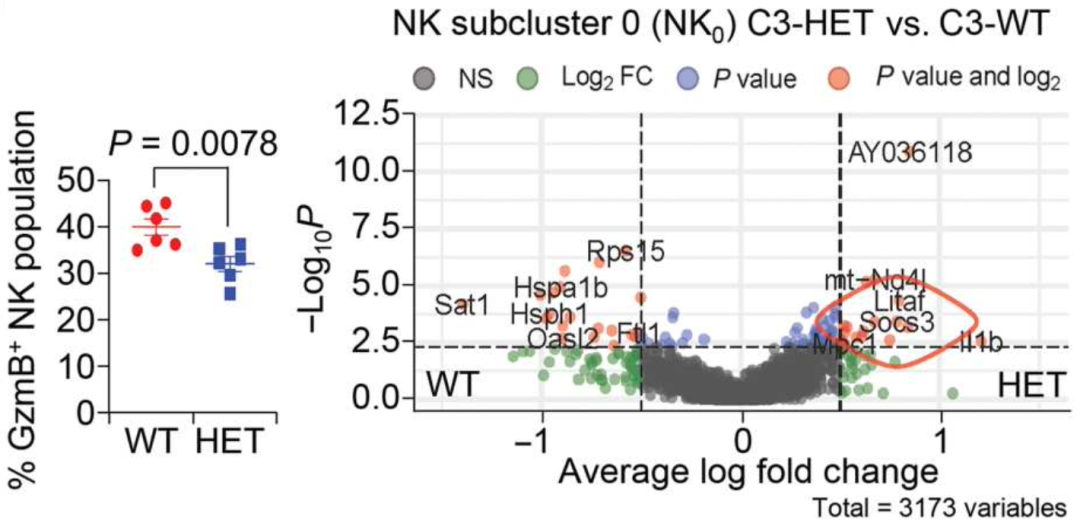
Preview
来源: 生物谷
这些结果表明,在TNBC的TME中未成熟NK细胞增加,并且可能与肿瘤转移和血管生成的增加有关。
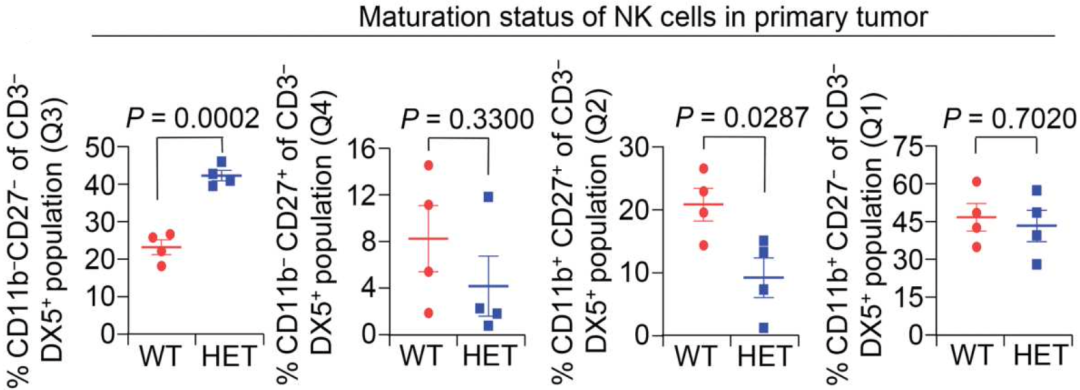
Preview
来源: 生物谷
C3-HET原发肿瘤C3-HET原发肿瘤中未成熟CD11b-CD27-NK细胞数量增加
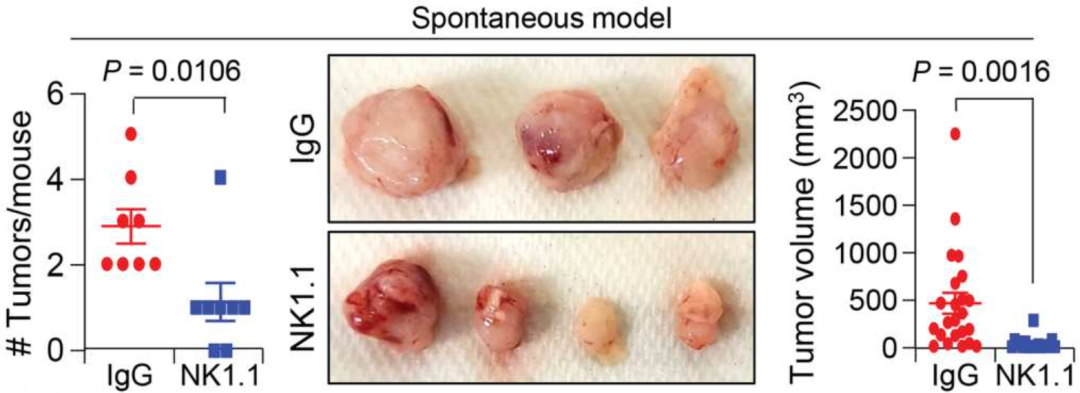
Preview
来源: 生物谷
清除NK细胞可以减少肿瘤生长、进展和转移
研究团队还将C3-HET浸润NK细胞与TNBC和非TNBC细胞系进行了共培养。与来自脾脏的活化NK细胞相比,C3-HET肿瘤浸润NK细胞的杀伤作用降低(P<0.0001)。后续实验进一步证明,TNBC肿瘤浸润NK细胞能够增加TNBC肿瘤细胞干细胞特性。
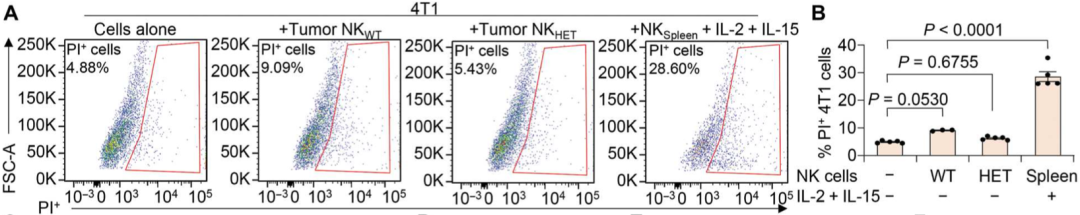
Preview
来源: 生物谷
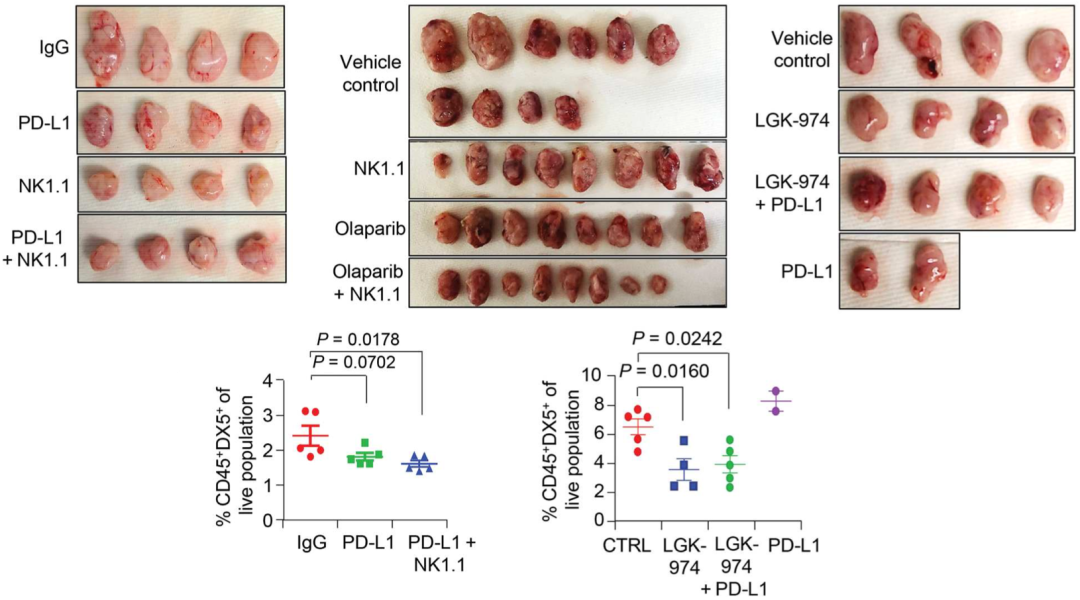
此外,清除NK细胞还可以提高荷瘤小鼠对PARP抑制剂奥拉帕利PARP抑制剂奥拉帕利的反应性。阻断Wnt信号通路也可以增强免疫治疗或化疗在TNBC肿瘤中的效果。
Preview
来源: 生物谷
清除NK细胞或阻断Wnt信号通路可以增强免疫治疗或化疗的效果
最后,研究团队在人类数据库中对研究结果进行了验证。TNBC患者TME中NK细胞的数量增加,主要为未成熟NK细胞,该亚群细胞增加与TNBC患者的不良临床结局相关。
参考文献
[1] Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin. 2020;70(1):7-30. doi:10.3322/caac.21590
[2] Garrido-Castro AC, Lin NU, Polyak K. Insights into Molecular Classifications of Triple-Negative Breast Cancer: Improving Patient Selection for Treatment. Cancer Discov. 2019;9(2):176-198. doi:10.1158/2159-8290.CD-18-1177
[3] Lehmann BD, Bauer JA, Chen X, et al. Identification of human triple-negative breast cancer subtypes and preclinical models for selection of targeted therapies. J Clin Invest. 2011;121(7):2750-2767. doi:10.1172/JCI45014
[4] Deepak KGK, Vempati R, Nagaraju GP, et al. Tumor microenvironment: Challenges and opportunities in targeting metastasis of triple negative breast cancer. Pharmacol Res. 2020;153:104683. doi:10.1016/j.phrs.2020.104683
[5] Villegas FR, Coca S, Villarrubia VG, et al. Prognostic significance of tumor infiltrating natural killer cells subset CD57 in patients with squamous cell lung cancer. Lung Cancer. 2002;35(1):23-28. doi:10.1016/s0169-5002(01)00292-6
[6] Ishigami S, Natsugoe S, Tokuda K, et al. Prognostic value of intratumoral natural killer cells in gastric carcinoma. Cancer. 2000;88(3):577-583.
[7] Coca S, Perez-Piqueras J, Martinez D, et al. The prognostic significance of intratumoral natural killer cells in patients with colorectal carcinoma. Cancer. 1997;79(12):2320-2328. doi:10.1002/(sici)1097-0142(19970615)79:123.0.co;2-p
[8] Marcenaro E, Notarangelo LD, Orange JS, Vivier E. Editorial: NK Cell Subsets in Health and Disease: New Developments. Front Immunol. 2017;8:1363. Published 2017 Oct 18. doi:10.3389/fimmu.2017.01363
[9] Hanna J, Mandelboim O. When killers become helpers. Trends Immunol. 2007;28(5):201-206. doi:10.1016/j.it.2007.03.005
[10] Thacker G, Henry S, Nandi A, et al. Immature natural killer cells promote progression of triple-negative breast cancer. Sci Transl Med. 2023;15(686):eabl4414. doi:10.1126/scitranslmed.abl4414
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
-来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


