更新于:2024-06-19
COVID-19 vaccine (Maxhealth Biotechnology)
新冠疫苗 (迈科康生物)
更新于:2024-06-19
概要
基本信息
原研机构  成都迈科康生物科技有限公司初创企业 成都迈科康生物科技有限公司初创企业 |
在研机构- |
非在研机构  成都迈科康生物科技有限公司初创企业 成都迈科康生物科技有限公司初创企业 |
最高研发阶段终止临床前 |
首次获批日期- |
最高研发阶段(中国)终止 |
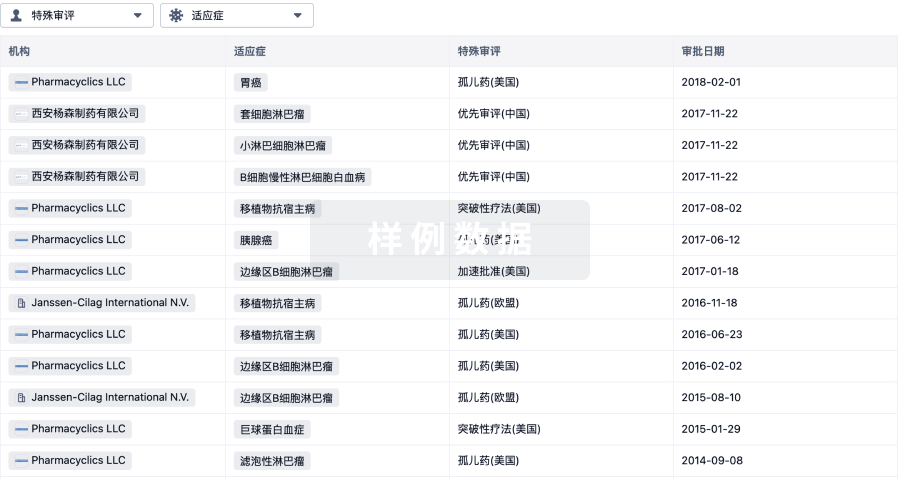
特殊审评- |
关联
100 项与 新冠疫苗 (迈科康生物) 相关的临床结果
登录后查看更多信息
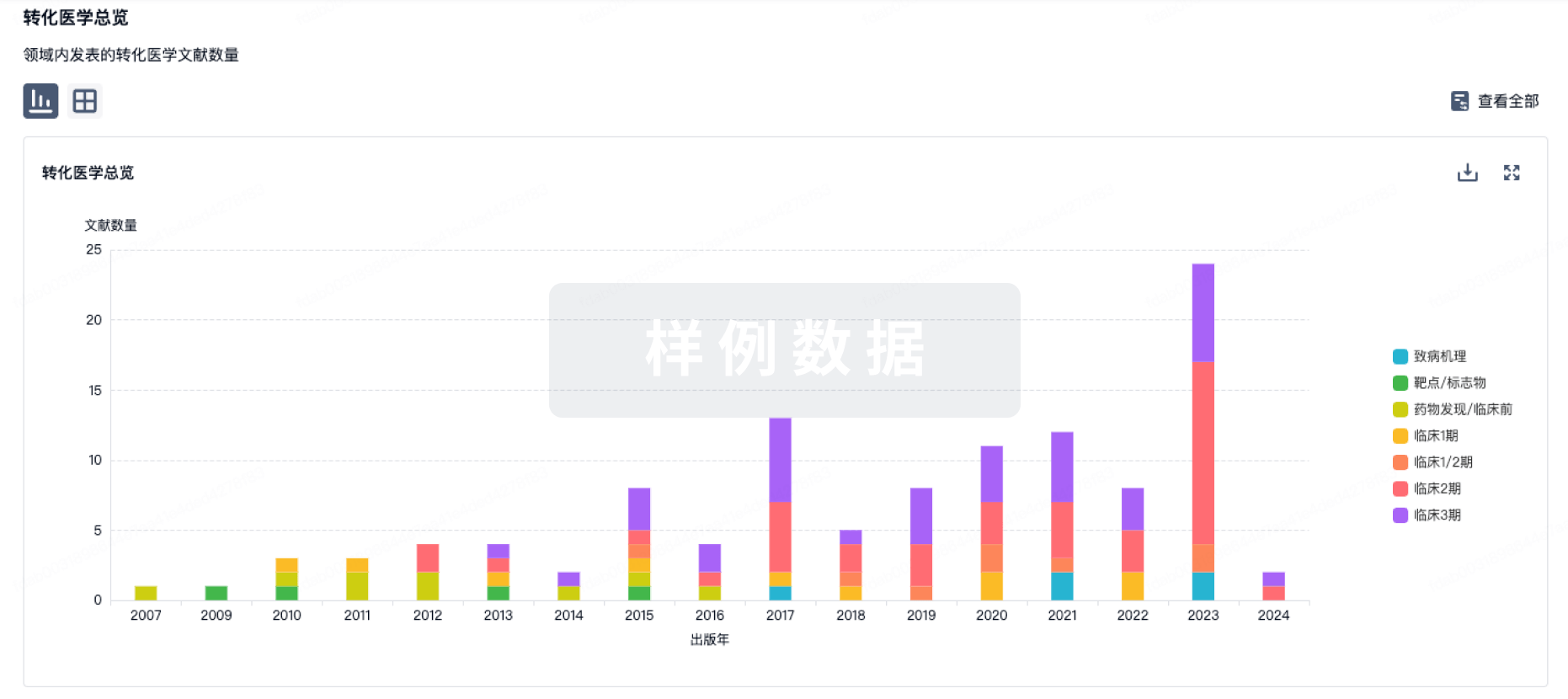
100 项与 新冠疫苗 (迈科康生物) 相关的转化医学
登录后查看更多信息
100 项与 新冠疫苗 (迈科康生物) 相关的专利(医药)
登录后查看更多信息
279
项与 新冠疫苗 (迈科康生物) 相关的新闻(医药)2024-06-06
不希望发生的事,正在发生。
当海外mRNA三剑客Moderna、BioNTech、Curevac全面复苏之际,国内mRNA产业链却全面溃败。沃森生物今日股价创下近7年新低,曾经把超一半研发费用投入到新冠mRNA疫苗临床研究中,最后拿到船票时船却不开了。国内mRNA三剑客艾博生物、斯微生物、丽凡达生物颗粒无收。
艾博生物2021年获得共计超11亿美元融资,位居全球生物技术融资之首,创始人英博意气风发:mRNA技术拥有无限潜力,而一切只是刚刚开始。
他没有说错,mRNA技术在海外狂飙突进,而国内却一直卡在开始阶段。在尖端生物科技领域,我们有停滞甚至放弃的迹象,风险宽容度最高的一级市场也变得保守。综合医药观澜数据,2024年1-5月,国内至少57家Biotech完成新一轮融资,其中仅有2家mRNA创新药企,涉及前沿技术领域的有15家,仅占比26%,以往霸榜的核酸药物、细胞疗法、基因编辑全面退潮。
回报在哪里?前沿技术穿越的死亡谷过于漫长,各方都心生寒意。当Biotech拥抱工程抗体(ADC、双抗)的组合式创新、小分子me-better的改良式创新,当传统药企驻守以仿创结合、以仿养创的商业堡垒,生物科技的中国式创新正走上一条务实的道路。
冒险精神消失了,少年老成,这是幸还是不幸?
01
mRNA外热内冷
mRNA技术没有证伪,只是在中国被打入冷宫。
Moderna的mRNA呼吸道合胞病毒(RSV)疫苗(mRESVIA)5月31日获得FDA批准上市。这是继新冠疫苗后全球第二款商业化mRNA疫苗,也是全球首款非新冠mRNA疫苗。
mRNA疫苗的成功高度依赖资本输血。mRESVIA的批准主要是基于一项在22个国家或地区开展的III期临床试验ConquerRSV,共有约3.7万名60岁或以上成年人入组。
mRESVIA在III期试验中未发现严重安全性问题,有效性方面不劣于全球已有上市的2款用于60岁以上成人的RSV疫苗,mRESVIA、Arexvy(GSK)、Abrysvo(辉瑞)分别可将RSV相关的LRTD风险显著降低83.7%、82.6%及66.7%。
2023年,Arexvy销售额为12.38亿英镑,Abrysvo销售额为8.9亿美元,mRESVIA也势必成为爆款。Moderna的2024年全年销售指引约为40亿美元,其中包括RSV疫苗的收入。
Moderna下一个重磅是mRNA-4157,有望成全球为首款上市的mRNA肿瘤疫苗,最早将于2025年商业化。与K药单药治疗相比,mRNA-4157联合K药治疗可显著改善经手术切除高风险黑色素瘤患者的无复发生存期(RFS),可使复发或死亡风险降低49%,并改善无远处转移生存期(DMFS),使患者的远处转移或死亡风险降低62%。目前该款疫苗有三项临床III期试验进行中,分别用以治疗经手术切除的黑色素瘤、非小细胞肺癌与皮肤鳞状细胞癌患者。
BioNTech在通用型肿瘤疫苗(FixVac,针对共有TAA的通用型货架产品)、细胞治疗(CARVac,CAR-T增强RNA疫苗)、细胞因子(IL-2/7)及小分子免疫调节剂(TLR激动剂)领域广泛布局。
BioNTech在手现金169亿欧元(2024Q1),成为融资渠道枯竭的中国Biotech的最大白衣骑士。自2023年起,BioNTech相继与昂科免疫、映恩生物、道尔生物、普米斯、宜联生物和药明生物达成协议,引进了多款单抗、双抗和ADC的开发和商业化权益。
Curevac今年4月催化剂不断,与德克萨斯大学MD安德森癌症中心联合开发mRNA新型癌症疫苗,与葛兰素史克合作的季节性流感疫苗开发计划的第二阶段中期数据披露。
Curevac股价自4月25日以来翻倍,主要受益于美股生物科技的整体回暖。纳斯达克生物科技指数(NBI)权重股福泰制药最近连续3天历史新高,年初以来涨幅接近19%,其他主要权重股年初以来涨幅也都可圈可点,包括Moderna莫德纳(55%)、阿斯利康(21%)、再生元制药(14%)、安进(8%)等等,BioNTech、Curevac也是其成分股。
美国通胀黏性过强,造成降息预期混乱,NBI今年经历较长时间蓄势,但长期向上趋势是明确的。6月5 日,加拿大央行宣布下调基准利率至4.75%,在G7国家中率先降息,而美国一系列经济数据疲软,5月ADP新增就业15.2万人,为3个月最低水平。市场共识转向全球降息,有利于NBI重拾升势。纳指生物科技ETF(513290)跟踪NBI,最近悄然逼近新高。
纳指生物科技ETF(513290)兼顾稳定性和高弹性,其标的指数NBI相比于XBI跟踪的标普生物科技指数的长期走势更加规整,风险收益特征更优。
错过了纳指100,不应该再错过纳指生物科技。
相信未来生物科技,定投纳指生物科技。纳指生物科技ETF(513290)在场内可以T+0交易,在场外可通过联接基金A(017894)、C(017895)进行申购、定投。
02
做配套,我们是擅长的
马云曾说:“天不怕地不怕,就怕CFO做CEO”。然后,他让张勇担任阿里巴巴CEO。
互联网科技领域的教训是,过于注重眼前的KPI、财务稳健,可能在长期的生态和创新模式迭代中输掉。
国内mRNA研发管线主要处于临床前或临床I期,创投机构确实会眼前一黑,看不到退出的那一天。
艾博生物官网称,mRNA药物研发是一场漫长的马拉松,其狂犬病疫苗、呼吸道合胞病毒疫苗(RSV)、带状疱疹疫苗、四价流感疫苗全部处于临床前阶段,肿瘤管线进度最快的是ABO2011(编码细胞因子IL-12mRNA的脂质纳米球注射液),去年6月获批临床,其他5条肿瘤管线还没提交IND。
据医药魔方数据库,国内药企开发的RSV mRNA疫苗多数处于临床前阶段。石药集团、阿法纳生物RSV mRNA疫苗IND申请均在今年4月获得受理,深信生物二价RSV mRNA疫苗IND申请在今年3月获得受理。艾美生物RSV mRNA疫苗及带状疱疹mRNA疫苗今年6月提交临床试验预申请。三叶草生物二价RSV PreF-三聚体亚单位候选疫苗,目前处于I期临床阶段。星锐医药的STR-V003海外进展较快,于6月启动I/II期研究。艾棣维欣的重组蛋白RSV疫苗(AEO11佐剂)AD110,预计2024年可以完成II期临床。
RSV疫苗算是国内mRNA非新冠管线中进展最快的,mRNA肿瘤疫苗估计还要在黑暗中摸索5年以上。尖端生物科技在早期总是会遇到效率低下、浪费巨大的问题,当前环境对这种不划算的创新模式已经没有耐心。
创新不能被计划,如果凡事都去卷即时回报、即期满足,生物科技领域将永远受制于人。
于是,引进模式再次抬头。今年2月7日,和其瑞医药完成近2亿元人民币的B+轮融资,堪称资本寒冬的一个亮点,其核心产品HMI-115是从拜耳(Bayer)引进的一款靶向泌乳素受体(PRLR)的单克隆抗体。
临床在研的基因编辑治疗项目
前面提到的福泰制药,其CRISPR/Cas9基因编辑疗法去年12月在美国上市,用于治疗12岁及以上的镰刀型细胞贫血病(SCD)患者,定价220万美元。
国内上市药企集体缺席基因编辑疗法,仅有财力薄弱、高度依赖融资的初创公司布局,并且处于临床早期,获批上市还有5年左右(详见2023年11月《基因编辑疗法在国内没戏》)。下游基因编辑公司可能会受制于支付条件,广东为地中海贫血高发病区,是目前唯一可行的商业化突破口。国内企业在基因编辑领域的优势还是做供应链,上游提供原料、耗材等基因合成,中游提供CDMO业务。
做配套,我们是擅长的。
信使RNA上市批准疫苗临床3期核酸药物
2024-06-06
·药融圈
【大会背景】
面对新时代医药行业变局,我们必须摒弃“旧地图”,用“新思路”谋发展,通过寻找战略合作伙伴而非简单的订单交易,进一步拓宽合作版图,不断锤炼发展韧劲,积极打造“新质生产力”,才可直穿寒冬,破卷重生。
2024年第六届CMC-China博览会,将于2024年8月15-16日在苏州博览中心举办,此次博览会以“洞悉医药价值,共谋突围大计”为宗旨,在嘉宾阵容、演讲主题、展商服务和资源对接等方面进行全面升级,致力于成为您“寻找到下一个战略合作伙伴”的理想平台。在CMC-China我们倡议大家用共赢的模式融入行业生态发展,摆脱“卷价格、卷质量”的困境,共创多赢未来。
本次博览会设置B、C、D、E四大场馆,涉及“生物药及合成生物学、药学CMC&创新&CXO、MAH&CXO&DDS、制药产业链”主题,精心设计300+专业议题,覆盖从仿制到创新,从研发到商业化各个环节,邀请数百位行业专家和业界精英到场,探讨前沿、分享经验,更好的破局内卷。
08/15-16
◎ 单克隆抗体药物开发策略及研发案例
◎ 双(多)特异性抗体药物开发策略及案例
◎ 复杂抗体药物开发策略
◎ 抗体偶联药物开发案例分享
◎ 细胞株的开发策略
◎ 抗体GMP审计策略及案例分析
◎ CMC开发中的产品相关及工艺相关杂质问题
◎ 稳定细胞株筛选及放大的成本效率的考虑
◎ 质量分析方法的开发案例
◎ 关键质量属性研究
◎ 抗体CMC全生命周期管理
◎ 工艺变更易忽略点
◎ 可开发性评估
◎ 抗体蛋白药物工艺开发策略
08/15 主题一
多肽及GLP-1药物未来发展趋势
◎ 09:00-09:20
国内外GLP-1/GIP双靶点药物开发格局与趋势
◎ 09:20-09:40
下一代口服GLP-1R激动剂开发
◎ 09:40-10:00
GLP1的偶联开发策略
◎ 10:00-10:20
多肽类偶联药物的研发、临床和成药展望
◎ 10:20-10:40
口服多肽和环肽的研发前景
◎ 10:40-11:00
GLP-1药物开发难点与生产挑战
◎ 11:00-11:20
多肽原料药GMP生产工艺的质量控制
◎ 11:20-11:40
绿色多肽原料制造与生产实践
◎ 11:40-12:00
多肽药物的制剂研究
◎ 12:00-14:00
午餐
◎ 14:00-14:20
多肽药物申报与生产及CMC质量研究
◎ 14:20-14:40
多肽产业的国际化之路
◎ 14:40-15:00
GLP-1的商业化和出海策略
◎ 15:00-15:20
多肽注射剂“国际化”注册及海外上市销售案例分享
◎ 15:20-15:40
多肽API供应链的机遇和挑战
◎ 15:40-16:00
GLP-1,除了减重,还能卷什么?
◎ 16:00-16:20
基于连续化学工艺的液相多肽合成
◎ 16:20-16:40
固相多肽合成方法的技术创新
◎ 16:40-17:00
合成多肽药物工艺优化
08/16 主题二
核酸药物开发论坛
◎ 09:00-09:25
新型核酸干扰药物创制和临床进展
◎ 09:25-09:50
mRNA医学:新冠疫苗及未来应用
◎ 09:50-10:15
小核酸药物出海案例分享
◎ 10:15-10:40
以核酸技术为基石的mRNA疫苗,小核酸药物和基因编辑
◎ 10:40-11:05
跨越mRNA疫苗及药物的技术和专业壁垒
◎ 11:05-11:30
mRNA疫苗非临床评价策略和关注点
◎ 11:30-11:55
小核酸药物的关键工艺和商业化要点
◎ 11:55-14:00
午餐
◎ 14:00-14:25
溶瘤病毒核酸药物的创新之路
◎ 14:25-14:50
mRNA疫苗的新型佐剂研发策略及挑战
◎ 14:50-15:15
对寡核苷酸固相合成的起始物料和关键工艺的一点思考
◎ 15:15-15:40
新型核酸药物递送系统的开发
◎ 15:40-16:05
ASO反义寡核苷酸药物技术发展现状与趋势
拟邀嘉宾
冯 冰 中肽生化 寡核苷酸研发资深总监药物出海案例分享
韩照中 领诺医药,CEO
万金桥 先衍生物,总经理
08/15 专题一
XDC领域的差异化创新和国际化策略
◎ 09:00-09:20
XDC偶联药物研发进展及挑战
◎ 09:20-09:40
ADC药物创新要点及与挑战
◎ 09:40-10:00
Nectin-4 ADC最新临床研究策略
◎ 10:00-10:20
双抗ADC早期设计和靶点选择
◎ 10:20-10:40
新型偶联技术bi-XDC的设计及优势
◎ 10:40-11:00
XDC药物国际注册策略的思考及实例分享
◎ 11:00-11:20
偶联药物BD合作与投融资策略
◎ 11:20-11:40
ADC药物出海之--海外临床开发策略和经验
◎ 11:40-12:00
偶联药物CMC难点及商业化策略
08/16 专题二
核素药物开发专题
◎ 高通量筛选技术与放射性新药物发现与优化
◎ 靶向GPC3放射性药物的筛选与开发
◎ 靶向放射性核素疗法的迭代与升级的展望
◎ 放射性药物CMC的全面解析
◎ 临床CRO助力中国放射性新药研发--挑战与应对
◎ 放射性药物注册策略与实施
◎ 医用放射性同位素的国产化及其应用
◎ 从投资角度看待放射性药物赛道
◎ 临床经验分享:靶向放射性药物对多发转移肿瘤治疗的优势
◎ 创新核药研发与商业化的新模式与案例解析
拟邀嘉宾
高长寿 信达生物,CSO
刘翠华 百奥泰生物高级副总裁
刘大涛 迈威生物,CEO
吕 明 尚健生物董事长
秦 刚 启德医药,CEO
唐华东 植德律所,合伙人
田文志 宜明昂科,创始人、董事长兼总经理
王春河 达石药业,董事长
王忠民 康方生物,副总裁
衣宪华 苏州普灵生物,CEO
张富尧 弼领生物,董事长&总经理
赵永新 多禧生物CEO
周 清 诗健生物,CEO
朱 义 百利药业,董事长
朱永红 岸迈生物,CMO
08/15AM 会场一
论坛一 农业、食品与能源
◎ 09:30-10:00
合成生物学与粮食安全
◎ 10:00-10:30
非粮生物基材料合成生物学红杉中国(拟)
◎ 10:30-11:00
合成生物学成分NMN张琦 邦泰生物创始人兼CSO
◎ 11:00-11:30
细胞培养肉与合成生物学
◎ 11:30-12:00
基因编辑与生物育种元育生物(拟)
08/15PM 会场一
论坛二 医美、医药、大健康
◎ 13:30-14:00
基于植物合成生物学的化妆品原料创新和应用王玉亮 上海交通大学农业与生物学院植物科学系党支部书记、硕导
◎ 14:00-14:30
益生菌益生元在特殊营养的创新研发和临床实证数据曾哲 达能全球研发中心(荷兰乌特勒支)高级科学家 &亚太区益生菌(科学事务)负责人
◎ 14:30-15:00
细胞外基质蛋白组合(ECMP)在美妆护肤领域应用及问题皮肤解决方案赵俊 合成生物蛋白安徽省联合共建学科重点实验室主任
◎ 15:00-15:30
珍稀药用植物天然产物的微生物人工合成刘晓楠 中国科学院天津工业生物技术研究所 副研究员
◎ 15:30-16:00
高值产物“樱花素”的“负碳”产业化开发(拟)邵惠 光玥生物创始人
◎ 16:00-17:00
圆桌讨论:合成生物学面临的监管挑战论坛嘉宾
08/15AM 会场二
论坛三 生物智造
◎ 09:30-10:00
人工智能蛋白质领域的研究(拟)洪亮 上海交通大学自然科学院与物理天文学院与药学院教授
◎ 10:00-10:30
AI技术蛋白质相互作用预测及其应用研窄常珊 江苏理工学院生物信息与医药工程研究所所长
◎ 10:30-11:00
菌种筛选与优化
◎ 11:00-11:30
AI在生物合成领域的应用
◎ 11:30-12:00
从实验室到商业化中的挑战
08/15PM 会场二
论坛三 技术、工具
◎ 13:30-14:00
酶制剂与合成生物学平台(拟)白挨玺 金斯瑞集团工业微生物事业部,南京百斯木运营
◎ 14:00-14:30
合成生物学新引擎:AI大模型改酶、挖酶&产业化案例分享(拟)卢星宇 天鹜科技CMO
◎ 14:30-15:00
酶进化技术重塑API中间体合成生态刘想 镁孚泰生物科技(上海)有限公司CEO
◎ 15:00-15:30
天然产物合成的高通量筛选
◎ 15:30-16:00
如何选择合适的高通量装置
08/16 会场一
论坛五 项目路演
◎ 09:30-09:50
非粮生物基材料项目
◎ 09:50-10:10
合成生物学与医药项目
◎ 10:10-10:30
生物酶催化相关项目
◎ 10:30-10:50
合成生物学生产代糖项目
◎ 10:50-11:10
合成生物学中试放大基地项目
◎ 11:10-11:30
AI+合成生物学应用项目
08/16 会场二
论坛六 商业化与后处理
◎ 09:30-10:00
发酵过程中的过程控制
◎ 10:00-10:30
细胞工厂的构建
◎ 10:30-11:00
合成生物学产物的后处理
◎ 11:00-11:30
胶原蛋白的分离与纯化
◎ 11:30-12:00
新型分离技术应用
08/15
FDA协会年会:加速创新药落地
◎ 精彩敬请期待...
08/16
肿瘤免疫论坛
◎ 09:00-09:20
实体肿瘤免疫治疗新策略
◎ 09:20-09:40
肝癌免疫微环境与干预策略
◎ 09:40-10:00
促肿瘤中性粒细胞的分子标记物与靶向治疗策略
◎ 10:00-10:20
免疫记忆与免疫治疗
◎ 10:20-10:40
靶向新抗原的抗肿瘤免疫治疗新策略
◎ 10:40-11:00
免疫介导的炎症性疾病的治疗
◎ 11:00-11:20
细胞免疫治疗临床转化最新进展
◎ 11:20-11:40
NK细胞治疗急性髓系白血病
◎ 11:40-12:00
肿瘤治疗的细胞药物递送系统的研究进展
◎ 12:00-14:00
午餐
◎ 14:00-14:20
CAR-T细胞产品的开发策略、临床应用与研究进展
◎ 14:20-14:40
血液肿瘤的免疫治疗-从新靶点发现到新型抗体与细胞治疗转化
◎ 14:40-15:00
双细胞免疫治疗在实体瘤以及联合治疗的进展
◎ 15:00-15:20
IPSC来源内皮祖细胞治疗脑卒中的临床应用
◎ 15:20-15:40
嵌合抗原受体T细胞免疫疗法(CAR-T)在消化道肿瘤的研究进展
拟邀嘉宾
李 斌 上海交通大学特聘教授、上海市免疫学研究所科研副所长
李 佳 朗盛投资,合伙人
李其翔 翰思生物,联合创始人&总裁和首席科学官
王晶晶 冠科生物 太仓公司总经理
邢 锋 瑅安生物,首席执行官
殷文颉 亘喜生物,药理毒理部高级总监
08/15AM 专题一
洞察创新药未来发展趋势
◎ 09:00-09:20
下一代可能的突破性治疗手段
◎ 09:20-09:40
中国生物医药投资热点的演变
◎ 09:40-10:00
立项如何选择差异化的未满足需求
◎ 10:00-10:20
核酸药物未来发展趋势
◎ 10:20-10:40
多肽药物未来发展趋势
◎ 10:40-11:00
ADC/抗体/小分子药物未来发展趋势
◎ 11:00-11:20
从数据的角度看趋势
◎ 11:20-11:40
从咨询的角度看趋势
◎ 11:40-12:00
从媒体的角度看趋势
08/15 PM 专题二
中国新药的理性发展方向(20min*7)
◎ 精彩敬请期待....
拟邀嘉宾
陈 椎 和誉医药,联合创始人兼CSO
戴卫国 丹罗生物,董事长
党 群 真实生物,总裁
杜镇建 北京富龙康泰的研发负责人
冯 焱 领泰生物,创始人&CEO
华 烨 烨辉医药,董事长兼首席执行官
李英富 成都海博为,创始人&董事长
刘 谦 阿斯利康中国,副总裁
任 峰 英矽智能,CEO
童友之 开拓药业,创始人&董事长&CEO
杨建新 基石药业,CEO
叶俊青 勃林格殷格翰外部创新合作中心,首席科学家
朱继东 奕拓医药,CEO
朱永强 江苏正大丰海制药,副总经理/药物研究院院长
08/16 AM
◎ 09:00-09:05
主持人开场
◎ 09:05-09:25
2024全球生物医药License/并购趋势与策略
◎ 09:25-09:50
炉边对谈:BIOSECURE前时代,中美生物医药如何实现业务承接和转型?
◎10:10-11:00
圆桌讨论:那些没有进入MNC视野的Biotech,出路在哪里?
◎ 10:50-11:00
茶歇
◎ 11:00-12:00
圆桌讨论:中国本土Pharma并购Biotech的底层逻辑与风险
08/16 PM
创新项目路演*9(20min/项目)
08/15 专题一
◎ 专题1:肿瘤领域临床开发策略20min*4
◎ 专题2:CNS临床开发策略20min*4
◎ 专题3:麻醉领域临床开发策略 20min*3
◎ 专题4:呼吸领域临床开发策略 20min*3
◎ 专题5:胃癌领域临床开发策略 20min*3
08/16 专题二
◎ 专题6:肺癌领域临床开发策略20min*4
◎ 专题7:临床数据统计与分析
监管科学视角下临床研究设计和质量的重大意义
侯 艳 北京大学,教授
新法规时代对药品临床试验的科学监管
田少雷 国家局食品药品审核查验中心原学术委员会副主任委员、处长
数字化助力监管决策——面向药品现代化监管的智能化服务平台
王维玉 北京灵迅医药科技公司的联合创始人
◎ 专题8:医学写作的挑战(20min*3)
拟邀嘉宾
陈柏州 加立生科,CEO
侯 艳 北京大学,教授
胡邵京 思康睿奇,CEO
黄 薇 石药集团 首席医学官
李 一 凯博思,副总裁
苏 霞 康龙化成,定量药理高级总监
田少雷 国家局食品药品审核查验中心原学术委员会副主任委员、处长
王维玉 北京灵迅医药科技公司的联合创始人
杨修诰 石药集团,高级医学总监
08/15
◎ 精彩敬请期待...
08/16
小分子cmc全生命周期管理
◎ 09:00-09:20
创新药CMC开发经验及案例分享
◎ 09:20-09:40
早期从CMC角度分析创新药的成药性
◎ 09:40-10:00
小分子创新药早期CMC开发策略
◎ 10:00-10:20
如何做好全周期CMC变更管理
◎ 10:20-10:40
创新药CMC开发经验及案例分享
◎ 10:40-11:00
有限时间下的小分子创新药的可开发性评估
◎ 11:00-11:20
后期及商业化阶段创新药CMC要点
◎ 11:20-11:40
小分子药物稳定性质量研究要点
◎ 11:40-12:00
新药研发中的关键晶型问题
◎ 12:00-14:00
午餐
◎ 14:00-14:20
临床早期原料药快速推进方案
◎ 14:20-14:40
原料药工艺开发的问题与思考
◎ 14:40-15:00
创新原料药不同研发阶段的质量控制标准
◎ 15:00-15:20
效率和成本之间的平衡新药原料药早期研发阶段质量
◎ 15:20-15:40
创新药早期注册策略与药学研发策略如何实现协同
◎ 15:40-16:00
创新药IND阶段CMC研究与可交付成果
◎ 16:00-16:20
创新药临床试验期间制剂变更评估和策略
◎ 16:20-16:40
原料药工艺变更后的杂质研究
拟邀嘉宾
陈 洪 苑东生物,副总经理
Elena FLAMMA,董事长
08/15
创新药中美双报如何制定研发策略
◎ 09:00-09:30
抗体药物中美IND快速申报策略
姜伟东 康抗生物,创始人&CEO
◎ 09:30-10:00
CAR-T产品美国申报上市经验分享
范晓虎 湾岛细胞创始人
◎ 10:00-10:30
中美IND申请非临床研究要点
◎ 10:30-11:00
中美申报CMC要点
Audrey Jia DataRevive德瑞达公司,总裁;前FDA CDER审查员
◎ 11:00-11:30
中美双报生物分析策略与实操分享
邹灵龙 康维讯,CEO
◎ 11:05-12:00
圆桌对话
◎ 12:00-14:00
午餐
◎ 14:00-14:30
支持出海申报的免疫原性分析要点
◎ 14:30-15:00
出海申报的临床试验设计与数据管理
杨修浩 石药集团,高级医学总监
◎ 15:00-15:30
支持出海的ADC毒素ADME研究
朱明社 南京美新诺医药,首席科学家
◎ 15:30-16:00
中美药品电子申报 (eCTD)要点
08/16
制剂出海论坛
◎ 精彩敬请期待...
拟邀嘉宾
Audrey Jia DataRevive 德瑞达公司,总裁裁;前FDA CDER审查员
范晓虎 湾岛细胞创始人
姜伟东 康抗生物,创始人&CEO
杨修浩 石药集团,高级医学总监
朱明社 南京美新诺医药,首席科学家
邹灵龙 康维讯,CEO
08/15
精准递送-纳米制剂专场
◎ 09:30-10:00
纳米制剂发展现状与新型纳米技术应用探索
◎ 10:00-10:30
纳米药物药代动力学的研究策略与相关技术指导原则解读
◎ 10:30-11:00
优化脂质体药物制剂的体内过程
◎ 11:00-11:30
药物纳米晶制备技术助力我国药物制剂创新发展
◎ 14:00-14:30
纳米脂质注射剂及其用于药物递送的研究和产业化
◎ 14:30-15:00
纳米药物的设计与临床转化
◎ 15:00-15:30
纳米制剂工业化的难点与解决方案
◎ 15:30-16:00
核酸纳米粒505(b)(2)微球及纳米乳液
◎ 16:00-16:30
纳米药物的理化CMC及其药效适配研究
08/16
攻克高精尖-复杂注射剂专场
◎ 09:30-10:00
长效注射剂现状、机遇和挑战
◎ 10:00-10:30
复杂注射剂产品设计与质控策略
◎ 10:30-11:00
复杂注射剂从小试、中试、到大生产应该注意的工艺问题
◎ 11:00-11:30
注射剂包装材料的技术要求与相容性研究
◎ 14:00-14:30
二代载药脂微球研发策略与临床研究思考
◎ 14:30-15:00
原位凝胶在药物递送中的应用和难点及案例分析
◎ 15:00-15:30
PIC/S GMP无菌药品附录对我国无菌药品检查的影响
确定出席嘉宾
李亚平 中国科学院上海药物所研究员/药物制剂研究中心主任
夏禄华 原康希诺(上海)生物科技有限公司副总经理
申有青 浙江大学教授祁小乐 中国药科大学教授
08/15 AM
入门篇—B证企业法规政策
◎ 9:30-10:00
MAH 制度渊源及现阶段B证行业趋势分析
◎ 10:00-10:30
B证企业关键人员能力素养要求
◎ 10:30-11:00
B证企业实战经验分享:现行法规下如何办理B证
◎ 11:00-11:30
B证企业质量体系建立及全生命周期质量风险管理
08/15 PM
生产篇—B证企业委托生产
◎ 14:00-14:30
委托生产最新监管政策解读
◎ 14:30-15:00
MAH B证企业如何遴选审核受托生产企业?
◎ 15:00-15:30
B证企业委托生产共线风险评估及案例分享
◎ 15:30-16:00
MAH药品全生命周期管理实践经验
◎ 16:00-16:30
【圆桌论坛】卑微“甲方”B证公司与“不听话”乙方受托生产企业
08/16 AM
产品篇—B证企业产品立项
◎ 9:30-10:10
MAH B证企业产品立项思路及案例
◎ 10:10-10:50
MAH制度下药品工艺技术管理
◎ 10:50-11:30
MAH制度下产品技术转移法规要求及常见问题
◎ 11:30-12:00
MAH B证企业药品注册现场核查关注点及缺陷案例分析
08/16 PM
变更篇—B证企业变更管理
◎ 14:00-14:30 药品上市后变更管理法规及申报策略
◎ 14:30-15:00
MAH制度下场地变更法规要求和实操指南
◎ 15:00-15:30MAH制度下持有人变更法规要求和实操指南
确定出席嘉宾
谭宏宇 上海淦堃生物医药技术工作室创始人
张自然 中国化学制药工业协会医药政策法规专业委员会主任
毕瑞凤 资深GMP 专家
谢海燕 丽珠医药集团质量管理总部总经理兼制剂质量总监
丽珠医药集团B证质量负责人
广东省药学会 药品生产质量受权人专业委员会 主任委员
吴 军 药品制造系统工程与GMP专家
邵 蓉 中国药科大学NDPE执行副主任、药品监管科学研究院执行院长
杨老师 原CDE审评专家
黄小枫 华益药业质量受权人
杨国华 国家GMP检查员,国家药监局高级研修学院特约讲师
08/15 AM
百亿赛道—吸入制剂究竟该如何做?
◎ 9:30-10:00
对吸入给药创新的思考
◎ 10:00-10:30
吸入制剂研发思路及关键要素
◎ 10:30-11:00
改良型吸入制剂开发策略与难点分析
◎ 11:00-11:30
干粉吸入剂(吸入粉雾剂)研发难点及挑战
08/15 PM
乘风破浪—吸入制剂BE研究挑战性在哪?
◎ 14:00-14:30
吸入制剂人体生物等效评价研究
◎ 14:30-15:00
吸入制剂关键质量属性研究以及吸入仿制药体外生等效APSD评价方法及重点
◎ 15:00-15:30
吸入制剂FDA与欧盟BE差异
◎ 15:30-16:00
吸入制剂临床研究策略与典型案例分析
08/16 AM
未来已来—吸入制剂产业化壁垒?
◎ 9:30-10:00
高壁垒吸入剂开发,如何占据竞争优势
◎ 10:00-10:30
鼻喷雾剂的开发及质量研究
◎ 10:30-11:00
吸入气雾剂产业化过程工艺控制
◎ 11:00-11:30
吸入制剂包装相容性研究与实施
08/16 PM
道阻且长—吸入制剂如何翻越审批大山?
◎ 14:00-14:30
美国FDA吸入制剂审评及其指导原则的思考
◎ 14:30-15:00
吸入制剂注册申报关键要点及案例分析
◎ 15:00-15:30
干粉吸入制剂的中欧审评评价及技术难点
确定出席嘉宾
游一中 常州市第一人民医院主任药师、副主任医师、中国包装联合会气雾剂专业委员会终身荣誉主任、中国颗粒学会吸入颗粒专委会名誉主任
郑 恒 国家药品审评中心专家, 湖北省药监局核查专家
沈丹蕾 全国吸入给药联盟主席,南京白令信息科技有限公司总经理
佟振博 东南大学教授
谷 丽 南京樟益医药科技有限公司 创始人和总经理
蔡 荣 高级工程师(教授级)、原上海市食品药品包装材料测试所
陈永奇 珠海瑞思普利医药科技有限公司董事长兼首席科学家史楷岐 博士、苏州易合医药有限公司创始人/总经理
08/15 AM
洞悉政策,鉴透皮之脉络
◎ 09:30-10:00
国内透皮制剂研究进展和申报格局
◎ 10:00-10:30
透皮制剂产品开发的国内外法规对比及案例分析
◎ 10:30-11:00
经皮半固体制剂的处方工艺开发和表征
◎ 11:00-11:30
可溶微针技术在医药领域的应用和挑战
08/15 PM
解构技术,破透皮之难点
◎ 14:00-14:30
Innovations for health. TTS/OTF/MAP/OBDS drug delivery solutions for improved patients’ outcome
◎ 14:30-15:00
外用制剂体外释放方法及实验注意事项
◎ 15:00-15:30
透皮制剂的辅料现状与展望
◎ 15:30-16:00
贴膏贴剂制剂开发及 PK-BE 评价的挑战及案例分析
◎ 16:00-16:30
【圆桌论坛】
①中国和日本在透皮贴剂的差距;
②氟比洛芬凝胶贴膏为何能一举突破20亿,成为TOP品种;
③如何解决透皮贴剂体外吸收效率低下的问题
08/16 AM
迭变技术,执透皮之要领
◎ 9:30-10:00
国内外透皮贴剂申报上市进展及药学研究
◎ 10:00-10:30
外用制剂质量研究及体外评价
◎ 10:30-11:00
透皮制剂的临床试验设计及要点
◎ 11:00-11:30
经皮给药制剂设计与质量控制
08/16 PM
参比案例,融透皮之万方
◎ 14:00-14:30
以阿达帕林凝胶贴膏为例,产品立项及开发壁垒
◎ 14:30-15:00
以氟比洛芬凝胶贴膏为例,产品立项及开发壁垒
◎ 15:00-15:30
以他克莫司软膏为例,产品立项及开发壁垒
确定出席嘉宾
全丹毅 江苏集萃新型药物制剂技术研究所董事长、所长
刘亚利 汕头大学医学院第一附属医院机构副主任、I期病房主任
谷 丽 南京樟益医药科技有限公司创始人、总经理
张海龙 长沙晶易医药科技股份有限公司总裁
Stefan Arnold LTS Lohmann Therapie-Systeme AG亚洲业务发展总监兼亚洲办事处主任
李成国 优微(珠海)生物科技有限公司联合创始人
张哲峰 南京知和医药董事长、首席咨询师
段云剑 深圳市华溶分析仪器有限公司技术总监
吴正红 中国药科大学教授、博士生导师
08/15 AM
◎ 9:30-10:00
仿制药企业战略重构:从大产品策略到大品牌战!
◎ 10:00-10:30
撬动大健康产业“蓝海”,药企如何优化战略布局?
◎ 10:30-12:00对话决策层 | 30位企业家/决策层核心观点碰撞
对话决策层 | 苦练内功 静待时机
对话决策层 | 大浪淘沙,国产仿制药品牌的创世纪
对话决策层 | 穿越内卷,剩者为王
对话决策层 | 精准聚焦,营销赋能
对话决策层 | 寒冬过尽,破晓已至
对话决策层 | 价值医疗时代已经来临,唯有创新才能赢得未来
对话决策层 | 在核心领域,行使自己的核心竞争力
........
08/15 PM
◎ 14:00-14:30
2024年仿制药行业10大现状
◎ 14:30-15:00
面向未来的仿制药立项,如何“以终为始”?
◎ 15:00-16:30对话决策层 | 20位企业家/决策层核心观点碰撞
对话决策层 | 剂型差和产品差是未来专科适应症领域解决方案的出路
对话决策层 | 危机中谋求转机
对话决策层 | 让创新可持续
........
08/15 AM
政策春风—中药政策解读
◎ 9:30-10:00
中药大时代,国内中药政策全面解读
◎ 10:00-10:30
中药注册管理专门规定政策解读
◎ 10:30-11:00
中药配方颗粒相关政策法规及监管探讨
◎ 11:00-11:30
中药注册变化后有效性安全性要求
08/15 PM
黄金赛道—中药开发&质量研究
◎ 14:00-14:30
新形势下中药新药研发思路与策略
◎ 14:30-15:00
首创高端中药制剂CMC研发流程
◎ 15:00-15:30
基于源头控制的中药制剂质量研究
◎ 15:30-16:00
基于中药有效成分的原创靶点发现
◎ 16:00-16:30
透过“百令胶囊”看同名同方药研发、审评趋势
08/16 AM
◎ 9:30-10:00
中药院内制剂开发的问题与策略
◎ 10:00-10:30
经典名方研发关键技术问题与解决方案
◎ 10:30-11:00
中药新药质量标准研究
◎ 11:00-11:30
中药连续制造研究及应用进展
08/16 PM
大有可为—中药临床与真实世界研究
◎ 14:00-14:30
源于临床经验的中药新药研发策略与实践
◎ 14:30-15:00
基于真实世界数据的中药安全性评价技术与方法
◎ 15:00-15:30
“三结合”审评证据体系下中药新药临床研究
确定出席嘉宾
杜若飞 上海中医药大学副研究员
姜宝红 中国科学院上海药物研究所研究员
周水平 天津天士力研究院执行院长
陈大全 烟台大学教授
孙 鑫 四川大学华西公共卫生学院(华西第四医院) 副院长
四川大学华西医院中国循证医学中心/中国Cochrane中心 主任
柏 冬 中国中医科学院中医基础理论研究所中医方证研究中心主任,研究员,博士研究生导师
程建明 南京中医药大学药学院教授,江苏省经典名方工程中心主任
08/15 AM
◎ 09:30-10:00
改良型新药研发过程中的成功与失败案例剖析
◎ 10:00-10:30
毛囊源性皮肤病的药物靶向递送和改良新药开发
◎ 10:30-11:00
复杂注射剂改良型新药研发关键技术和实例分析
◎ 11:00-11:30
改良型新药中的新适应症产品开发策略及案例分析
08/15 PM
◎ 14:00-14:30
以亮丙瑞林/戈舍瑞林为例的注射用微球制剂研发案例
◎ 14:30-15:00
从紫杉醇制剂迭代看改剂型新药设计思考
◎ 15:00-15:30
基于“药辅合一”的天然成分纳米递送系统研究案例
◎ 15:30-16:00
中药改良新药研发案例分析
◎ 16:00-16:30
以GLP-1为例的微针贴剂研发案例及分析
08/16 AM
◎ 09:30-10:00
以洛索洛芬/氟比洛芬为例的凝胶贴膏研发难点解析
◎ 10:00-10:30
以阿尔兹海默症为例的纳米药物递送研发案例分享
◎ 10:30-11:00
以右美托咪定为例的鼻用喷雾剂研发案例分享与思考
◎ 11:00-11:30
难溶性药物口服制剂关键技术及案例分享
08/16 PM
◎ 14:00-14:30口溶膜剂在儿科改良型新药中的案例分析
◎ 14:30-15:00
以干眼症为例的眼用制剂研发案例分享与思考
◎ 15:00-15:30
植入式给药系统在改良新药研发中的应用案例
确定出席嘉宾
何仲贵 沈阳信达泰康医药科技有限公司首席科学家
杨 劲 中国药科大学教授
高会乐 四川大学教授
张 宇 沈阳药科大学教授
张 宁 西交利物浦大学教授,原CDE高级审评员
盛晓霞 杭州领业医药科技有限公司总经理
王泽人 深圳药欣生物联合创始人、董事长和首席科学家
08/15 AM
◎ 09:30-10:10
从仿制药到改良型新药:我国医药企业的转型升级之路
◎ 10:10-11:10
高度内卷之下,仿制药的立项思路与产品布局
◎ 11:10-11:40
基于临床需求的改良型新药立项策略与实施案例
08/15 PM
◎ 14:00-14:40
以透皮给药技术平台为导向的产品立项及案例分享
◎ 14:40-15:20
以渗透泵技术平台为导向的产品立项及案例分享
◎ 15:20-16:00
以眼部给药技术平台为导向的产品立项及案例分享
◎ 16:00-16:40
以儿科药物掩味技术平台为导向的产品立项及案例分享
08/16 AM
◎ 9:30-10:10
产品为王——以产品线规划选品思路
◎ 10:10-10:50
成本优势——以集采品种选品思路
◎ 10:50-11:30
独一无二——以特色、差异化布局选品思路
08/16 PM
◎ 14:00-14:40
遥遥领先——以市场消费趋势为导向选品
◎ 14:40-15:20
未雨绸缪——以临床需求为导向选品
◎15:20-16:00
另辟赛道——以技术平台为导向选品
确定出席嘉宾
魏利军 北京药眼信息咨询有限公司创始人兼CEO
张廷杰 风云药谈 创始人
吴翠栓 北京德立福瑞 执行董事
郭新峰 南京循证生物科技有限公司创始人
魏世峰 北京罗诺强施医药技术研发中心有限公司董事长兼CEO
陈 洪 博士
吴 涛 北京汇诚瑞祥医药生物科技有限公司 首席科学家
08/15 AM观大势 谋全局-行业趋势、研发立项专场
◎ 09:30-10:00
我国缓控释制剂发展态势及战略对策
◎ 10:00-10:30
以缓控释新药为例探讨改良型新药的立项
◎ 10:30-11:00
口服缓控释制剂的特点和临床应用
◎ 11:00-11:30
缓控释制剂开发重难点剖析及案例分享
08/15 PM闯新路 走在前-制剂工艺专场
◎ 14:00-14:30
基于制剂结构的缓控释制剂反向工程
◎ 14:30-15:00
缓控释制剂中关键辅料应用及相关技术探讨
◎ 15:00-15:30
热熔挤出和连续制粒
◎ 15:30-16:00
缓控释制剂的技术可行性评估和处方工艺的选择
◎ 16:00-16:30
亲水凝胶缓释骨架片关键技术与案例分享
08/16 AM涉激流 过险关-注册审评专场
◎ 09:30-10:00
CDE审评中缓控释制剂常见问题及案例分析
◎ 10:00-10:30
口服缓控释产品中美双报的技术和法规要求
◎ 10:30-11:00
口服固体缓控释制剂BE审评
◎ 11:00-11:30
口服固体缓释控释制剂一致性评价注册现场核查
08/16 PM闯新路 走在前-制剂工艺专场
◎ 14:00-14:30
口服固体缓控释制剂的工艺和质量研究
◎ 14:30-15:00
口服缓控释制剂的产业化研究
◎ 15:00-15:30
缓控释制剂技术相关话题
08/15国际原料药供应对接
◎ 09:30-10:00对接国内和海外采购负责人
◎ 10:00-10:30原料药中间体与合成生物学、连续流的融合
◎ 10:30-11:00原料药与下游MAH B证关联战略合作
◎ 11:00-11:30研发和生产企业资源对接,项目战略合作落地
◎ 14:00-14:30研发企业如何与上市企业合作,资本化退出
◎ 14:30-14:50药企寻找原料药合作的与原料药CRO形式合作
◎ 14:50-15:10国内原料药CDMO未来业态预测,并现场大家可以找合作
◎ 15:10-15:30跨界重生、不内卷
08/16 PM闯新路 走在前-制剂工艺专场
◎ 09:30-10:00
关联审评审批制度下药用辅料的登记与变更
◎ 10:00-10:30
新型药用辅料发展趋势及其在制剂中的应用和风险考量
◎ 10:30-11:00
药品上市后药用辅料变更研究的技术考量
◎ 11:00-11:30
药用辅料的质量研究和标准制定考量
◎ 14:00-14:30
高端制剂用特殊功能性辅料实例分析研究
◎ 14:30-14:50
以口服固体制剂为例的关键药用辅料应用
◎ 14:50-15:10
以透皮制剂为例的关键药用辅料应用
◎ 15:10-15:30
以注射剂为例的关键药用辅料应用
08/15绿色制药技术大会:催化剂
◎ 09:30-10:00
绿色制药理念及工业化发展
◎ 10:00-10:30
不对称催化的实际应用和案例
◎ 10:30-11:00
氧化反应、催化氧化如何实现降本增效
◎ 11:00-11:30
绿色制药的挑战和机遇
◎ 14:00-14:30
催化技术在能源转化和环境保护中的应用
◎ 14:30-14:50
催化反应工程的建模设计和优化
◎ 14:50-15:10
催化剂的活性和选择性调控
◎ 15:10-15:30
源于工艺的连续流差异化开发实践
◎ 15:30-16:00
连续性反应技术在小分子原料药商业化生产中应用
◎ 16:00-16:30
绿色催化技术及产业化应用
08/16绿色制药技术大会:连续流
◎ 09:30-10:00
连续流差异化开发策略
◎ 10:00-10:30
小分子合成的连续流改造
◎ 10:30-11:00
连续流制造技术未来发展变革趋势
◎ 11:00-11:30
小分子合成的连续流改造实践案例分享
◎ 14:00-14:30
如何将绿色制药原则与连续流制造技术结合实现可持续药品生产
◎ 14:30-14:50
反应中间体的转化和连续流系统的设计案例分享
◎ 14:50-15:10
绿色分析技术在连续流制造中的应用
◎ 15:10-15:30
连续流微化工放大生产之硬件如何改造升级
◎ 15:30-16:00
制药行业连续化装备的难点卡点
◎ 16:00-16:30
绿色化学的本质及实现路径
08/15绿色制药技术大会:连续流
◎ 09:30-10:30从集采及企业战略浅谈产品立项
◎ 10:30-11:30原料制剂一体 专精特新深耕
◎ 14:00-15:00把优势平台化 做行业合作者
◎ 15:00-16:00Big Pharma如何引领行业“潮流”
08/16原料药企业家年会
◎ 09:00-09:30原料药制剂垂直产业链合作探讨
◎ 09:30-10:00CMC原料药年度观点分析
◎ 10:00-10:30原料企业未来发展展望
◎ 10:30-11:00如何在医药寒冬让原料药行业重获新生
◎ 14:00-14:30特色原料药的发展思路
◎ 14:30-15:00新形势下,原料药公司的“新增量
◎ 15:00-15:30原料药国际贸易形势与展望
◎ 15:30-16:00小品种原料药的布局之道
08/15 AM
医药全渠道营销
◎ 09:00-09:30
后MAH时代中国医药市场发展趋势分析
◎ 09:30-10:00
集采反腐之下,院内处方药院内推广策略
◎ 10:00-10:30
线上线下融合,中国医药零售大变局
◎ 10:30-11:00
全维度解析--院外市场面面观
08/15 PM
医药产品的商业化落地策略
◎ 13:00-13:30
药品学术体系搭建与合规推广
◎ 13:30-14:00
模式之战——决胜第三终端市场
◎ 14:00-14:30
品牌药的集约推广——白龙马之路
◎ 14:30-15:00
合规与数字化的双链路,如何速打造团队
◎15:00-15:30
专业的区域CSO如何帮助产品快速发展?
08/16 AM
医药产品的商业化落地策略
◎ 09:00-09:30
专业的区域CSO如何帮助产品快速发展?
◎ 09:30-10:00
数字化推广在创新药品推广中的实战应用
◎ 10:00-10:30
代理制模式下,企业如何培养发展“学术专员”队伍
◎ 10:30-11:00
专家讨论:下一个风中,是创新药吗?
08/16 PM
批文交易大会
以上议程更新中,以会议现场为准...
END
苏州国际博览中心
2024年8月15-16日
观众限时免费登记,提前锁定门票!
↓ 请点击下方“阅读原文” ↓
2024-06-06
该问题表现的既棘手又有热门趋势:棘手的是,当前来自妇幼和疾控两方权威意见不统一,甚至相左;热门倾向的是,九价不缺货了,导致一些主观安全感不够的女性需求在增加。
现在讨论这个问题可能恰逢其会——比起既往九价“紧俏”下明显的排他主义,继续矜持可能对于库存压力有害无利,因此更重要的是探讨如何解决这一问题。
01/ 当前相左的两个权威意见是什么?
医防双方对接种必要性的分歧较小——仅靠打HPV疫苗,无论几价都不可能完全避免宫颈癌的发生。筛查,尤其是已经有性生活的女性(无论是否接种疫苗),筛查是必不可少的。
因此,国内外专家对于打完二价或四价再打九价的必要性意见一致——暂无必要。对于高风险人群,更应该注重定期筛查和症状预警。
而现实关于打完二价或四价再打九价的研究和循证证据几乎为0,也可见其必要性和实际意义可能确实不大。 而在能不能打的问题上,双方分歧较大:
权威意见1:主要是妇幼保健临床专家的可以接种。该意见的权威性源于宫颈癌和HPV疫苗的目标对象是女性,女性健康促进行为离不开妇科专家指导。目前HPV疫苗应用认可度最高的专家共识——《人乳头瘤病毒疫苗临床应用中国专家共识(2021年)》,就是由妇幼保健专家所在的多个协会制定和发布。
权威意见2:主要是疾控体系的暂不推荐,也有自行加码后给出“不能接种”者(如四川疾控是“暂不推荐”,而自贡疾控是“不能”)。该意见的权威性源于疫苗属于疾控管理范畴,接种HPV疫苗只能前往接种门诊。
图左:四川省疾控公众号;图右:自贡市疾控公众号
这种意见相左的情况美国也有:九价疫苗说明书提到,接种完四价可在一年后重新全程接种九价。但如果参考美国妇产科学会的建议,接种完四价不建议再重新接种九价。(其实前者回答的是“能不能”,后者回答的是“有没有必要”)
而就近的驳论例子也有:去年打完单价的灭活新冠疫苗,今年能不能打二价的重组蛋白新冠疫苗?去年打了三价的流感疫苗,今年能不能再打四价的流感疫苗?当然能,且有必要。(主要从必要性考虑)
听谁的?听谁的似乎不重要,医防“分家”的现状下,接种门诊不给接种,受种者也就丧失了参与决策权。
02/ 为何会出现意见相左的情况?
出现这两种意见相左的根本原因,并非是疫苗本身的原因,更可能是双方知识结构和工作性质的差异。
疾控体系应当站在公共卫生层面施策,接种决策建议通常较为保守。他们习惯于“法无允许应规避”,而非“法无禁止皆可行”——这里的“法”指的是法律法规和说明书等具备法律效力的资料。
实际上关于打完二价暂时不推荐再打九价,麻烦的问题不是问题本身,而是说明书中没有讲打完二价多久可以打九价——这就需要证据的支撑。
客观原因是疫苗生产企业不同,企业缺乏支持该系列临床试验的动力。当然也不排除像四、九价公司出于市场考虑的那样,近几年国产二价可能大概率会补充打完二价打九价的临床研究证据,比如同时具有国产二价和国产九价(将上市)的万泰、沃森。
此外还涉及疫苗管理:一旦放开口子那HPV疫苗可能会面临着更加无序的预约接种场面(过去是这样)、接种率的统计也更麻烦,并且也可能会增加预防接种差错的风险……所以也应理解CDC的苦衷。
并且疾控体系出于对疫苗制造商利益点的规避,对于能否接种的答复会更谨慎。当然不排除一些地区会采取“一刀切”的策略,避免不必要的麻烦。
图源于PATH组织官网
临床系更多基于个体层面的考虑。他们可能把二价和九价当做两款疫苗,不需要考虑疫苗管理是否便利、接种工作检查和投诉等复杂情况,只需要权衡风险和获益,可以看作是来自“第三方”专业人士的建议。
他们临床用药经验丰富且善于举一反三:已知二价基本等于四价,既然打了四价能打九价,那打完二价自然也可以打九价。目前缺乏证据支持打完二价再打九价,当然也没有证据显示打完二价再打九价会出现糟糕的情况,因此直接参考四价证据就OK——打完二价或四价后至少间隔1年后可接种九价。
严重不良事件对于疫苗来说本身就是小概率事件,任何疫苗都可能发生。根据《全国疑似预防接种异常反应监测方案》,AEFI的最长报告时限为12个月(卡介苗)。因此理论上来讲,间隔1年再接种的疫苗出现的严重不良事件,不应牵连前列疫苗。
03/ 现有的循证证据怎么说?
既往多款新冠疫苗的临床证据提示,异源序贯接种的免疫原性可能比同源更强。那么这是否也意味着,打完二价再打异源的九价,一些型别的免疫原性是否要优于打完四价再打同源的九价?
九价说明书中引用的“打完四价1年后接种九价”的研究证据,源于2015年默克公司(四、九价生产商)资助的1项随机对照临床研究。
研究背景和大家的诉求差不多——先前接种了四价的人可能会认为对HPV型别的更广泛保护是有价值和适当的,并寻求九价HPV疫苗的额外覆盖。(实际上妇科体系基本都不建议也认为没必要这样做,更多是市场需求下的商业考虑)
研究尽管给出了“对曾接种过四价的12-26岁青少年女性,再接种3剂九价后HPV31/33/45/52/58型具有较高的免疫原性,而且总体上耐受性良好”的结论,但在结果部分同时提到了一个临床意义不明的发现——虽然HPV6/11/16/18型在加强后抗体水平更高,但另外5种型别HPV 31/33/45/52/58的抗体水平均显著低于仅直接接种九价的女性。
图源于文献:左侧此前接种过4价再接种9价者,右侧为直接接种9价者
该现象不确定是否是由同源接种带来的结果,也可能受到HPV6/11/16/18型抗体反应增强的同时,抑制了其他同个亚支型别的免疫反应——即受到了抗体交叉反应的影响。HPV31/33/52/58型与HPV16同属于HPV大家族的α-9支,HPV45则与HPV18同属α-7。
另外一项使用二价和九价的混合序贯免疫研究也有类似发现:在两针程序中,1针二价、2针打九价的研究组,9个型别全部阳转,并且HPV16/18型抗体水平更高。并且在打了第1针二价后,已经有50.0%-76.7%的受试者对九价其他7个型别产生了不同水平的抗体,这也证实了型别相似性带来的交叉免疫反应的存在。
总之,若打完二价者有强烈打九价的意愿,建议至少间隔12个月(其他型别没那么快到癌,已到癌大概率是接种前已到癌)。若接种门诊不依从,当我没说……
04/ 是否应考虑正在发生的变化?
目前的立场文件到底怎么说
事实上关于接种完四价1年后可接种九价的证据质量并没有那么高:不仅局限于样本量较小的研究,且缺乏多个可以复现的临床试验,并且面对的试验人群和实际需求人群也不一致——试验人群是12-26岁年轻女性,实际有需求的则更可能是风险感知更高的20-45岁成年女性。
出于证据不充分和公共卫生层面的考虑,WHO并没有关于推荐全程接种完二价或四价之后再重复接种九价的建议。也就是既没有“推荐”的建议,也没有“不推荐”的建议。
图源于网络
然而2016年,为了解决在个人层面上(由医疗保健提供者或疫苗接种者)提出的问题,欧盟区多位学者联合发布了一份针对9-14岁女孩(EPI目标人群)HPV疫苗应用过渡期的立场文件或声明:
九价既可用于完成此前未完成接种程序的方案(方案B和C),也可考虑用于之前已完成接种程序的情况(方案A和D),以扩大覆盖面。(ps:该立场文件仅作为过渡期参考,不能替代各国免疫规划)
针对9-14岁女孩的A、D方案,再次接种的九价均为2针程序,两个方案分别为:
方案A:0-6程序全程接种完2/4价后,间隔6个月后再进行2剂次九价接种;
方案D:先使用2/4价按照0-2-6月程序完成全程接种,然后在第12个月和第18个月使用九价完成2剂次接种。(该情况适用于9-14岁未采用“两针法”的情况)
“不能”的意见或将给政府项目带来隐忧
从目前来看,“暂不推荐”的建议表面上隔离了二价和九价间的联系,实际上也已经把接种门诊推到一些有诉求的受种群体的对立面,更不用提“不能”。
尽管疾控系的言论已经够谨慎了,但“不推荐”三个字可能已经给已经将二价纳入EPI、未来计划将二价纳入EPI的地区广泛实施消除宫颈癌战略埋下了不小的隐患——家长可能会为此犹豫而不参与政府惠民项目,接种门诊也需要面对更多的咨询和答疑工作量……
而这,又恰恰属于公共卫生层面需要考虑的范畴,这似乎也与前面出于公共卫生层面考虑给出的“不推荐”建议背道而驰。
因此,疾控体系是否应当在契合公共卫生角度的情况下,以发展的思维调整既往保守的建议?
参考资料:
Obstet Gynecol. 2020 Aug;136(2):e15-e21.
Vaccine. 2015 Nov 27;33(48):6855-64.
Virology. 2004 Jun 20;324(1):17-27.
Vaccine. 2018 November 12; 36(46): 7017–7024.
Vaccine. 2016 Feb 3;34(6):757-61.
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
疫苗
100 项与 新冠疫苗 (迈科康生物) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 新型冠状病毒感染 | 临床前 | 中国 |  成都迈科康生物科技有限公司初创企业 成都迈科康生物科技有限公司初创企业 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用