癌症治疗的魔法子弹——ADC从概念到临床的发展旅程
7月10日,BeiGene和DualityBio宣布达成一项协议,BeiGene将获得一种针对选定实体瘤患者的研究性ADC疗法的全球临床和商业许可的独家选择权。 DualityBio将继续进行临床前研究活动,并支持研究新药的上市申请,而BeiGene在行使其选择权后将持有全球临床,制造和商业权利。根据协议条款,DualityBio将收到一笔预付款,并可能根据某些开发,监管和商业里程碑获得额外付款,总额高达13亿美元,外加分层版税。合作旨在加速该资产的开发,并为全球患者带来更多的突破性ADC药物。
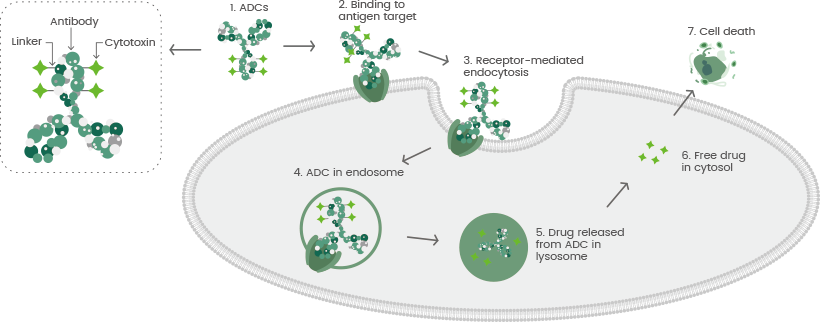
抗体偶联药物(ADC)是一类被设计为用于癌症靶向治疗的生物药品。与传统化疗不同,ADC旨在靶向并杀死肿瘤细胞,同时减少健康细胞的耗损。在智慧芽新药情报库中,已有1163种药物属于ADC,分布在多种靶点。要获取关于正在开发的ADC药物的最新信息,只需点击下面的图片注册免费访问新药情报库的海量数据。
ADCs的概念源于1900年Paul Ehrlich的工作。他设想了一种像“神奇子弹”一样的药物,可以选择性地将有毒剂量输送到微生物或肿瘤细胞。
第一次成功的ADC临床试验发生在1983年,使用了与长春新碱结合的抗癌胚抗原抗体。在1990年代,第一代ADCs使用鼠源性抗体作为骨干。然而,它们在人体循环中的连接剂是不稳定的,ADCs的半衰期也很短。
2000年,FDA批准了第一个ADC:吉姆杜沙胺奥佐加霉素(商品名:Mylotarg),针对CD33阳性急性髓系白血病。其使用卡立霉素作为细胞毒性荷载,并通过水合肼连接剂进行链接。然而,由于对肝脏的严重毒性和疗效de 缺乏,在2010年被撤回。2017年,以较低的剂量和不同的使用方法重新引入。
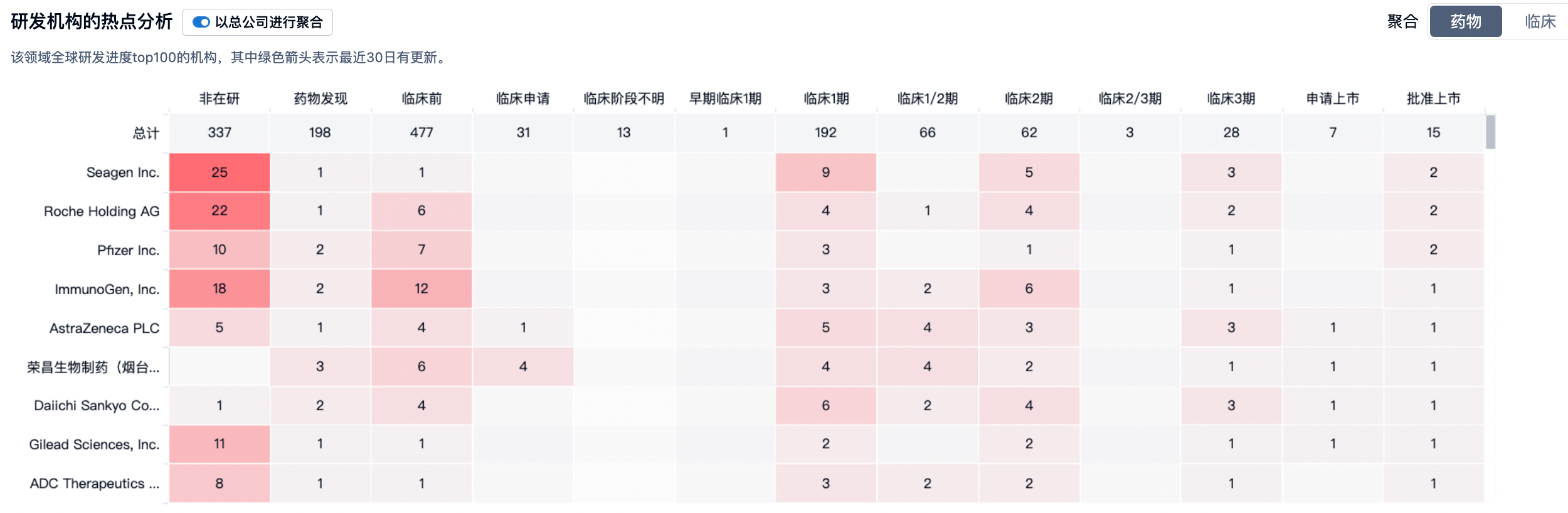
从那时起,已有几种针对霍奇金淋巴瘤、乳腺癌、泌尿道癌和多发性骨髓瘤等各种癌症的ADC获得了批准。这些ADC使用了不同的抗体、连接剂和载荷,以获得更好的效果和安全性。例子包括贝伦珠单抗(Adcetris)、曲妥珠单抗乙酰化肽(Kadcyla)、伊诺图珠单抗奥佐加霉素(Besponsa),和贝瑞坦曲单抗(Blenrep)。新药情报库的竞争格局分析提供了基于全球ADC药物最高阶段的前100家机构的热度图:
在快速发展的癌症研究领域,抗体偶联药物(ADCs)的开发带来了一系列独特的挑战。首先,目标抗原的选择至关重要。理想情况下,这个抗原应该在肿瘤细胞上高度表达,并在正常细胞上最小程度地表达,以减轻毒性风险。这个抗原还应该在抗体结合后能够实现内化,以直接促进药物的释放,并且足够稳定,不会受到肿瘤微环境或治疗措施的影响。
接下来,抗体工程至关重要。它需要对目标抗原具有高特异性和亲和力,并具有良好的药代动力学和生物分布。这些抗体还应该展示最小的不良反应,如免疫原性、细胞因子释放或补体活化。此外,为了实现最佳的连接器和药物负载附着,可能需要一个合适的结合位点和药物与抗体比例(DAR)。
连接器设计也存在挑战。它需要在血液中的稳定性和肿瘤细胞中的可切割性之间找到平衡,以允许活性药物释放。连接器的长度、灵活性、毒性和免疫原性的考虑对ADCs形成和功能至关重要。
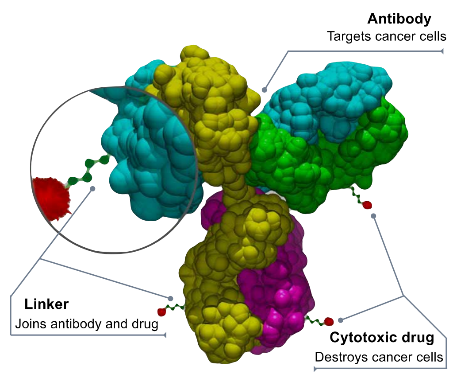
药效物质的选择是另一个需要关注的问题。这些药效物质应该对肿瘤细胞具有强烈和有效的作用,同时对非目标毒性、耐药性最小,并在此类偶联和输送中具有最佳的溶解性。
制造过程也是一个额外的挑战。ADCs的生产是一个复杂且昂贵的过程,需要对偶联反应、纯化、配方和储存等各个方面严格控制。质量会受到聚合、降解、异质性、杂质和稳定性等因素的影响。
最后,由于剂量选择、病人选择、生物标记鉴定、安全监测和效果评估的要求,ADCs的临床研发是具有挑战性的。替代标记、组合策略和上市后研究,也构成了重大的障碍。
尽管有这些强大阻碍,抗体药物偶联物(ADCs)的潜在益处是巨大的,使其开发成为当代癌症研究和治疗的重要元素。目前,热切探索ADC发展的新方向。一个关键的关注领域是利用新的目标抗原,如细胞表面受体、酶、运输蛋白或糖蛋白,为选择性靶向肿瘤细胞及其微环境提供新的机会。
人们也在努力提高药物抗体的比例(DAR),期望通过每个抗体传递更多的负载分子来增强ADC的效能。这可能通过使用特定位置的偶联方法、多价抗体或甚至基于聚合物的载体来实现。
通过使用更小的抗体片段、双特异性抗体或工程抗体来增加抗体对实体瘤的渗透,是另一个引人入胜的视角,这可能有助于在肿瘤组织内更好地分布ADC。
寻找对抗ADC所赋予的抗性机制的策略,如降低抗原表达水平或负载抗性,也在进行中。采用组合治疗、替代负载或新型连接器可能在这个领域具有决定性的作用。
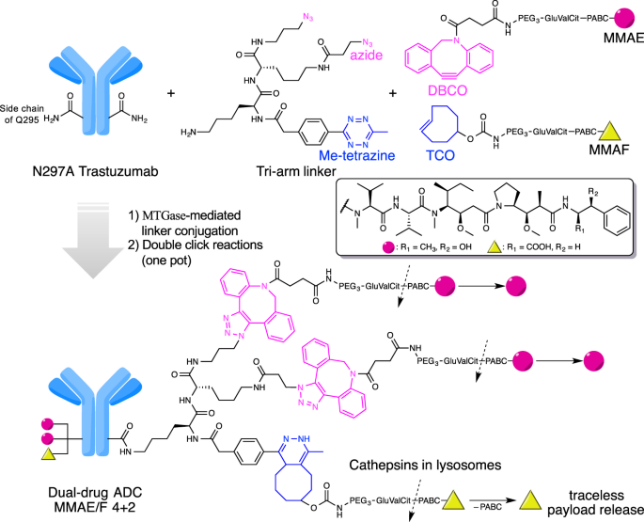
提高肿瘤细胞对ADC(抗体偶联药物)的吸收和处理效率是一种有希望的途径,其中pH敏感连接剂,酶响应连接剂或自溶连接剂可能导致肿瘤细胞内更好的药物载体激活。与非目标药物载体的暴露进行抗衡是一个关键问题,人们正在考虑使用掩蔽药物载体,前药药物载体或定向输送系统等方法来减轻与ADCs相关的系统毒性和不良反应。最后,使用非细胞毒性药物载体,如免疫调节剂,基因沉默剂或放射性配体,为探索可能引入的新的ADC作用模式开辟了令人兴奋的领域。尽管存在复杂性和多重挑战,但ADCs的未来看起来很有希望,具有可观的潜力来改善癌症治疗结果。