KRAS G12C抑制剂走向市场:游戏已开始
最近,阿斯利康的研究人员发现了一种新的药物候选物AZD4747,这种药物在治疗带有KRAS G12C突变的肿瘤方面显示出前景。这种突变限制了GTP酶KRAS将GTP水解为不活跃的GDP结合状态的能力,导致下游信号通路的持续激活。KRAS G12C突变在肺腺癌中的发生频率高,而在胰腺和结肠腺癌中的发生频率较低。
KRAS基因突变在许多人类癌症中都很普遍,是最常突变的癌基因之一。大约95%的胰腺癌、40%的结直肠癌、25%的非小细胞肺癌,以及甲状腺、卵巢、膀胱、红斑狼疮、乳腺、肝脏等其他类型的癌症中都检测到了KRAS基因突变。
KRAS阳性癌症的全球发病率正在显著增加。病例数从2016年的180万增加到2020年的超过200万。预计到2025年病例将超过228万,到2030年将超过256万。截至2023年7月10日,根据智慧芽新药情报库,在过去的30天里,新增了4种针对KRAS的靶向药物,6项新的临床试验和55项新的专利。想获得关于开发中的KRAS靶向药物的最新更新,只需点击下方图片即可免费注册获得新药情报库的最新情报。
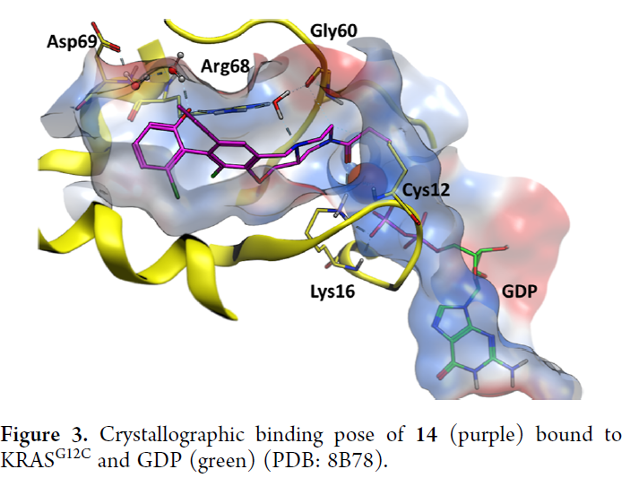
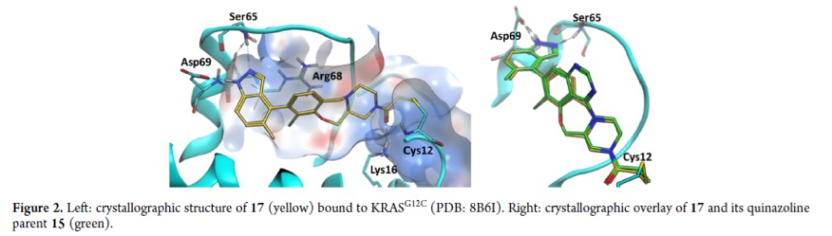
阿斯利康团队使用基于结构的药物设计方法来识别AZD4747,这是一种对KRAS G12C有高度的潜力和选择性的抑制剂。这个药物候选物已经针对效能和药物代谢和药效学(DMPK)特性进行了优化。研究员使用与非活性KRAS G12C结合的AZD4747的晶体结构来确定其结合方式。氯苯酚开关Ⅱ群体与Arg68相互作用,并通过水分子与Asp69产生相互作用。C8乙炔基暴露在溶剂中,而八氮杂环则以一种方式呈现一个sp3杂化的N哌嗪原子与一个桥接水分子。这个中性的N原子稳定了水分子,该水分子本身则通过与Arg68和Gly60的相互作用进一步稳定为四面体几何形状。
AZD4747与Cys12形成共价键,并与Lys16相互作用。它对KRAS G12C中的半胱氨酸的反应高度选择性,优于其他含半胱氨酸的蛋白质,并在带有导致小鼠异种移植病模型强烈肿瘤退化的G12C突变的癌细胞中,展现出选择性的抗增殖表型。
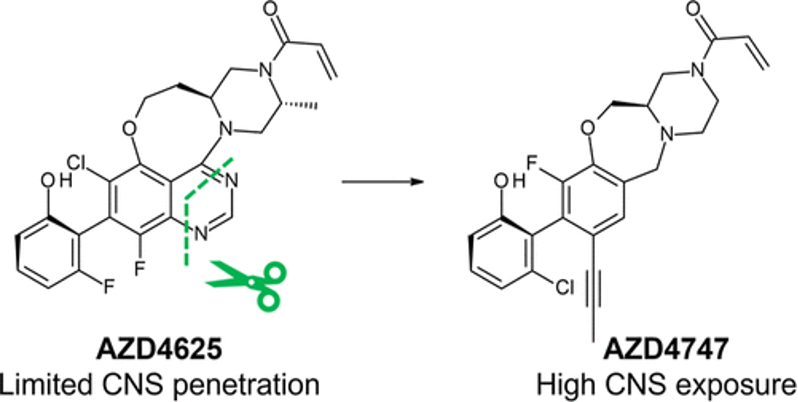
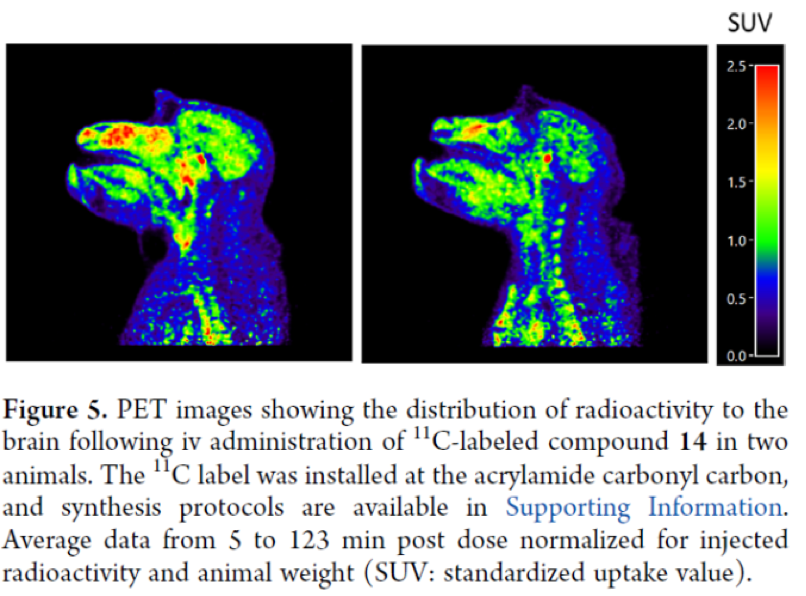
研究者还发现,AZD4747表现出理想的分子属性,以在中枢神经系统(CNS)中实现药物暴露,并且其对人类P-gp和BCRP的体外排泄潜力已大幅降低。狗和猴子的平均体内 Kpu,u 分别为0.7和1.6,这表明这些物种中的中枢神经系统可用性相对未受主动排泄影响。基于这些结果,建议AZD4747能够穿越人类完整的血脑屏障,从而显示出治疗中枢神经系统转移病人的潜力。
开发KRAS G12C抑制剂的竞争非常激烈,有多种药物正在临床试验中。首个获得FDA批准的KRAS G12C抑制剂是sotorasib,于2021年5月草案加快批准,用于治疗经过前期治疗并具有KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者。该批准基于CodeBreaK 100试验的结果,该试验显示sotorasib在36%的患者中缩小了肿瘤,反应的中位持续时间为10个月。sotorasib也正在与免疫疗法、化疗或针对NSCLC和其他KRAS G12C癌症的靶向疗法一起进行临床试验。
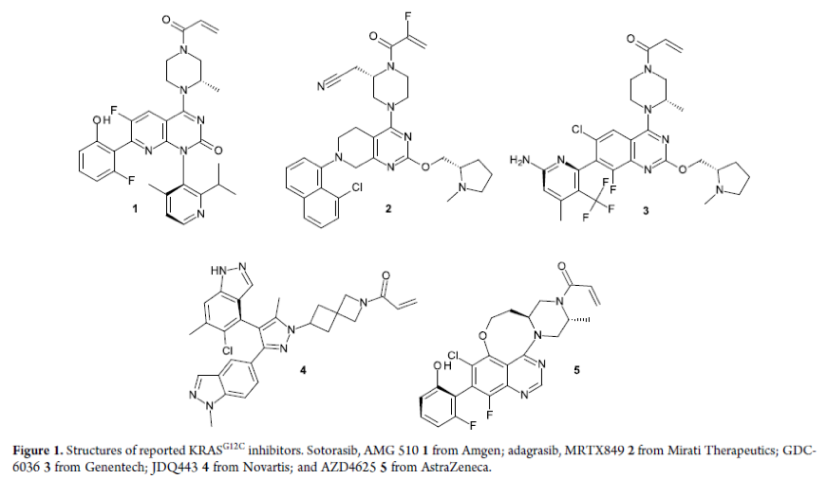
目前,像AMG510和MRTX849这样的药物候选已经获得批准,世界各地还有许多其他抑制剂处于临床阶段。除了Genentech的GDC-6036、Novartis的JDQ443和AstraZeneca的AZD4625的已公布结构外,还有Eli Lilly的LY3537982、Boehringer Ingelheim的BI 1823911和InventisBio的D-1553的临床试验正在进行中,其结构尚未公开。由于毒性,早期分子Eli Lilly的LY3499446和Johnson & Johnson的JNJ-74699157已被停止。正在积极开发的其他KRAS亚型包括G12D、G12V和G13D。
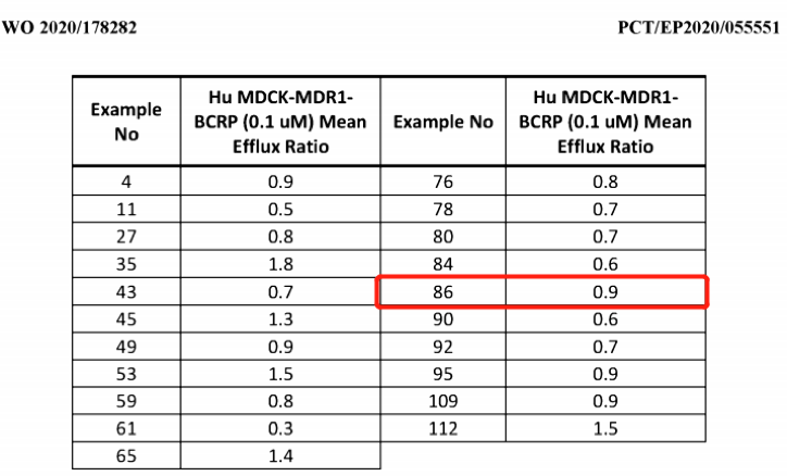
使用关键词KRAS和AstraZeneca在Synapse专利数据库中搜索,找到四项WO专利:WO2020178282,WO2019215203,WO2019110751和WO2018206539。最后三项专利与能穿透脑血屏障的KRAS抑制剂可能相关性不大。WO2020178282的85和86实施例提到了AZD4747化合物,这是两种对映体的消旋混合物。只有86化合物的活性和排泄数据被测量,这表明它代表 AZD4747。MDCK_MDR1_BCRP细胞表达两种能将化合物输送穿过脑血屏障的排泄泵。在这个分析中,排泄比率≤2的化合物有可能作为能穿透脑血屏障的药物。
具有这种可能性的化合物如下所示,包括根据其他评估确定具有均衡药物属性的86化合物。WO2020178282的最早优先权日期是2019年3月5日。该专利于2020年3月3日提出,于2020年9月10日公布。中国公布的CN113508118A预计到期日期为2040年3月3日。
KRAS G12C抑制剂sotorasib在KRAS突变的非小细胞肺癌(NSCLC)的临床试验中显示出了令人充满希望的抗肿瘤活性。然而,这些试验排除了中枢神经系统(CNS)转移的患者,限制了对sotorasib渗透到大脑的能力的数据。Sabari等人的回顾性分析以及对临床前数据的回顾表明,也针对KRAS G12C的实验性药物adagrasib可能具有中枢神经系统活性。
在临床前的脑膜炎模型中,adagrasib渗入到脑脊液,导致肿瘤退化和生存期延长。在两名未经治疗的脑膜炎的非小细胞肺癌患者中,adagrasib在脑脊液中的浓度超过了抑制肿瘤生长所需的IC50值。这两名患者都有相应的脑转移病灶,这表明adagrasib可能具有针对脑转移的临床活性。然而,一些意见认为,仅来自两名患者的有限数据是不够的,因为治疗和预防脑转移对患者的预后至关重要。
这些发现支持进一步研究adagrasib在有未经治疗的脑转移的KRAS G12C NSCLC患者中的作用。一个I/II期临床试验(NCT03785249)正在招募822名患有KRAS G12C突变的晚期实体瘤患者,以评估adagrasib的安全性、耐受性、药物水平、分子效应和临床活性,预计将在2024年9月发布结果。
在另一种实验性KRAS G12C抑制剂D-1553的早期临床试验中,三名基线脑转移患者中的一名达到了部分反应,客观反应率为17%。在这名患者中,20mm以上的转移病灶缩小了近一半。其他两名患者的疾病稳定,疾病控制率为100%。
一些脑转移的癌症患者可能存在血脑屏障的损害,即使在临床前模型中没有穿透到大脑,也可能允许某些化合物穿透到大脑。正在开发adagrasib的阿斯利康公司已经成功开发出其他能渗透到大脑的药物,这可能有利于这些患者。临床前和有限的临床数据暗示,KRAS G12C抑制剂adagrasib和D-1553可能对非小细胞肺癌中的脑转移有活性。正在进行的临床试验将提供更为充实的证据,证明它们在这个关键的患者群体中的效果。




