罗氏新一代C5补体单抗crovalimab在美申报上市,治疗PNH
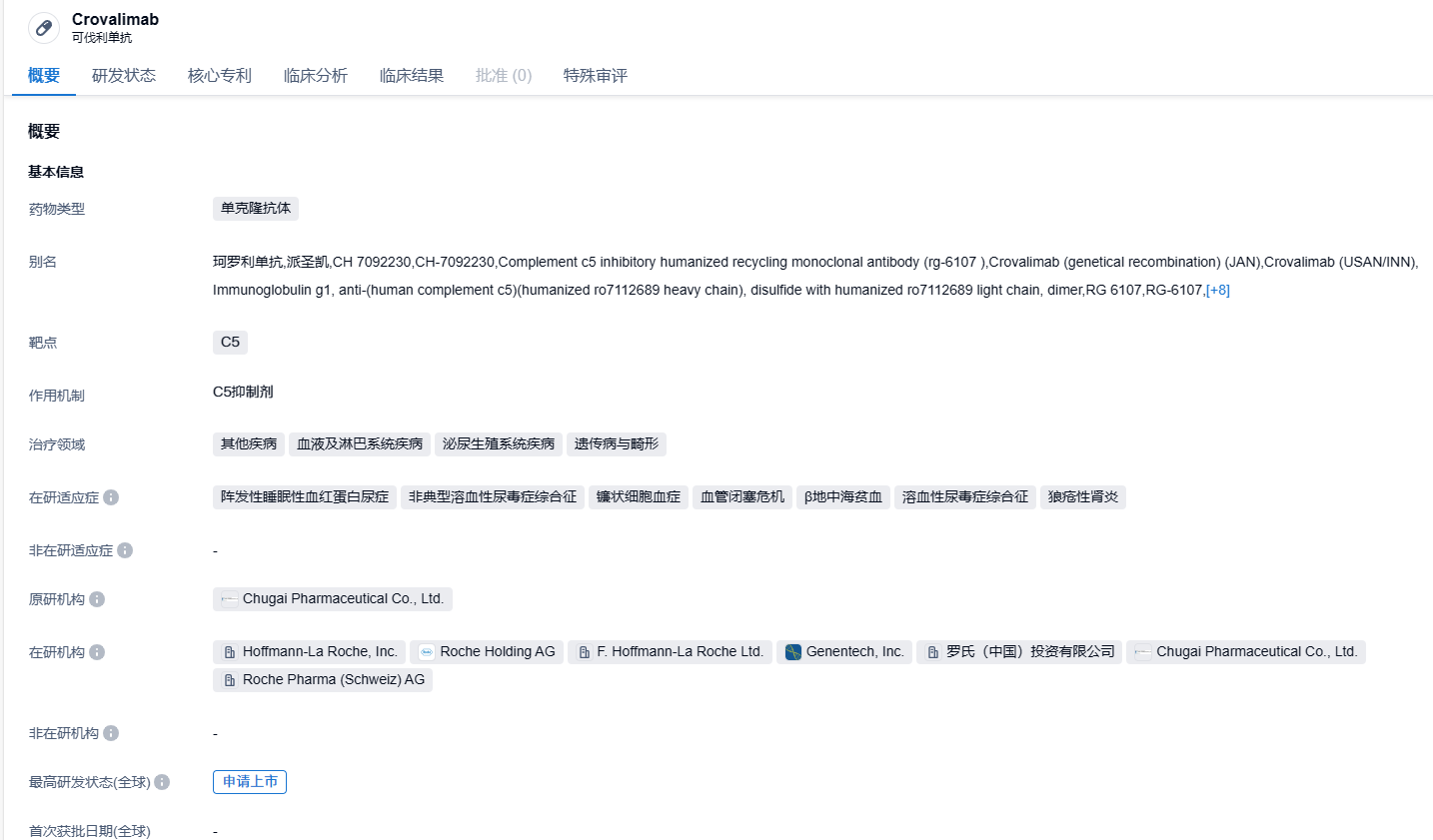
2023年9月6日,罗氏旗下基因泰克宣布,美国FDA已受理该公司新型补体C5单克隆抗体Crovalimab(珂罗利单抗)的生物制品许可申请(BLA),用于治疗突阵发性睡眠性血红蛋白尿(PNH)。如果获得批准,Crovalimab将成为首款治疗PNH的每月仅需用药一次的皮下制剂,并且患者可自行给药。
Crovalimab(珂罗利单抗)是罗氏开发的一种通过连续单克隆抗体回收技术(Smart-Ig)工程化改造的新一代C5抑制剂,可以阻断补体C5裂解为C5a和C5b,有望抑制补体活化。该药物结合了等电点、新生儿Fc受体(FcRn)和pH依赖性亲和性技术,使其不仅能够与C5高效结合,使内皮细胞对与C5结合crovalimab的吸收增强,同时还可以使新生儿Fc受体介导的crovalimab高效再循环。2022年8月,珂罗利单抗注射液在国内的上市申请已获得受理,并被纳入优先审批品种,拟用于治疗PNH。除PNH,目前Crovalimab还被开发用于非典型溶血性尿毒症(aHUS)、镰状细胞病和其他补体介导的疾病。
此次申报使基于两项III期研究(COMMODORE 1和COMMODORE 2)的积极结果。COMMODORE 1是一项多中心、随机、开放标签、阳性对照的III期临床试验,评估了珂罗利单抗替代依库珠单抗或ravulizumab治疗的安全性。COMMODORE 2是一项多中心、随机、开放标签、阳性对照的III期临床试验,评估了珂罗利单抗(每4周1次,皮下注射)对比依库珠单抗(每2周1次,静脉注射)治疗未接受过补体抑制剂治疗的PNH患者的疗效和安全性。结果显示,在COMMODORE 1研究中,患者从接受依库珠单抗或ravulizumab治疗转为接受珂罗利单抗治疗后有所获益且风险较低;在COMMODORE 2研究中,珂罗利单抗非劣效于依库珠单抗。
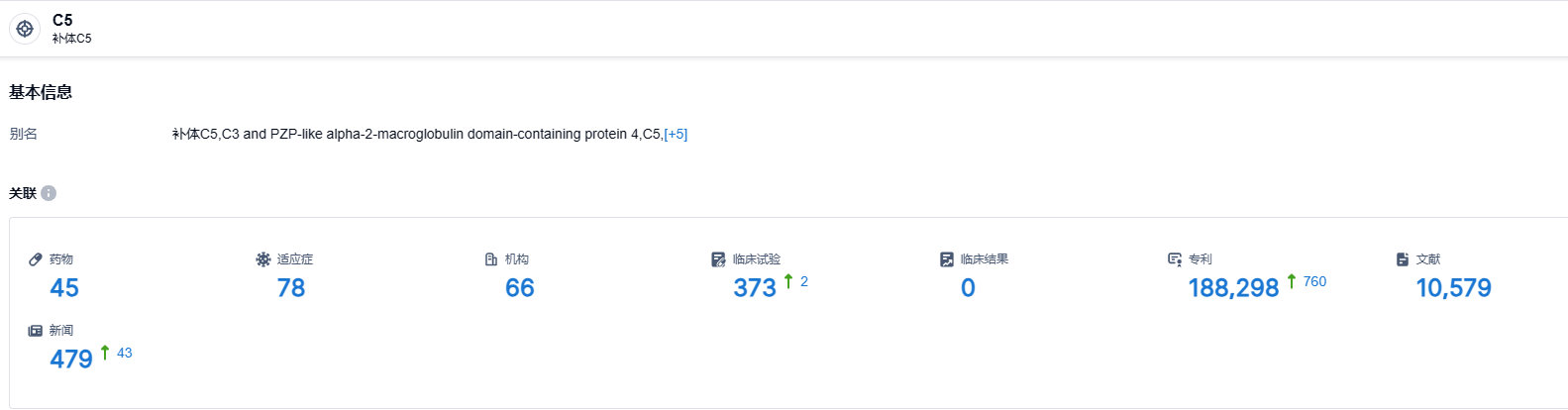
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 C5 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年9月7日,C5 靶点共有在研药物45个,包含的适应症有78种,在研机构66家,涉及相关的临床试验373件,专利多达188298件……补体蛋白C5是非常成功的一个补体药物靶点,首款药物Soliris(依库珠单抗)2020年销售额高达40.64亿美元,2022年销售额为37.62亿美元。Crovalimab作为每月仅需用药一次的皮下制剂,并且患者可自行给药,极大的方便了患者使用,具有成为重磅炸弹药物的潜力。