辉瑞CGRP受体拮抗剂zavegepant鼻喷雾剂启动亚洲3期临床,针对偏头痛
2023年8月10日,中国药物临床试验登记与信息公示平台官网显示,辉瑞(Pfizer)已启动一项在亚洲成人中评估zavegepant鼻喷雾剂用于偏头痛急性期治疗的疗效和安全性的3期研究。该试验将在全球共计64家研究机构开展,计划在国际入组1400人,在中国入组980人。
zavegepant是是Biohaven Pharmaceutica开发的第三代高亲和力、高选择性的小分子CGRP受体拮抗剂鼻内喷剂,目前正在开发鼻喷雾剂和口服制剂两个剂型。CGRP全名是降钙素基因相关肽,是一种血管舒张神经肽,其释放水平在偏头痛发作时明显增高,而且与头痛程度正相关。通过可逆性地阻断CGRP受体,从而抑制CGRP神经肽的生物活性,可以实现缓解与预防偏头痛发作。2022年10月,辉瑞宣布已完成对Biohaven公司的收购,交易总额约为116亿美元。2023年3月10日,辉瑞宣布FDA已批准zavegepant(商品名:ZAVZPRET)上市,用于有或无先兆的成人偏头痛急性治疗。ZAVZPRET是首款也是唯一一款获批上市的降钙素基因相关肽(CGRP)受体拮抗剂鼻喷雾剂。
此次辉瑞在中国启动的是一项3期国际多中心、随机、双盲、安慰剂对照、平行组研究,试验目的是通过给药后2小时无疼痛以及无最困扰症状,评估zavegepant相比安慰剂用于亚洲成人偏头痛(有或无先兆)急性期治疗的疗效和安全性。该试验主要终点指标是给药后2小时疼痛强度为无(无疼痛)的受试者百分比,以及给药前报告了最困扰症状(MBS),并在给药后2小时无此症状的受试者百分比。
FDA批准zavegepant上市是基于两项双盲安慰剂对照研究(NCT04571060, NCT03872453)的数据,该研究包括至少1年偏头痛病史(伴有或不伴有先兆)的成年人,如果未经治疗,偏头痛发作平均持续4至72小时。 两项研究的结果显示,在2小时内,Zavzpret治疗在疼痛缓解和大多数烦人症状(恶心、畏光、恐音)缓解的主要终点上优于安慰剂。
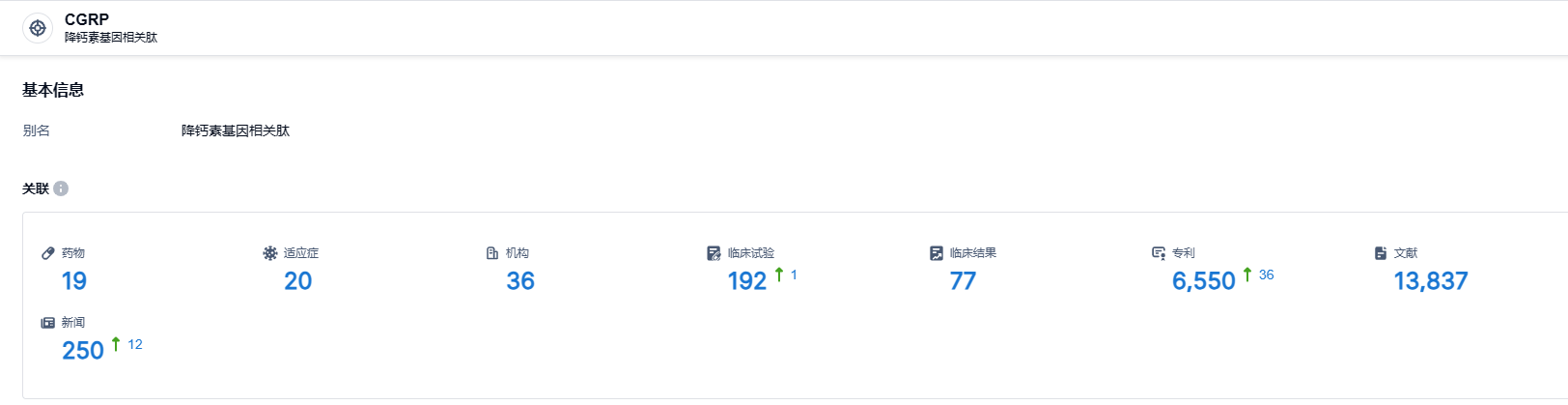
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 CGRP 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年8月11日,CGRP靶点共有在研药物19个,包含的适应症有20种,在研机构36家,涉及相关的临床试验192件,临床试验结果77件,专利多达6550件……据估计,全球约有13亿偏头痛患者,其中女性患病率是男性的2~3倍,存在极大的市场需求。CGRP/CGRPR类靶向药物市场潜力巨大,整体市场有望突破百亿美元,辉瑞zavegepant疗效确切,将在偏头痛市场占据一席之地。