科伦博泰TROP2 ADC疗法SKB264 3期临床试验达主要终点,治疗三阴性乳腺癌!
2023年8月14日,科伦博泰宣布,其靶向TROP2-ADC产品SKB264(MK-2870)用于治疗既往经二线及以上标准治疗的不可手术切除的局部晚期、复发或转移性三阴性乳腺癌(TNBC)患者的3期临床试验达到主要研究终点,即独立审查委员会(IRC)评估的无进展生存期(PFS)。在预先设定的期中分析中,与接受标准化疗的对照组相比,SKB264 (MK-2870)在无进展生存期方面有统计学上的显著改善。
SKB264是由科伦博泰拥有自主知识产权的靶向TROP2的人源化单克隆抗体、可酶促裂解的Linker和新型拓扑异构酶I抑制剂组合而成的新一代抗体偶联药物(ADC),结合了单抗对肿瘤细胞表面靶抗原的特异性和细胞毒性药物的高效性。此前,SKB264已获得国家药品监督管理局(NMPA)药品审评中心(CDE)突破性疗法认定,用于治疗局部晚期或转移性三阴乳腺癌和EGFR-TKI治疗失败的局部晚期或转移性EGFR突变非小细胞肺癌。 在国外,科伦博泰已有偿独家许可默沙东在大中华区(包括中国大陆、香港、澳门和台湾)以外开发、使用、制造及商业化SKB264(MK-2870),海外临床研究正在美国、加拿大、澳大利亚、法国、比利时和波兰有序开展或准备开展中。 多项全球多中心注册性临床研究在筹备中。
本次达到主要终点的该试验是SKB264在中国的首个注册3期研究,为SKB264对比研究者选择方案用于治疗既往经二线及以上标准治疗的不可手术切除的局部晚期、复发或转移性三阴性乳腺癌患者的随机、对照、开放性、多中心3期临床试验。据悉,科伦博泰于近期召开了独立数据监查委员会(IDMC)会议,对SKB264的3期临床试验期中分析数据进行了审阅,IDMC决议表明该研究达到了主要研究终点独立评审委员(IRC)评估的无进展生存期(PFS)。在预先设定的期中分析中,与对照标准化疗组相比,SKB264的无进展生存期具有统计学意义上的显著改善。根据期中分析结果,科伦博泰计划就提交SKB264的新药申请(NDA)事宜与中国国家药监局药品审评中心(CDE)进行沟通。
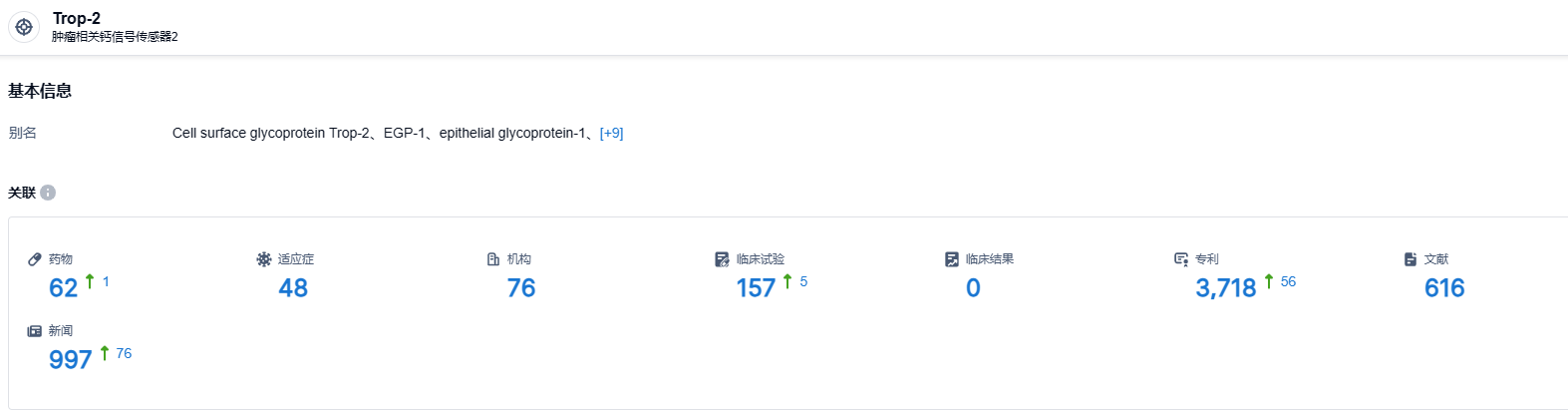
根据智慧芽新药情报库所披露的信息 (点击下方图片直达TROP2靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年8月15日,TROP2 靶点共有在研药物62个,包含的适应症有48种,在研机构76家,涉及相关的临床试验157件,专利多达3718件……SKB264是科伦博泰拥有自主知识产权的核心产品之一,此次治疗三阴性乳腺癌的3期临床试验达主要终点,有望助力该药成功上市。