福沃药业第三代口服SERD 新药FWD1802启动1期临床,治疗乳腺癌
2023年9月15日,深圳福沃药业有限公司(以下简称“福沃药业”)宣布,其自主研发的第三代口服选择性雌激素受体降解剂(SERD)FWD1802用于ER+/HER2-不可切除的局部晚期或转移性乳腺癌患者的1期临床研究成功完成第一例受试者给药。FWD1802已在美国和中国获批开展临床试验。
FWD1802是福沃药业开发的一款第三代口服特异性雌激素受体降解剂,SERD是雌激素受体(ER)的竞争性拮抗剂,可以引起ER蛋白构象改变并降解。FWD1802兼具ER降解和拮抗的双重作用,具有比同类药物更强的体内、体外药效,并且对于上一代用药后产生的ER突变同样有效。这使得FWD1802不止可以成为上一代SERD的后线治疗,更有潜力替代上一代SERD,成为新的标准治疗。同时,FWD1802展示出了良好的体内生物利用度,在临床上患者可以采用更加便捷的口服用药。美国FDA于2023年3月23日许可FWD1802临床试验申报(IND),中国国家药品监督管理局(NMPA)于2023年7月5日签发《药物临床试验批准通知书》(通知书编号: 2023LP01288、2023LP01289、2023LP01290),同意开展单药在ER+/HER2-不可切除的局部晚期或转移性乳腺癌受试者中的临床试验。
SERD是一种小分子,它们通过与癌细胞表面的雌激素受体(ER)相结合,降低雌激素受体的稳定性,诱导它们被细胞正常的蛋白降解机制降解,从而降低雌激素受体水平,抑制癌细胞的生长。与抑制雌激素活性的调节剂不同,SERD理论上通过介导雌激素受体的降解,能够更为全面地抑制雌激素受体的功能,并且可能解决雌激素受体突变产生的耐药性。目前有多款SERD新药正在临床开发中,例如卫材的艾拉司群(elacestrant)已向FDA递交了的新药上市申请,如若获批,该药将成为全球一个上市的口服SERD药物。
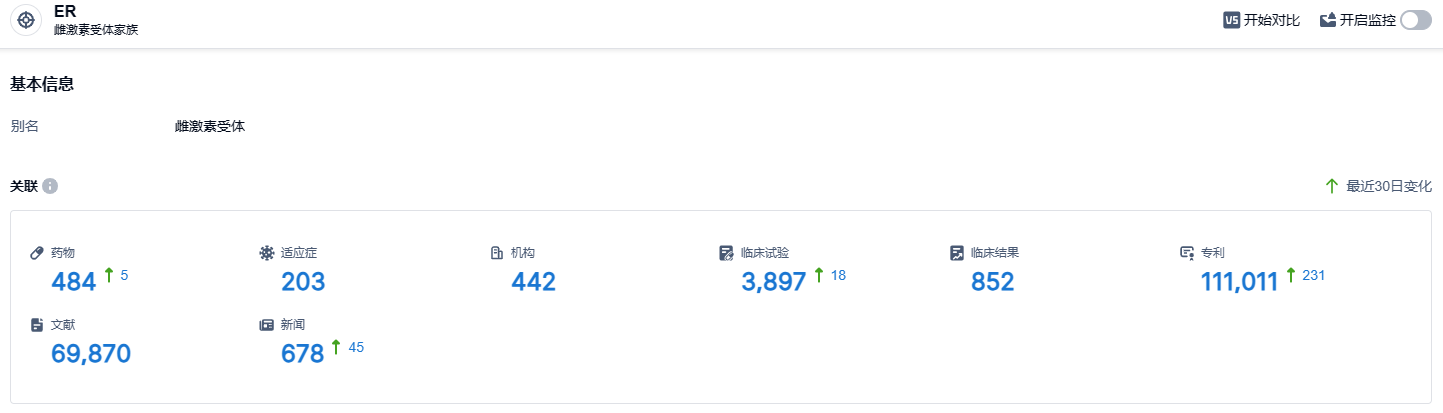
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达ER 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年9月16日,ER靶点共有在研药物484个,包含的适应症有203种,在研机构442家,涉及相关的临床试验3897件,专利多达111011件……福沃药业专注于抗肿瘤领域新一代靶向治疗创新药物研发和产业化。建立了包括多个国家1类创新药在内的产品管线,适应症覆盖前三大实体瘤和自体免疫疾病,其中2个产品已进入中美国际临床阶段,分别为FWD1509和FWD1802。期待FWD1802这款口服SERD新药能够开发顺利,为乳腺癌患者带来新的治疗选择。