预约演示
最新资讯
德昇济医药HER2/CD47双抗D3L-001在中国获批临床,针对晚期实体瘤
2023-09-05
阅读时长 2分钟
2023年9月4日,中国国家药监局药品审评中心(CDE)官网公示,德昇济医药申请的1类新药HER2/CD47双特异性抗体D3L-001获得临床试验默示许可,拟开发用于HER2阳性晚期实体瘤。公开资料显示,这是一款靶向HER2/CD47的双特异性抗体,此前已在美国获批临床。
D3L-001是德昇济医药开发的一款靶向HER2/CD47的双特异性抗体,能够通过HER2的高亲和活性优先与肿瘤细胞结合,降低其与正常组织的结合,从而减少CD47靶点潜在的血液毒性,并能使抗体依赖的细胞毒性作用(ADCC)和抗体依赖的细胞吞噬作用(ADCP)协同作用发挥到最大程度。
在2023年美国癌症研究协会(AACR)年会上,德昇济医药展示了D3L-001的临床前研究数据。据该公司早前新闻稿介绍,D3L-001与已经处于临床研究阶段的D3S-001以及该公司后续研发管线产品之间存在协同和联合的潜力。
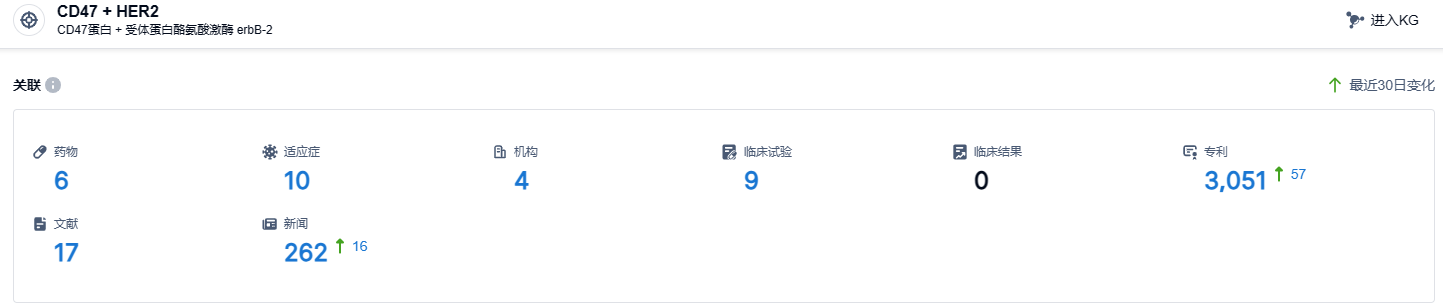
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 HER2/CD47 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年9月5日,HER2/CD47靶点共有在研药物6个,包含的适应症有10种,在研机构4家,涉及相关的临床试验9件,专利多达3051件……德昇济医药目前已建立包括6款自主研发的候选新药产品管线,其中小分子药物涉及:KRAS G12C选择性抑制剂D3S-001、ERK1/2选择性抑制剂D3S-002、D3S-003;大分子涉及:HER2/CD47双抗D3L-001、D3L-002、D3L-003。目前,D3S-001、D3S-002、D3L-001已经开展临床试验,均是针对恶性肿瘤,期待这些新药的后续表现。

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
继续阅读
返回博客首页 →最新资讯
阅读时长 2分钟
阿斯利康BTK抑制剂阿可替尼胶囊新适应症在国内获批上市,治疗血液肿瘤
2023-09-02
阿可替尼是阿斯利康自主开发的第二代选择性BTK抑制剂,通过与BTK共价结合抑制其活性。在B细胞中,BTK信号导致B细胞增殖、转运、趋化和粘附所需的途径激活。
最新资讯
阅读时长 2分钟
君实生物抗PD-1/VEGF双抗JS207获批临床,针对晚期恶性肿瘤
2023-09-02
中国国家药监局药品审评中心(CDE)官网公示,君实生物1类新药抗PD-1/VEGF双抗注射用JS207获得临床试验默示许可,拟开发用于治疗晚期恶性肿瘤。
最新资讯
阅读时长 2分钟
创胜集团启动CLDN 18.2单抗TST001全球III期临床,联合治疗胃癌
2023-09-02
Osemitamab (TST001) 是创胜集团开发的一种高亲和力的靶向Claudin18.2的人源化单克隆抗体,具有增强的抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)活性。
最新资讯
阅读时长 2分钟
再鼎医药靶向HER2新药马吉妥昔单抗注射液在国内获批,治疗乳腺癌!
2023-09-02
马吉妥昔单抗(margetuximab)是再鼎医药从MacroGenics公司引进的一种作用于HER2的Fc优化型单克隆抗体,本次获批的适应症为用于转移性HER2阳性乳腺癌患者三线及以上治疗。
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。