Alector/GSk潜在FIC疗法latozinemab获FDA突破性疗法认定,治疗痴呆症
2023年2月8日,Alector Therapeutics公司和GSK宣布,美国FDA已授予在研抗体疗法latozinemab突破性疗法认定。
Latozinemab(AL001)是一种针对PGRN的单克隆抗体。PGRN是大脑内免疫反应的关键调节因子,与多种神经退行性疾病(包括FTD、阿尔茨海默病和帕金森病)相关。Latozinemab的作用机制涉及抑制SORT1,这是介导PGRN降解的受体,目的是提高患者的PGRN水平。它已经获得FDA授予的孤儿药资格、快速通道资格和突破性疗法认定。2021年7月,Alector公司与葛兰素史克(GSK)达成数额可达23亿美元的研发合作,其中包括联合开发AL001。
这一突破性疗法认定是基于名为INFRONT-2的2期临床试验结果。试验数据显示,latozinemab将患者血浆和脑脊液中PGRN水平恢复到年龄相当的健康志愿者的水平。同时,初步评估数据显示,与历史对照相比,latozinemab可能减缓患者的疾病进展。Latozinemab(AL001)是一种针对PGRN的单克隆抗体。PGRN是大脑内免疫反应的关键调节因子,与多种神经退行性疾病(包括FTD、阿尔茨海默病和帕金森病)相关。
2022年阿尔茨海默氏症和帕金森病会议上公布了latozinemab治疗具有 C9orf72 突变的FTD的12 个月INFRONT-2 II期临床结果(60 mg/kg q4w for 96 weeks)。公布的试验结果显示,latozinemab表现出良好的安全性和耐受性,并且迅速提高血浆和脑脊液(CSF)中的PGRN蛋白水平。接受latozinemab的患者,与匹配的历史对照组相比,临床症状进展速度减缓54%。
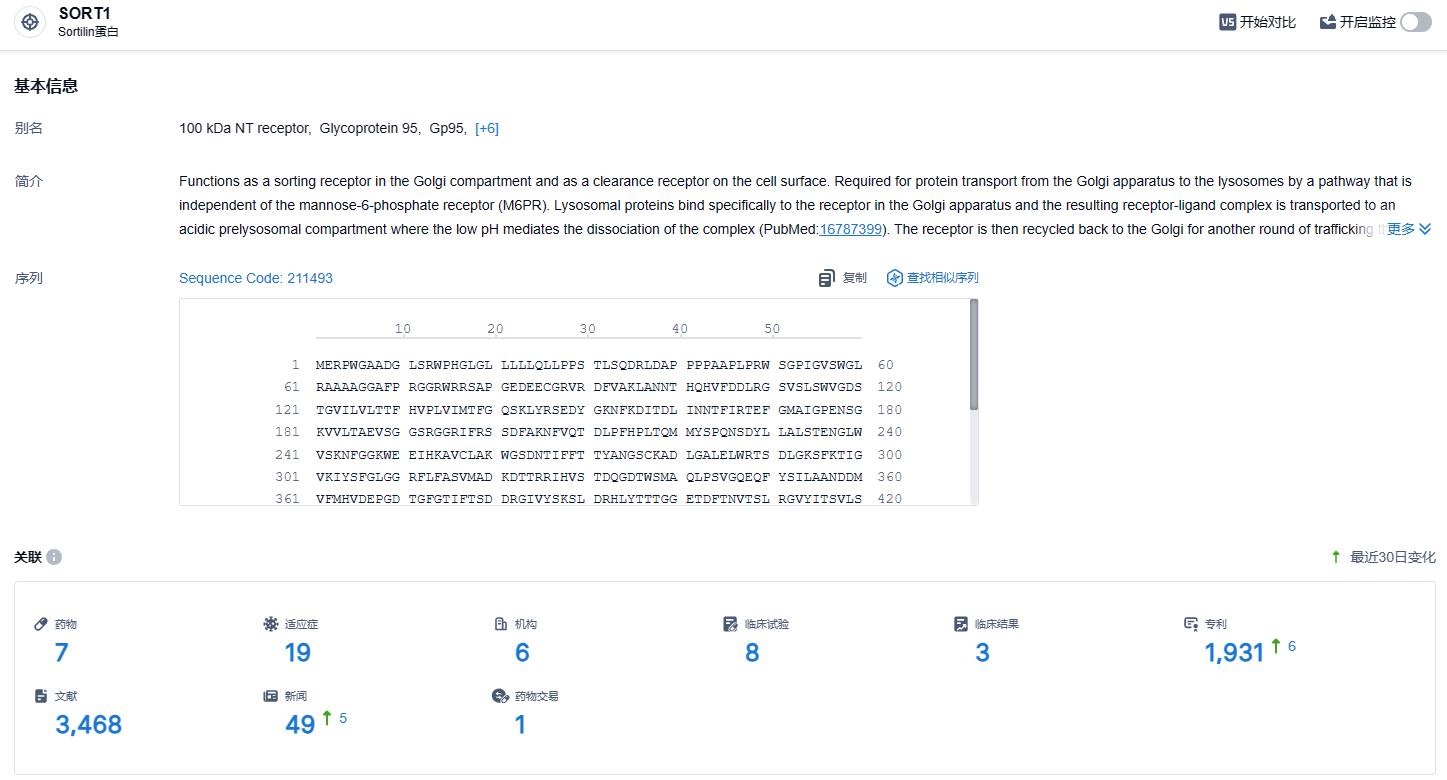
根据智慧芽新药情报库所披露的信息 (点击下方图片直达SORT1靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年2月19日,SORT1靶点共有在研药物7个,包含的适应症有19种,在研机构6家,涉及相关的临床试验8件,专利多达1931件……额颞叶痴呆(Frontotemporal dementia,FTD)是早发性(中年)痴呆的常见原因之一,会导致患者行为、语言和执行功能的损害,并且在65岁以下的患者中,发生率与阿尔茨海默病相似,患者缺少有效的治疗选择。期待latozinemab能够研发顺利。