预约演示
更新于:2025-05-07
LIGHT
更新于:2025-05-07
基本信息
别名 CD258、Herpes virus entry mediator ligand、Herpesvirus entry mediator ligand + [11] |
简介 Cytokine that binds to TNFRSF3/LTBR. Binding to the decoy receptor TNFRSF6B modulates its effects. Acts as a ligand for TNFRSF14/HVEM (PubMed:10754304, PubMed:9462508). Upon binding to TNFRSF14/HVEM, delivers costimulatory signals to T cells, leading to T cell proliferation and IFNG production (PubMed:10754304). |
关联
8
项与 LIGHT 相关的药物靶点 |
作用机制 LIGHT抑制剂 |
在研适应症 |
最高研发阶段临床2期 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
靶点 |
作用机制 LIGHT刺激剂 |
在研适应症 |
非在研适应症 |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
作用机制 LIGHT抑制剂 [+1] |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
10
项与 LIGHT 相关的临床试验ACTRN12623000845639
The Effect of Photobiomodulation with or without Hyperbaric Oxygen Therapy on Cognition in Adults with Mild and Moderate Cognitive Impairment
开始日期2023-09-04 |
申办/合作机构- |
ChiCTR2300074908
Clinical efficacy of Low-Level Red-Light on young children with myopic amblyopia
开始日期2023-08-20 |
申办/合作机构- |
CTRI/2023/07/055810
A split face interventional controlled trial to determine treatment efficacy of intense pulse light 690nm filter compared to triple wavelength diode laser(755nm,810nm,1064nm) in females diagnosed with facial hirsutism with Fitzpatrick phototypeIV-VI.
开始日期2023-08-10 |
申办/合作机构- |
100 项与 LIGHT 相关的临床结果
登录后查看更多信息
100 项与 LIGHT 相关的转化医学
登录后查看更多信息
0 项与 LIGHT 相关的专利(医药)
登录后查看更多信息
818
项与 LIGHT 相关的文献(医药)2025-07-01·The Ocular Surface
Topical low-dose heparin in ocular Stevens Johnson Syndrome and associated molecular correlations: A randomized controlled pilot study
Article
作者: Velpandian, Thirumurthy ; Singh, Lata ; Jain, Sandeep ; Sharma, Namrata ; Sen, Seema ; Maharana, Prafulla Kumar ; Kashyap, Seema ; Venugopal, Renu ; Sharma, Shivam
2025-05-04·Autophagy
Drosophila
aux orchestrates the phosphorylation-dependent assembly of the lysosomal V-ATPase in glia and contributes to SNCA/α-synuclein degradation
Article
作者: Tsai, Yu-Ting ; Ho, Margaret S ; Lee, Yi-Hua ; Liu, Chang ; Wang, Linfang ; Zhang, Shiping ; Yi, Shuanglong ; Yan, Wei ; Cheng, Yi-Hsuan ; Li, Shuhua ; Liu, Yang ; Wang, Honglei ; Lin, Yu-Tung ; Lin, Chia-Ching ; He, Kai-Wen ; Wang, Ruiqi
2025-04-01·Journal of Stroke and Cerebrovascular Diseases
Exploring the bidirectional relationships between alzheimer's disease and cerebral small vessel disease: Insights from mendelian randomization
Article
作者: Zhao, Ying ; Shang, Jihong ; Gong, Wen ; Liu, Tian
44
项与 LIGHT 相关的新闻(医药)2024-12-10
摘要:对抗疾病上升和传播最宝贵且成本效益最高的健康措施是疫苗接种。癌症疫苗(CV)是临床肿瘤学家极具前景且有益的工具。众多肿瘤相关抗原为免疫疗法和疫苗接种提供了极好的靶点。为确保抗原持续释放到免疫系统,载体被用于疫苗管理。最近,研究人员专注于可以专门针对肿瘤组织的疫苗输送系统,避免了与系统效应相关的挑战。本章讨论了旨在开发更精确疫苗输送系统以治疗肿瘤的研究。装载抗原的载体在靶向治疗中显示出前景,通过激活免疫系统以触发对疾病抗原的独特免疫反应。这些载体可以被抗原呈递细胞(APCs)主动摄取。有多种载体系统可用,包括物理方法和非物理方法,如类病毒颗粒(VLP)/病毒体、聚合物微粒和纳米颗粒(NPs)、脂质体、古菌脂质脂质体(archaeosomes)、免疫刺激复合物和细胞穿透肽(CPP)。本章将讨论它们在未来CV开发中的潜力以及它们的治疗潜力。
1.引言
1.1.癌症简介
几十年来,癌症一直是死亡的主要原因。然而,开发成功的癌症治疗方法非常具有挑战性。理解恶性肿瘤的病因和癌症细胞扩散过程至关重要。一系列以异常细胞无控制增殖为特征的恶性疾病统称为“癌症”。它被认为是继心血管疾病之后全球第二大死因。2015年,世界卫生组织(WHO)报告称,癌症单独导致了全球5800万死亡中的760万。研究表明,到2030年,全球将有1540万癌症相关死亡,比每年增加1000万例。化疗、放疗和手术是癌症常见且有效的治疗方法。这些治疗的有效性取决于癌症的类型。化疗的一个缺点是它无差别地针对快速分裂的细胞,导致恶性和健康细胞的破坏。放疗和手术的主要限制是它们不能消除转移。因此,仍然需要更有效、伤害更小的癌症治疗方法。研究表明,癌症疫苗(CVs)可能比传统化疗更有效,因为它们与患者的免疫系统协同工作以抑制癌细胞的生长。
1.2.疫苗简介
自1798年爱德华·詹纳首次测试天花疫苗以来,疫苗显著降低了疾病发病率和死亡率,潜在地使它们成为有史以来最重要的医学创新。尽管疫苗无疑已被证明是有益的,但在载体生产、运输和可用性方面的进展将非常有利。路易·巴斯德的“三步”范式——分离、灭活和注射——历史上一直是疫苗开发的基础。然而,随着我们对免疫学、病理学和微生物学的更好理解,疫苗开发正转向更“合理设计”的观点。这些合理设计的疫苗通常由最小成分组成(如亚单位或肽段),这使它们免疫原性较低,但在安全性和生产成本方面提供了优势。预计整合和优化这些方法,连同实施新的剂量和佐剂策略,可以帮助弥合这一效力差距。
1.3.癌症疫苗
CVs通过激活适应性免疫系统工作,最终消除癌细胞,同时通过诱导对肿瘤的免疫反应提供预防性防御。这种方法减少了来自身体不同器官或器官系统的癌细胞的肿瘤复发可能性。这归因于免疫系统识别体内肿瘤细胞的固有能力。抗原作为免疫系统刺激物,为身体对抗癌细胞做好准备。许多调查已经识别出与癌症相关的广泛抗原,其中一些目前正在临床试验和研究中作为CVs使用。现代技术在识别肿瘤中T细胞特别识别的抗原方面取得了重大进展。肿瘤抗原(TAs)可以分为两大类:肿瘤特异性共同抗原和肿瘤特异性独特抗原。由多种肿瘤细胞表达的共享抗原有时被称为肿瘤相关抗原(TAAs)。最有效的免疫疗法剂和/或输送系统与在正常组织中表达程度不同的最合适的TAs协同工作,以实现最佳治疗效果。因此,选择合适的疫苗输送机制对于发展癌症治疗的免疫策略至关重要。
1.4.治疗性免疫疗法
研究人员已经认识到治疗性抗癌疫苗相较于预防性疫苗的必要性。治疗性疫苗在疾病发生后进行管理,旨在完全停止恶性细胞的生长或控制转移和疾病复发。在针对癌症的免疫激活中涉及的主要因子是抗原呈递细胞(APCs),特别是树突状细胞(DCs)。通过针对肿瘤微环境(TME)中的DCs,可以将促进肿瘤生长的炎症转向杀伤肿瘤模式。DC特异性抗体和DC激活剂,结合癌症特异性抗原,诱导强烈的抗原特异性CD4+和CD8+ T细胞介导的免疫反应。在触发细胞介导的免疫反应后,癌细胞被干扰素-γ(IFN-γ)、肿瘤坏死因子-α(TNF-α)、趋化因子和接触介导的细胞毒性所破坏。许多纳米颗粒(NP)/脂质体配方包含靶向分子,如抗体和免疫调节剂,以及肿瘤特异性抗原,以促进APCs的激活,主要是DCs。由于其大小和组成,纳米配方很容易被DCs摄取,导致T细胞和抗体反应。大多数治疗性疫苗接种技术通过DC介导的抗原特异性细胞毒性T淋巴细胞(CTL)反应导致肿瘤退缩。这些配方设计交付的货物(抗原/抗体/Toll样受体(TLR)配体/细胞因子,见图1.1)用于进一步分类这一部分。
图1.1 癌症疫苗诱导免疫的机制途径。
在过去20年中,对肿瘤疫苗和免疫学的研究,这些都是当前癌症治疗的诱人替代品或补充品,已显著增加。这些方法旨在刺激患者的免疫系统识别和消除肿瘤细胞。它们提供了几个重要优势,包括能够:
诱导针对性的肿瘤细胞死亡,对健康非肿瘤细胞的伤害最小;
通过系统性诱导抗肿瘤免疫反应,同时针对原发性和继发性转移;
产生免疫记忆,为未来潜在的肿瘤复发提供长期保护。
2.疫苗输送系统
2.1.物理方法
DNA疫苗诱导的免疫反应类型可能因其管理方法而异。DNA可以通过静脉内(I.V.)、皮下(S.C.)、肌肉内(I.M.)或鼻内(I.N.)给药。一些研究表明,皮肤给药具有免疫学优势,与传统给药方法相比,具有更强的免疫反应。然而,由于缺乏能够一致且准确将疫苗输送到皮肤的有效给药系统,皮肤免疫接种的结果有时不明确。疫苗管理的鼻途径也因其局部和系统效应而受到关注。然而,缺乏有效的疫苗配方和安全的鼻内给药方法。当前研究正在调查基于聚丙烯酸盐聚合物的颗粒系统以增强粘膜免疫反应。标准疫苗通常使用皮内(I.D.)或皮下(S.C.)接种。在各种动物模型和临床研究中,肿瘤内和/或淋巴结内疫苗接种已被证明比其他方法更有效。在“癌症研究进展”中报告的一项研究报告中,皮下初次免疫后序贯进行静脉加强疫苗接种比单独任一管理方法产生了更强的抗肿瘤效果。注射途径可能受到几个因素的影响。最近的发现表明,使用生物弹道方法,如基因炮或Biojector 2000,可以提高效率。在小鼠上进行的研究表明,与针头注射相比,需要100倍更少的DNA就能引发抗体反应。生物弹道和针头注射可能导致不同的免疫反应。基因枪通常诱导DNA疫苗的T辅助型2(Th2)反应,而针头注射通常引发Th1反应。这种差异可能归因于使用更高的注射剂量。需要注意的是,这种结果并不常见。先前的研究表明,使用未经任何涂层的裸露DNA疫苗的基因枪输送会导致Th1偏向的免疫反应,表明基因枪轰击中使用的Au颗粒可以改变产生的免疫反应。此外,无论途径如何,某些抗原都可以影响免疫反应。增加表达DCs的抗原数量的一些技术包括激光疗法前的皮内注射、电穿孔前的肌肉内注射和微胶囊疫苗的肌肉内注射。以下讨论通过物理输送增强基于基因的免疫接种的策略。这些方法也在图1.2中描述。
图1.2 通过物理方法进行癌症疫苗递送的不同方法。
2.1.1.纹身
最近,纹身被提出作为一种将脱氧核糖核酸(DNA)物理注入表皮细胞的方法。这种方法与用于天花疫苗接种的有效策略相似,因为它似乎加快了强健宿主防御和有效免疫的发展。免疫后抗原的快速和零星合成可能解释了这种效果。研究表明,与皮内注射和基因枪递送相比,DNA纹身后的基因表达更高。通过纹身进行DNA转移似乎与肌肉内注射相比,导致不同的基因表达模式。在一个实验中,肌肉内(I.M.)注射100微克DNA导致至少比纹身20微克DNA高出10倍的基因表达峰值。纹身后基因表达立即增加,然后在接下来的四天内逐渐减少。相比之下,观察到肌肉内注射DNA后基因表达水平升高,峰值出现在七天后,可能持续长达30天。尽管DNA浓度较低且基因表达减少,但与肌肉内DNA注射相比,纹身DNA诱导了更强的细胞和体液免疫反应对抗原。此外,已经研究了通过纹身或肌肉内针头注射施用的DNA疫苗的有效性,与两种添加剂:心脏毒素和含有小鼠GM-CSF的质粒DNA(pDNA)的效果。本研究中使用了编码L1主要衣壳蛋白的人乳头瘤病毒16型(HPV16)基因作为模型抗原。结果显示,肌肉内给药分子佐剂显著提高了HPV16 L1 DNA疫苗的效果。此外,纹身设备施用的HPV16 L1 DNA比肌肉内针头递送配合分子佐剂产生了更强更快的体液和细胞免疫反应。然而,当需要更即时和强大的免疫反应时,纹身递送DNA是一种实用且经济的技术,可以应用于实验室。纹身导致几个小的机械损伤,随后出血、坏死、炎症和皮肤再生,这无意中增强了免疫系统。因此,纹身“仅”部分取代了佐剂的作用。
2.1.2.基因枪
基因枪是一种生物弹道装置,允许DNA通过使用附近的室击中目标DNA直接进入细胞。通过体外或体内基因枪技术,包括原代培养和知名细胞系在内的各种体细胞类型,已被作为悬浮或粘附培养物移植。这些事件导致树突状细胞(DCs)扩展和迁移到附近的淋巴组织,在那里它们启动T细胞以目标方式响应抗原。最近,使用TAA、人类gpl00和报告基因测定作为实验平台,进行了针对黑色素瘤的皮肤疫苗接种。研究发现,在不同类型的癌症中,包括肺癌、乳腺癌、膀胱癌和结直肠癌中,表皮生长因子受体(EGFR)蛋白高度表达。在一项小鼠实验中,通过三种不同的技术传递编码人类EGFR外域的pDNA来评估免疫和抗癌反应:肌肉内针头注射(I.M.)、镀金的DNA基因枪和未镀金的DNA基因枪。在动物肺癌研究中,未镀金pDNA基因枪注射显示出最大的抗肿瘤效果和CTL活性。这些发现可能指导未来人类临床试验中使用的DNA疫苗的开发。创建一个针对表达该基因的恶性肿瘤的EGFR DNA疫苗可能需要DNA免疫。此外,发现由胞嘧啶-磷酸-鸟嘌呤组成的CpG基序可以修改基因枪轰击后在引流淋巴结(LN)中建立的Th2型细胞因子环境。发现表明,插入CpG基序可以提高局部LN中白介素(IL)-12 mRNA的水平,无论它是通过皮内注射、肌肉内注射还是基因枪轰击给药。这些结果表明,CpG基序注射在局部LN中诱导了T辅助细胞类型1(Th1)偏向的环境。DNA疫苗和CpG基序的结合可以激活Th1免疫反应,并作为一种“警告信号”。与常规肌肉内(I.M.)注射相比,使用基因枪进行皮内(I.D.)给药被发现是施用人类乳头瘤病毒(HPV)DNA疫苗最有效的方法。最近,有报道称可以使用低压下的基因手枪传递无载体裸DNA。与金颗粒包被的DNA免疫相比,无载体无保护的预防性HPV DNA疫苗有效地减少了局部皮肤损伤。通过与金颗粒层HPV DNA疫苗进行比较,研究人员确定它也能增强对HPV抗原的T细胞免疫并改善抗肿瘤效果。最近的临床调查使用了一种名为Sig/E7detox/HSP70 DNA疫苗的HPV16 DNA疫苗,该疫苗编码与HSP70连接的信号肽与HPV16 E7(E7 detox)的抑制变体。在之前的研究中,使用三种不同的递送方法施用了pNGVL4a-Sig/E7(detox)/HSP70疫苗:针头肌肉内注射、生物喷射器和基因枪。目的是评估抗原和抗肿瘤反应。基因枪DNA免疫方法产生的E7特异性CD8+ T细胞数量最多,与针头肌肉内注射和生物喷射器给药相比。
2.1.3.超声波
为了促进细胞内DNA的融合,细胞膜可以通过超声波(US)暂时性破坏。此外,治疗性超声波与微泡造影剂的结合可能提高基因转染的效率。这一过程使得DNA能够直接且成功地转移到细胞质中。虽然已经使用这种技术将蛋白质送入细胞,但尚未将抗原引入树突状细胞(DCs)用于癌症免疫疗法。体外和体内研究表明,使用US技术可以促进裸pDNA进入结肠癌细胞。此外,在小鼠鳞状细胞癌模型中,在US处理前进行裸pDNA的肿瘤内注射增强了DNA的运输和基因表达。目前,US正在临床环境中进行研究。Memgen开发的CV在加州大学圣地亚哥分校进行的II期研究(ID:NCT00849524)中,反复通过静脉(I.V.)给药给患有慢性淋巴细胞性白血病/小淋巴细胞性淋巴瘤(CLL/SLL)的患者。
2.1.4.电穿孔
在这种方法中,对皮肤施加电脉冲,导致暂时性孔隙形成,促进DNA细胞内进入。一旦移除电能,皮肤就会恢复其结构,并由于孔隙关闭而保持免疫原性物质。历史上,毫秒和微秒脉冲已在电穿孔(EP)中得到应用。最近的研究探索了使用极强纳秒电脉冲(10-300纳秒)在极高强度(10-300千伏/厘米)下直接将DNA转移到细胞核。EP可以通过增加蛋白质表达,释放炎症趋化因子和细胞因子,吸引如巨噬细胞和DCs的APCs到EP部位来增强免疫反应。与单独肌肉内DNA注射所达到的水平相比,EP介导的pDNA传输增加了抗原特异性的体液和细胞免疫反应。已证明,在体内,EP在小型和大型动物中都能可靠地增强免疫反应,表明其在人类中的潜在应用。随后EP和US之间的比较显示了使用EP转染骨骼肌与暴露的pDNA的有效性。在最近的研究中,已经证明单独在小鼠中通过EP给药pDNA已被证明是成功的作为增强免疫。这种成功可能归因于EP增强疫苗所达到的高水平抗原生成。值得注意的是,与使用两剂DNA和EP剂量相比,这种方法显示出更大的成功。这种策略特别吸引人,因为它消除了需要两种不同的疫苗类型。例如,研究表明,当使用表达结肠癌细胞CT26的CTL表位AH1的DNA疫苗时,疫苗的剂量和体积显著影响小鼠的启动和肿瘤保护效率。动物模型已被用来研究EP驱动的DNA疫苗策略治疗前列腺癌。为了有效刺激针对表达前列腺抗原的肿瘤的抗肿瘤免疫反应,通过肌肉内介导的EP在体内给药编码phPSA的质粒。结果表明,phPSA疫苗治疗显著延缓了恶性肿瘤的进展并延长了动物的寿命。研究人员采用了多种策略来开发最佳的HPV DNA疫苗,包括融合E6和E7肿瘤抗原(E6/E7)、组织型纤溶酶原激活剂(tpa)信号序列、包含CD40配体(CD40L)和Fms样酪氨酸激酶3配体(Flt3L)。当E6和E7融合(E6/E7(Co))时,E6/E7抗原特异性CD8(+) T细胞反应减少,但预防性抗肿瘤影响增加。与CD40L相关的HPV DNA疫苗相比,Flt3L融合的HPV DNA疫苗显示出改善的治疗抗肿瘤结果和增加的E6和E7特异性CD8+ T细胞反应。在卡罗林斯卡大学医院进行的I/II期临床调查中,Chron Vac-C,一种治疗性DNA疫苗,通过EP给药给以前感染过病毒的患者,以通过增强免疫反应加快他们的康复。这项临床试验在瑞典医院的胃肠病学和传染病诊所进行。这是最早使用EP技术给人们使用的针对传染病的DNA疫苗之一。为了通过MHC类I途径增强抗原处理和传递,并增强细胞毒性CD8+ T淋巴细胞的产生,有必要通过与免疫刺激性分子如钙网蛋白(CRT)的相互作用将TAs亚细胞定位。即使在当前的进步下,找到一个可靠的DNA递送机制仍然是确保免疫治疗方法有效性的关键。在比较三种疫苗接种技术的研究中——传统的肌肉内(I.M.)注射、通过电穿孔(EP)介导的I.M.递送和表皮基因枪介导的粒子递送——使用了pNGVL4a-CRT/E7(detox)DNA疫苗。结果表明,EP是免疫E7最有效的方法,因为它产生了最大量的E7特异性细胞毒性CD8+ T细胞。
最近,几种HPV DNA疫苗已经成功地使用电穿孔(EP)技术给猕猴和老鼠模型生物进行了接种。其中一种疫苗是VGX-3100,它包含针对HPV亚型16和18的E6和E7蛋白的质粒。目前,该疫苗正在进行I期临床试验。建议有CIN 2或3病史的个体以及接受过手术的人接种这种疫苗。Cyto Pulse比以往的肌肉内电穿孔技术更有效地特异性针对皮肤细胞。Cyto Pulse开发了两种临床疫苗输送设备,DermaVax和Easy Vax。Easy VaxTM专注于皮肤的表皮层,广泛用于预防性病毒疫苗接种。另一方面,Derma VaxTM主要针对皮肤的真皮层。这种方法适用于需要强烈免疫反应和高剂量的情况,如基因治疗和癌症疫苗(CVs)。Derma Vax将在进行中或计划中的临床研究中使用。其中一项研究,编号NCT01064375,旨在使用ID EP(El-porCEA)创建一种DNA疫苗来治疗结直肠癌。该研究评估了CEA DNA免疫技术在结直肠癌患者中的免疫原性和安全性。
2.1.5.激光
体外研究表明,激光束可以将能量(首次高达20兆电子伏)传递给目标细胞,通过局部热效应改变膜的通透性。对于药用用途,需要额外的能量(高达250兆电子伏)。最近,这种尖端方法被描述为提高注射质粒的转染效率的有效方式,并在T细胞和体液免疫中引发针对抗原的免疫反应。这种新方法仅在少数试验中使用,显示出开发治疗性HPV DNA疫苗的巨大潜力。
2.1.6.喷射注射器
喷射注射器用于将雾化的药液或悬浮液注入皮肤,使用弹簧机制或压缩气体(通常是二氧化碳、氮气或氦气)包含在一个小药筒或大罐中。这种方法允许药物直接到达肌肉或更深入地穿透皮下或真皮层。
2.1.6.1.液体喷射注射器
液体喷射注射器正在开发为一次性和多次使用组件。对于像糖尿病这样的慢性疾病,使用可重复使用的设备来每天给予持续效果的剂量。预装药物的可更换设备用于办公室基础免疫、大规模疫苗接种和紧急情况,如治疗过敏和偏头痛发作。
这些设备在不需要针头的情况下对液体进行加压,这会在皮肤上形成孔。压缩气体或弹簧可以用作动力源。这导致压力配置文件较低,将剩余的液体推入皮肤。由于药物已经是液体形式,因此无需重新配制。
Walther等人已经证明,使用注射器、有限喷射注射少量暴露的pDNA用于半乳糖苷酶(LacZ)和绿色荧光蛋白靶基因范式,可以成功且安全地在各种临床前癌症模型中进行非病毒基因转染。对喷射注射的肿瘤进行定性和定量分析,揭示了有效的基因转录、增加的肿瘤内分散和深入的DNA渗透。基于这些有趣的临床前数据,进行了一项I期基因交换实验,使用喷射注射将微量的pDNA肿瘤内注射。通过定量和定性检查LacZ在mRNA和蛋白水平的表达,评估了基因转移的效率。这个实验的结果证明了这种方法在治疗局部可及的转移性实体瘤如黑色素瘤、乳腺肿瘤和其他类型的恶性肿瘤方面的有效性。对使用喷射注射器输送小干扰RNA的临床前研究也显示出额外的癌症基因治疗应用的潜力,包括DNA疫苗接种、免疫基因治疗和基因抑制技术。此外,体内喷射注射输送人TNF-α作为CD的自杀基因显著减少了肿瘤进展。
然而,液体喷射注射器也有一些缺点。它们需要精确的动力源控制,以准确可靠地向不同的皮肤类型或同一个人的皮肤的不同区域输送疫苗。喷射的高速冲击血管和神经,导致出血和不适,可能会降低患者的依从性。
2.1.6.2.固体剂量注射器
以固体形式交付的疫苗的稳定性,无论是药物还是变应原,都消除了对冷链储存的需求。这允许同时给予初始剂量和加强剂量,增强了患者的依从性。一种交付固体配方的方法是Powderject方法,它使用氦气驱动的设备将药物以超音速推进到皮肤的外层。药物颗粒由氦气微缸中的压缩气体加速,使它们在激活时能够穿透皮肤。使用时,设备直接应用于皮肤。Corgentech和辉瑞都在探索这项技术,分别用于开发局部麻醉剂和在金载体颗粒上交付DNA疫苗。另一种方法是滑块固体剂量注射器方法,其中手动操作器推动药物。操作器由一个小型固体杆组成,包含药物和辅料。当达到预定的弹簧力时,操作器自动启动并给予药物。推动动作至关重要,因为它确保了药物一致且受控地输送到皮肤的深层,无论皮肤类型或位置如何。这与Powderject方法不同,在Powderject方法中,建立一致且有效的治疗率可能是具有挑战性的。在需要给予多个剂量的情况下,操作器可以设计为可重复使用的设备,带有预装药物盒,以方便使用。
2.1.7.微针(MN)
微针(MN)由多个微结构投影组成,涂有药物或疫苗。它被应用于皮肤以将活性物质皮内输送,绕过角质层。与依赖扩散的经皮给药系统不同,MNs手动暂时性地破坏表皮,促进药物或疫苗进入其目标部位。由于它们的尺寸很小(直径1微米,长度1到100微米),MNs与普通针头不同。它们可以由各种材料制成,如金属、硅、二氧化硅、聚合物、玻璃等。MNs可以设计得足够短,以避免神经末梢,同时仍然到达角质层,减少不适、感染或受伤的风险。空心MNs、实心MNs、涂有药物的MNs和可溶解MNs是不同设计中的一部分。这些设计通过各种机制使药物的给药成为可能,允许研究治疗时间控制。实心MNs通常用于组织预处理,以增强治疗药物向选定组织的输送。在这里,微小针头的引入及其随后的移除在组织中创造了只有几纳米宽的孔,允许后来应用的氢凝胶或药物溶液到达更深的组织层。另一方面,MNs可能具有分层结构,下层输送治疗化学品,上层为穿透目标组织提供机械支持。通过这种方式,MNs应用后,不同的MN层将分解,允许治疗分子流入组织。基于癌症免疫的免疫接种旨在动员宿主的先天免疫来破坏肿瘤组织。这些方法通常侧重于将疫苗输送到皮肤,皮肤是身体最大的免疫器官,含有丰富的APCs,如巨噬细胞、朗格汉斯细胞和DCs。这些APCs可以激活T和B细胞,从而引发对肿瘤的更广泛的免疫反应。为了实现这一目标,研究人员正在研究含有免疫刺激佐剂和/或抗原的MN贴片的使用。Zaric等人通过结合甲基乙烯基醚和顺丁烯二酸酐MNs与OVA负载的PLGA NPs,展示了一种刺激免疫系统对抗表达OVA的B16黑色素瘤肿瘤的方法。作者在这一过程中使用了水包油双乳液技术来生成OVA负载的PLGA NPs用于MNs,然后将NPs添加到甲基乙烯基醚和顺丁烯二酸酐的溶液中(19×19阵列)。这些研究人员观察到MNs能够穿透小鼠皮肤并达到真皮层和附近的DCs在体外测试中。研究人员还观察到,转染的DCs能够迁移到近端LN,在那里它们可以激活CD8+ T细胞并诱导产生如IFN-γ等细胞因子。此外,这种由MNs释放NPs触发的免疫系统激活,导致表达OVA的B16黑色素瘤肿瘤生长延迟了13天。同样,Kim和同事开发了一种使用Pluronic F127和聚乙二醇(PEG)的MN贴片,以同时共输送resiquimod(R848)和TAs。人TLR7和TLR8作为R848的配体,表达在巨噬细胞、树突状细胞和B细胞等免疫细胞上。R848与TLR7/8之间的相互作用导致IL-12、IFN-γ和TNF的产生,随后触发针对抗原的体液和Th1免疫反应。在这项研究中,使用表达OVA的淋巴瘤细胞允许同时给予OVA,将免疫反应集中在由E.G7-OVA组成的肿瘤异种移植物上。
聚二甲基硅氧烷(PDMS)模具被用来沉积Pluronic F127/R848和PEG/OVA的混合物,然后在室温下在真空中固化,之后被切割成一个包含49个金字塔形针头的微针(MN)阵列。发现这些微针可以穿透小鼠的皮肤并将有效载荷释放到附近的细胞中。作者还观察到溶解的微针形成了纳米胶束,可能有助于R848和OVA分布到RAW264.7细胞中,从而诱导巨噬细胞成熟和细胞因子释放。体内实验表明,装载R848和OVA的微针可以迁移到淋巴结并激活皮肤抗原呈递细胞(APCs)。
另一方面,微针可以被设计为基于抗体的免疫疗法,旨在克服或绕过肿瘤细胞发出的免疫抑制信号。Ye及其同事开发了一种由透明质酸(HA)组成的微针阵列,用于向B16F10黑色素瘤肿瘤递送1-MT和抗PD1抗体。通过特别针对T细胞表达的PD-1受体,抗PD1抗体可以逃避癌细胞的抑制信号,允许T细胞激活。
2.2.病毒和非病毒递送系统(非物理的)
2.2.1.病毒载体
2.2.1.1.病毒载体
病毒的遗传物质可以被改变以递送转基因到感染的细胞中,因为它们天生具有免疫原性。然而,使用病毒载体在临床试验中的有效性并没有产生与传染病研究相似的结果。重组病毒可以在免疫细胞中表达转基因,特别是抗原呈递细胞(APCs)如树突状细胞(DCs)。这导致肿瘤抗原(TAs)向细胞毒性T淋巴细胞(CTLs)的呈递增加,从而更频繁和强烈地攻击肿瘤细胞。抗原由疫苗载体表达。
病毒可以自然感染人类细胞并引发T细胞和体液反应,使它们适合作为疫苗递送方法。某些病毒可以被修改为特别针对肿瘤细胞或具有固有的溶瘤特性。溶瘤病毒疗法(OVT)被广泛用于癌症治疗,因为它可以选择性地裂解肿瘤细胞并诱导对病毒和肿瘤抗原的免疫反应,导致长期记忆T细胞的产生。溶瘤病毒不仅可以直接裂解细胞,还可以被基因修改为疫苗疗法的递送载体。腺病毒、单纯疱疹病毒、副粘病毒、弹状病毒、牛痘病毒和其他病毒株是递送机制的可行选择。
腺病毒已被广泛研究作为治疗乳腺癌的溶瘤病毒平台。这是因为与健康组织相比,乳腺癌细胞中E2F-1的表达更高。腺病毒基因组策略性地位于E2F-1启动子下游,允许通过整合免疫调节元素IL-15进行选择性病毒疗法。Yan等人通过创建一个整合E2F-1启动子和IL-15的重组腺病毒载体来证明这种复制选择性病毒疗法。由Zhu等人开发的另一种重组腺病毒,通过hTERT启动子控制腺病毒E1A基因,并通过缺氧响应元素(HRE)启动子控制腺病毒E1B基因。这种重组腺病毒还包括IL-24基因,它诱导肿瘤特异性凋亡并抑制肿瘤细胞生长。
逆转录病毒,特别是RNA病毒,可以被用作DNA递送载体来管理恶性肿瘤,当病毒蛋白gag、pol和env被移除时。重组逆转录病毒载体有能力表达肿瘤细胞特有的转基因。GDEPT(基因导向酶前药疗法)利用重组逆转录病毒将非活性药物转化为肿瘤细胞内特有的活性有毒代谢物。MetXia-P450逆转录病毒载体在减少MDA-MB-231乳腺癌异种移植模型中恶性组织的生长并对T47D乳腺癌细胞对环磷酰胺(CTX)敏感方面显示出有希望的结果。Rexin-G是一种单独的疫苗方案,用于治疗包括乳腺癌在内的各种实体癌。它基于重组复制无能逆转录病毒载体,并表达促进凋亡和抑制血管生成的合成人类cyclin G1转基因。
TLRs 3和9可以被细小病毒-H1利用以刺激人类免疫系统,这触发了一个NF-κB依赖的适应性免疫反应。从乳腺癌患者的肿瘤中分离出的原发性乳腺癌细胞比正常细胞对H1PV有更高的亲和力。重组HIPV也已被用于癌症免疫疗法。具有增加的炎症细胞因子(IFN-γ和TNF-α)转基因的基因修饰HIPV显示出治疗益处。
病毒载体-DC疫苗和病毒载体-CAR T是病毒介导疫苗递送的两种关键方法。用转基因技术靶向DC已被证明是引导免疫反应朝向耐受或免疫的有效策略。使用病毒载体遗传修饰DC的关键优势是通过这种方法实现的DC成熟度增强。在Chen等人的一项体外研究中,与Ad5一起传递ErbB-2/neu基因的DCs导致了对过度表达该基因的乳腺癌细胞系的治疗性和保护性免疫。
最近对癌症疗法的研究集中了很多注意力在使用CAR修饰的T细胞和溶瘤病毒一起针对和指导实体瘤。已经探索了将基于基因的疫苗或治疗性转基因递送到实体恶性肿瘤的肿瘤微环境(TME)的潜力。病毒载体与肿瘤特异性T淋巴细胞的相互作用被发现可以增强它们的效应能力。患有血液学恶性肿瘤的患者从CAR修饰的T细胞中显示出显著的好处。根据Bajgain等人的发现,共表达倒置的细胞因子受体(4/7ICR),它连接IL4受体外域和IL7受体内域,通过转化抑制性IL4信号,增强了CAR T细胞在体内乳腺癌模型中的抗癌活性。
2.2.1.2.细菌载体
Busch和Fehleisen首次建立了癌症和细菌(化脓性链球菌)之间的联系。他们发现在癌症患者中由该生物引起的丹毒感染抑制了肿瘤生长。在19世纪,William Coley利用减毒的粘质沙雷菌和化脓性链球菌组合来治疗骨骼和软组织肉瘤。这种混合物被命名为Coley毒素。这一发现激励研究人员专注于寻找和利用细菌菌株或其产品来治疗不同的癌症。实际上,某些细菌成分,包括外毒素,已被发现能直接启动对肿瘤细胞的抗癌作用,而不是间接效果。使用细菌作为具有治疗价值的转基因递送系统提供了许多好处。在恶性细胞的厌氧条件下,像梭菌这样的特定细菌种类非常活跃和移动性强。由于它们能够到达难以接触的肿瘤区域,以及肿瘤细胞的高代谢活性使它们对化疗产生抗药性,细菌被认为是递送抗癌药物或基于基因的疫苗以治疗恶性肿瘤的潜在选择。
用于乳腺癌疫苗的最常见细菌种类包括鼠伤寒沙门氏菌、单核细胞增生李斯特菌、新威氏梭菌、丁酸梭菌、长双歧杆菌、青春期双歧杆菌和大肠杆菌。鼠伤寒沙门氏菌和梭菌据报道被用作溶瘤载体。在引入抑制的S. Typhimurium和长双歧杆菌以及合成TRAIL等分子的载体后,显著减缓了肿瘤的生长,显示出宿主基因组中凋亡基因(自杀基因)的转录增加。通过破坏细胞周期并触发细胞死亡,通过产生p53和Bax,由铜绿假单胞菌产生的阿祖林蛋白破坏恶性细胞并阻止乳腺癌和黑色素瘤的生长。为了测试细胞因子LIGHT(也称为TNFSF14或HVEM-L)在Balb/c小鼠D2F2乳腺癌模型中的有效性,Loeffler等人创建了一个嵌合的S. Typhimurium VNP20009菌株。S. typhimurium RE88与表达Fra-1和IL-18的DNA疫苗联合使用,预防了乳腺癌的生长和转移,这激活了免疫细胞(T细胞、自然杀伤(NK)细胞和DC)并阻断了血管生成。通过口服给予转基因S. typhimurium SL3261和人粒细胞/巨噬细胞集落刺激因子(hGM-CSF),体内减缓了4 T1乳腺癌的进展。经过减毒的鼠伤寒沙门氏菌菌株通常被用作人类和兽医学中的活载体。已经证明人类对用于疫苗管理的减毒沙门氏菌(S. typhimurium和S. typhi)反应良好。革兰氏阳性细菌单核细胞增生李斯特菌可以利用溶血素、李斯特菌溶素O和磷脂酶等形成孔的酶从吞噬体中逃逸并进入细胞胞质。这为疫苗递送提供了一个多功能的载体,并实现了更有效的基因转移。许多研究表明L. monocytogenes作为癌症治疗递送系统的效力。在Wood等人的一项研究中,使用针对CD105(Lm-LLOCD105A和Lm-LLOCD105B)的基于李斯特菌的疫苗治疗了乳腺癌小鼠模型。PROSTVAC疫苗,也称为PSA-TRICOM,包括重组禽痘-PSA-TRICOM增强剂和重组牛痘-PSA-TRICOM(前列腺特异性抗原加上三个共刺激分子的TRIad)的初始注射。在II期临床试验中,患有转移性、激素难治性前列腺癌的个体接受了PSA-TRICOM。
2.2.1.3.类病毒颗粒(VLPs)
被称为VLPs的高度结构化的、极其重复的结构,由病毒衣壳蛋白包装而成。这种衣壳蛋白的高密度提供了许多构象病毒表位,可以诱导强大的免疫反应。重要的是,VLPs是由病毒衣壳蛋白自行组装而成,没有任何病毒致病核酸。由于它们无法复制,它们提供了一种相对于通常用于免疫的减毒病毒的潜在更安全的选择。第一个基于VLP的疫苗针对乙型肝炎病毒(HBV)。在20世纪60年代末,Baruch Blumberg博士偶然发现了急性和慢性乙型肝炎患者血清中的独特澳大利亚抗原。他还提供了VLP生产的初步具体证据。在随后的年份中,电子显微镜被用来研究病毒形态,在20世纪80年代初,使用酵母表达系统首次组装了HBV VLPs。
伽马疱疹病毒EBV是人类发现的第一种致癌病毒,它攻击上皮细胞和B细胞。EBV与多种恶性肿瘤有关,包括淋巴瘤、胃癌和鼻咽癌,这些疾病可能发生在免疫功能正常和免疫功能低下的个体中。EBV也是单核细胞增多症的主要原因。为了开发另一种EBV疫苗模型,将EBV的gp350/220与新疾病病毒的融合F蛋白融合,使得gp350/220外域以VLP颗粒形式呈现。利用中国仓鼠卵巢细胞生产EBV-VLPs,并对BALB/c小鼠进行免疫。这导致了持久且针对性的抗体反应,即使不使用佐剂,也能在体外抑制EBV感染。为了创造一种多价疫苗,将对EBV入侵至关重要的糖蛋白gH/gL或GB、EBV核抗原1和表达在所有EBV感染细胞表面的潜伏膜蛋白2(LMP2)也纳入VLPs中。gH/gL-EBNA1和GB-LMP2 VLPs成功地在CHO细胞中生产,无需使用佐剂,并证明了它们在BALB/c小鼠中诱导高中和抗体滴度或EBV特异性T细胞反应。因此,这些EBV-VLPs可以作为治疗EBV相关恶性肿瘤的有效治疗性疫苗,以及预防EBV感染的预防性疫苗。表1.1显示了一些作为CV递送剂的VLPs的例子。
2.2.1.4.病毒体
这些极小的圆形单层脂质膜囊泡(150纳米)缺乏通常包含原始病毒遗传物质的核衣壳。然而,它们装满了病毒膜蛋白,如流感病毒中的血凝素和神经氨酸酶。这些蛋白使病毒体膜能够通过与免疫系统细胞融合,直接将其内容物——特定抗原——传递给靶细胞。这一过程即使在免疫原性较弱的病原体存在的情况下也能触发特定的免疫反应。一旦抗原被传递,细胞内的病毒体被完全消除。与其他脂质体和蛋白脂质体载体系统不同,病毒体的免疫学特性受到夹在磷脂双层之间的病毒蛋白的强烈影响。这种插层不仅为病毒体配方提供了结构稳定性和均匀性,而且还决定了抗原的表位是否位于病毒体表面(PeviPROTM)或内部,从而影响病毒体配方诱导的免疫反应类型(PeviTERTM)。使用PeviPROTM会触发免疫学体液反应,导致由于细胞内体中抗原的分解而呈现MHC II抗原。除了在体内引起CD4+和CD8+阳性反应外,PeviTERTM产生的抗原还可以产生强烈的CTL反应。病毒体封装确保通过MHC I途径正确呈现抗原,因为抗原自然地被送入抗原呈递细胞的细胞质中。
2.2.2.非病毒载体
2.2.2.1.阳离子和可生物降解聚合物
最近,制药研究和工业利用阳离子和其他碳水化合物聚合物的能力来调节药物、蛋白质、抗生素、肽、DNA或疫苗的分布。近年来开发了多种系统,如聚赖氨酸及其共轭物、壳聚糖、聚乙烯亚胺(PEI)、脂多胺、二乙基氨基乙基-右旋糖酐(DEAE-右旋糖酐)、聚酰胺胺(PAMAM)树状聚合物、右旋糖酐过氧物酶多阳离子和右旋糖酐过氧物酶多阳离子。包括树状聚合物(高度分支的PAMAM)和壳聚糖(一种可生物降解的线性氨基多糖)在内的许多阳离子聚合物,已被检查其基因转移能力。此外,壳聚糖可以通过静电相互作用与带负电的DNA(多聚体)形成复合物。最近,使用基于渗透的方法生产了壳聚糖和壳聚糖/DNA纳米球。PEI和聚(L-赖氨酸)(PLL)作为基因治疗的聚合物进行了广泛研究。由于它们的性质,可以在PEI聚合物的表面附加靶向配体和/或PEG,为基因载体提供立体稳定性。当聚乙二醇化PEI多聚体与肿瘤特异性配体共轭并静脉给药时,转染效率比聚乙二醇化(无转铁蛋白)PEI多聚体提高了五倍。研究人员研究了阳离子多聚电解质对体外恶性细胞和植入艾氏肉瘤或引起腹水的小鼠白血病(L5178Y)的影响。在肿瘤移植后5天,高分子量PEI、聚乙烯胺和PPI在中性pH下给药,导致实体艾氏肉瘤小鼠的肿瘤生长减少了10%到40%。唯一能延长由白血病细胞引起的腹水小鼠寿命的物质是PPI。因此,阳离子聚合物可能通过直接与肿瘤细胞静电相互作用并诱导宿主的一般免疫反应而有用。2013年,一种溶瘤腺病毒(Ad-DB7-U6shIL8)(oAd/PNLG)被涂覆了聚合物N-(2-氨基乙基)-2-氨基乙基甲氧基聚(乙二醇)-b-聚-N-L-谷氨酸(PNLG)聚合物。2014年,另一种阳离子聚合物被创造出来,这次特别设计了精氨酸部分以促进低水平和高水平的CAR表达。mPEG-PEI-g-Arg-S-S-Arg-gPEI-mPEG(PPSA)具有生物可还原的二硫键以减少细胞毒性,并具有几个精氨酸功能部分以增加转基因表达。溶瘤腺病毒(DWP418)在与PPSA复合后(DWP418/PPSA),被瘤内注射到CAR阴性MCF7异种移植小鼠中。结果表明,与裸露的DWP418相比,DWP418/PPSA提供了更强的抗肿瘤效果。
2.2.2.2.微粒(MPs)作为疫苗递送载体
作为疫苗递送工具,微尺度颗粒或胶囊相较于可溶性抗原具有优势。通过使用MPs,它们还可以提供持续的抗原释放、延长的抗原呈递,以及将抗原和佐剂同时传递给同一APC,大量抗原可以被传递给APCs。佐剂和抗原可以被共同封装在单个颗粒中、分开放置,或集体附着在其表面。能够增强和延长免疫反应的疫苗分布的最佳尺寸范围仍然不明确,如引用研究的发现所示。文献中包含许多使用各种可生物降解颗粒配方作为CVs的临床前研究。这些用于CVs的颗粒已使用众所周知的基于聚(α-羟基酸)的聚合物制成,如聚乳酸(PLA)和PLGA,以及更多实验性的聚合物,如聚酸酐。来自聚酸酐的MPs被报道具有固有的免疫佐剂属性。这类聚酸酐的例子包括2,6-二氧杂辛烷和1,8-双(p-羧基苯氧基)-3,6-二氧杂辛烷(p-羧基苯氧基)己烷。合成佐剂CpG和OVA使用双乳液溶剂蒸发技术共载于聚酸酐颗粒(直径1-3微米)。这些MPs提供了额外的预防性保护,以对抗表达OVA的肿瘤威胁,证据是与用可溶性OVA和CpG免疫的小鼠相比,肿瘤生长更慢,小鼠死亡率得到改善。接受这些MPs免疫的小鼠也显示出比用可溶性OVA和CpG免疫的小鼠更高水平的OVA特异性CD8+ T细胞。在肿瘤裂解物的背景下,CpG在另一种基于颗粒的疫苗配方中显示出有益效果。通过反复冷冻和解冻肿瘤细胞(无论是自体还是异体)得到的粗TA制剂,可以作为可溶性疫苗使用,或封装在颗粒中。目前正在研究利用肿瘤裂解物的潜在癌症疫苗。根据De Temmerman等人的研究,小鼠被腹腔注射含有肿瘤裂解物(来自B16.F1黑色素瘤)和CpG的PLGA(75:25)MPs。结果,脾脏中的T细胞数量显著增加。研究表明,腹腔中的树突状细胞(DCs)吞噬了MPs并将它们运输到脾脏,在那里它们触发了TH1免疫反应,证据是分离的脾细胞中IFN-γ产量增加。正在探索以碳酸钙或二氧化硅为基础的无机MPs作为疫苗载体。人类EGFR 2抗原已被装载到直径1微米、高400纳米的多孔硅MPs上。用抗原装载的硅MPs免疫刺激了肿瘤特异性CTL反应的发展,CD11c+ DCs的广泛浸润,以及肿瘤内I型IFN和MHC II表达的增加。此外,多孔二氧化硅MP载体(MSV)能够同时给同一DCs施用源自B16的抗原酪氨酸相关蛋白(TRP)2和TLR激动剂如CpG或MPLA。基于二氧化硅MPs的免疫可能通过协调有效的宿主免疫反应显著增加荷瘤小鼠的中位生存期。无机CaCO3 MPs也已开发用于封装肿瘤裂解物,目的是用于个体化抗癌疫苗。由于APCs吸收TLR激动剂的速率更高,TLR配体吸附和抗原封装的CaCO3 MPs在激活APCs和增强CV效果方面优于TLR激动剂和抗原的可溶性混合物。
2.2.2.3.纳米颗粒作为疫苗递送系统
利用纳米颗粒(NP)系统作为疫苗载体有潜力通过增加抗原递送到特定免疫细胞的效率来增强免疫细胞的免疫反应。目前,口服纳米颗粒系统用于疫苗被认为是最有希望的方法。事实上,控制时间释放剖面对于免疫刺激可能不像在更高剂量下产生药理反应那样关键。通过化学修饰,疫苗抗原可以被压缩在NPs内部或共轭在NPs表面。使用NPs递送的抗原已被证明比其他方法更有效,这可能导致快速抗原解体或减弱的免疫反应。表1.2列出了一些用于癌症递送的NPs。此外,除了抗原的定向释放外,某些复合NPs还实现了抗原的持续释放,以增强免疫系统的暴露。此外,几种NPs RNA干扰治疗目前正在进行人类临床研究,以评估其有效性和安全性。图1.3展示了用于心血管(CV)递送的不同NPs。
图1.3 用于癌症疫苗递送的不同纳米颗粒。
1.聚合物纳米粒子:壳聚糖、γ-聚谷氨酸(γ-PGA)、HT,以及其他合成和天然聚合物,如PEI、PLA、聚丙烯硫化物、丙烯酸基聚合物和PLGA等被包含在内。包括PLGA、PEI和壳聚糖在内的聚合物的使用在临床前和临床试验中显示出巨大潜力。与聚-L-赖氨酸和PEI相比,壳聚糖显示出更低的毒性。PLGA/PLA颗粒作为肿瘤疫苗和免疫疗法的主要优势在于它们能够作为一种无毒的治疗载体,同时递送抗原和佐剂,并且可以分散在长时间内。壳聚糖纳米粒子展示了肿瘤细胞选择性。越来越多的研究集中在修饰壳聚糖以增强壳聚糖纳米粒子的选择性和生物利用度。修饰后的壳聚糖纳米粒子表现出靶向精准、pH敏感性和热敏感性等特点。体外抗肿瘤测试表明,500 mg/L浓度的壳聚糖纳米粒子抑制了宫颈癌Hela细胞27%,肝癌SMMC-7721细胞23%,胃癌BGC-823细胞29%,乳腺癌MCF-7细胞55%。当树突状细胞(DCs)暴露于可溶性抗原、PLGA修饰颗粒或含有抗原的PLGA纳米粒子时,Shen等人研究了抗原吸收和CD8+ T细胞激活。Reddy等人开发了通过激活补体级联反应和产生原位危险信号来激活DCs的普朗尼克稳定的聚丙烯硫化物纳米粒子。刘等人描述了基于纳米粒子的多佐剂全细胞肿瘤疫苗用于癌症治疗。他们还使用PLGA纳米粒子作为全细胞肿瘤疫苗的递送系统,并证明了有效抑制肿瘤生长。为了应对这些挑战,目前正在探索聚合物纳米粒子包裹的姜黄素,或纳米姜黄素。在小鼠模型中,静脉注射携带TAA肽(TRP-2)和TLR-4配体(7-酰基脂质A)的PLGA颗粒显示出用两剂抑制肿瘤生长的效果。Bourquin和同事扩展了他们早期的研究,利用装载CpG的阳离子明胶纳米粒子。他们证明了用OVA和这些纳米粒子免疫的小鼠能够产生专门和保护性的抗肿瘤免疫反应。纳米乳液疫苗被用来递送肿瘤特异性抗原,结果在小鼠中引发了强烈的肿瘤靶向抗体和CTL反应。这最终提供了对肿瘤生长的保护。魏和同事开发了靶向黑色素瘤的纳米乳液疫苗,包裹TAAs,MAGE-1和/或MAGE-3。此外,他们的配方包括SEA和HSP70,这被认为可以增强肿瘤特异性免疫的发展。史等人创建了一种免疫刺激疫苗以预防胃癌,递送CpG和MG7抗原。在最近的一项研究中,小鼠被接种了装载TAA EphA2的γ-PGA纳米粒子,以评估诱导对EphA2表达肿瘤细胞的保护水平。用EphA2-PGA纳米粒子免疫的小鼠显示出增加的EphA2特异性CD8+ T淋巴细胞刺激,目标细胞分解和减少的整体肝脏生长,作为肿瘤保护的指标。
2.无机纳米粒子:尽管无机材料的生物可降解性差,但基于无机材料的疫苗已经得到了广泛的研究。无机颗粒被用作佐剂和抗原递送载体以增强免疫反应。疫苗中使用的四种最常见的无机颗粒类型是铝、Ca3(PO4)2、二氧化硅和金。
研究表明,铝颗粒既可以作为载体也可以作为佐剂来刺激免疫系统,尽管它们可以安全地与抗原结合并改变它们的结构,从而降低疫苗的有效性。李等人使用OVA和炭疽保护抗原蛋白作为模型抗原,开发了表现出增强抗原-抗体反应的氢氧化铝纳米粒子。磷酸钙颗粒由于其生物可吸收性、无毒性、佐剂特性和易于抗原装载,成为疫苗应用的有吸引力的选择。胶体金,由金纳米粒子(AuNPs)组成的溶液,已被用作免疫诊断标记和癌症治疗的治疗剂。作为一种有效的癌症疫苗(CVs)递送方法,Ojeda和同事开发了一种具有自组装单层碳水化合物抗原的AuNP系统,称为糖纳米粒子。根据Lee等人的说法,基于AuNP的CVs可以通过激活树突状细胞(DCs)上的Toll样受体9(TLR-9)来增强免疫反应。Kang等人研究了携带OVA的AuNPs对OVA运输到淋巴结(LNs)和激活CD8+ T细胞反应的影响。阴离子poly I:C和阳离子抗原肽自组装在金纳米粒子模板(iPEM-AuNPs)上,形成了一个无需溶剂或额外结构组件的免疫增强纳米系统,显著增加了抗原特异性CD8+ T细胞的数量。
基于硅的颗粒是疫苗开发中常用的一种无机颗粒,由于其生物相容性和在尺寸和形状方面的多功能性而受到青睐。已经证明,介孔硅颗粒在体内有效地作为持久的抗原载体。Kim等人使用OVA模型抗原和CSF佐剂开发了介孔硅棒作为控制的疫苗递送系统。介孔硅纳米粒子已被研究用于它们与各种细胞系的体外相互作用,包括HeLa细胞、3T3内皮细胞、人类间充质干细胞和人类结肠癌细胞。Myungi和同事在小鼠肿瘤模型中记录了使用硅纳米粒子作为疫苗递送技术增强抗原特异性B细胞和T细胞反应的生成,从而诱导保护性抗癌免疫。
3.磁性纳米粒子:Hai-Yan Xie、Wei及其团队报告了一种磁性癌症纳米疫苗,在磁场的影响下显示出显著改善的淋巴结保留,导致对癌的疫苗效果增强。当施加磁场时,淋巴结中的CD8+ DCs显示出对装饰有抗CD205的磁体素的摄取显著增加。
4.树状分子:这些是通常形成球形大分子的合成聚合物,并且具有由重复分支的链组成的结构。这些树状分子由三个不同的结构域组成:末端基团、重复分支单元和一个提供可变表面功能的中心核心。在各种树状分子类别中,基于PPI的树状分子和PAMAM被广泛使用,并引起了显著关注。Chahal等人通过用2-十三烷氧基环氧乙烷处理PAMAM G1树状分子,开发了新型烷基化树状分子,从而生产出包含脂锚定PEG和mRNA的纳米粒子。这项技术促进了特异性识别抗原的抗体和CTLs的产生。通过利用树状分子,将G250肾癌细胞特异性抗原与GM-CSF嵌合分子融合,创建了一种特别有效的疫苗,引发针对肾癌的特异性免疫反应。
2.2.2.4.脂质体和脂质纳米颗粒(LNP)
构成球形纳米囊泡的磷脂双层被称为脂质体。磷脂的头部是亲水的,而尾部是疏水的,使它们能够在水环境中自组装形成脂质体。基于脂质的技术,如脂质体,通常用于人类临床试验,特别是在癌症基因治疗中。通过调整脂质体的脂质组成、电荷、大小和表面特性,可以创建一个多功能的NP疫苗递送系统,提供一系列理想属性。脂质体已被用于运输RNA、DNA和抗原,增强对癌症疫苗目标抗原的免疫反应。脂质体纳米药物在癌症治疗、疫苗开发和胆固醇管理等领域的先进疗法中具有巨大潜力。
在1998年,Longenecker的研究团队描述了一种24-mer人类糖蛋白1(MUC1)肽脂质体疫苗。这种疫苗使用MPLA作为佐剂,比KLH偶联疫苗在小鼠中引起了更强的Th1反应并提供了保护。此外,HER-2/neu63-71与CpG的脂质体共包载导致显著的CD8+ T细胞反应和现有肿瘤的消退。与PLGA纳米粒、ISA-51和乳液相比,脂质体在诱导功能性抗原特异性T细胞方面更为有效,这一点由另一项研究所证实。Stimuvax,也称为BLP25脂质体疫苗或L-BLP25,是由Oncothyreon与默克公司合作开发的癌症疫苗。它针对MUC1的外源性核心肽以刺激免疫系统。MUC1是一种在包括前列腺、乳腺、肺和结直肠肿瘤在内的各种肿瘤中广泛表达的I型膜糖蛋白。VacciMax(VM)是另一种用于癌症肽疫苗的脂质体技术。包含MPLA和QS-21的AS01脂质体配方能够产生CD8+ CTL和抗原特异性抗体反应。将短MUC1表位、Th表位和激活TLR2的合成三酰化脂肽(Pam3CSK4)结合的三部分疫苗可以整合到脂质体中,在小鼠中产生高IgG抗体滴度,甚至无需外部佐剂。早期针对肺癌、肝癌、结肠癌和直肠癌的试验表明,含有muramyl二肽衍生物(ImmTher®)的传统脂质体增强了巨噬细胞对Ewing肉瘤的细胞破坏作用。开发了一种非紫外线活性的仙台病毒脂质体和复制蛋白抗原的组合。这些脂质体使得仙台融合蛋白能够添加到各种类型的哺乳动物细胞中,促进直接进入细胞质。与这些疫苗相比,传统脂质体的临床测试显示癌症风险较低。赵等人使用蛋白质抗原载体在小鼠模型的恶性肿瘤中增强免疫识别,使用DNA脂质体-多阳离子复合物。由于其高效率,最近作为疫苗佐剂在实验测试中被研究,用于传递与宫颈癌相关的抗生素蛋白HPV16 E7。为了创建pH敏感的融合性二油酰磷脂酰乙醇胺/蛋黄磷脂脂质体,Eiji Yuba及其同事使用了两种pH敏感的不同类型的聚(甘油醇)衍生物,它们具有线性(MGlu-LPG)结构或超支化(MGluHPG)结构。LNPs,与脂质体类似,是生物相容性和生物可降解药物管理的关键平台。徐等人开发了具有不均匀脂质双层和钙磷酸核心的钙磷酸脂质纳米粒,用作TRP2肽疫苗递送方法以治疗皮肤癌。脂质-钙磷酸疫苗刺激了与游离TRP2肽/CpG相比更强的抗原特异性CTL反应,导致在肺癌模型和B16F10 S.C.中肿瘤生长的更大减少。
2.2.2.5.免疫刺激复合物(ISCOM)
被称为免疫刺激复合物(ISCOM®)疫苗的颗粒状抗原递送载体由磷脂、胆固醇、免疫原和皂苷组成。在这项研究中,我们展示了利用ISCOM®技术开发具有抗癌特性疫苗的优势。通过使用动物模型和模型癌症抗原,观察到ISCOM®疫苗可以独立于CD4+ T细胞刺激CD8 T细胞反应,在三种不同的肿瘤模型中提供保护,并增强Th1偏向的免疫。此外,发现将疫苗抗原与ISCOM®结构耦合显著改善了免疫反应的前三个阶段。值得注意的是,ISCOM®疫苗激活的CD8 T细胞不受体内针对疫苗抗原的抗体存在的影响。虽然免疫接种已被证明对表达疫苗抗原的肿瘤有效,但对表达疫苗抗原阴性的邻近肿瘤细胞没有观察到活性。这表明,通过决定因素传递或旁观者激活并没有实现显著的抗癌作用。作为尚未经过大量人类测试的第三代抗肿瘤疫苗的一部分,正在开发各种合成的非活性佐剂和递送策略。这些包括ISCOM®疫苗、VLPs、脂质体、MF59和热休克蛋白(HREs)。另一类免疫刺激佐剂由植物提取物组成,而不是与细菌或病毒病原体相关的化学物质。南美洲的Quillaja saponaria树皮产生皂苷,它们是水溶性和结构多样的化合物,具有强大的促炎症活性。用于疫苗开发的最常用的RP-HPLC分数的Quillaja saponaria提取物是QS21。被假定为佐剂活性部位的三萜醛类,已在临床前研究中发现可诱导强烈的混合T辅助1(Th1)、体液和CD8 T细胞反应。ASC/NALP3炎症体途径将前IL1和前IL-18转化为它们的生物活性形式,QS21已被证明在很大程度上激活了这些。这证明了它与TLR4配体的组合,以触发前体的上游表达。然而,大量QS21可以引起细胞膜溶解和抗原呈递细胞(APCs)的死亡,表明由此产生的免疫反应的强度和意义与炎症体激活的程度没有直接关系。QS21在癌症免疫治疗疫苗配方中经过了广泛的测试,使用了神经节苷脂抗原(GD2、GD3或GM2)。尽管经常有强烈的体液反应,但没有个体细胞介导免疫的明确证据。QS21和MPLA在佐剂配方AS01和AS15中结合,类似于MAGE-A3癌症疫苗(GSK)。
2.2.2.6.肽和蛋白质偶联递送系统
与其他方法相比,肽疫苗具有几个优点。首先,自从1984年Merrifield因发明固相肽合成而获得诺贝尔奖以来,肽的制造和纯化过程不断发展并实现了自动化。因此,许多合同制造公司现在为研究和治疗目的提供高质量的合成肽,这些肽有详尽的描述且价格合理。与整个蛋白质或其他类型的抗原相比,肽更容易合成和放大。它们的合成简单直接,允许创建针对特定抗原靶标的肽疫苗。这消除了对蛋白质正确折叠或目标抗原位置的担忧,无论是表面结合还是细胞内。另一方面,CAR T细胞疗法需要关注表面抗原。其次,肽代表了癌症表位的最简单和最基本的生物学组成部分。通过使用肽疫苗,可以开发具有明确作用机制的疫苗策略。免疫反应可以精确针对所需的表位。相比之下,确定如肿瘤裂解物等疫苗的内容(包含一系列抗原、其他蛋白质和额外的肿瘤组分)可能具有挑战性甚至不可能。然而,肽疫苗的适度免疫原性可能是它们最大的缺点。肽通常与递送机制和/或佐剂结合使用,因为它们本身通常不足以引发足够的免疫反应。尽管这些系统正在进行研究,但仍需要改进。破伤风类毒素是另一种在肽偶联疫苗(CVs)开发中使用的载体蛋白。Kunz的研究团队描述了一种由破伤风类毒素和源自MUC1的肽组成的合成疫苗。这种疫苗显著增加了小鼠中抗原特异性免疫反应的水平。随后,研究人员将MUC1糖蛋白与Thomsen-Friedenreich抗原和破伤风类毒素的二氟衍生物结合起来,产生能够结合到MCF-7乳腺癌细胞系的MUC1特异性抗体。根据Tsuruma等人的说法,一项针对晚期或复发性结直肠癌患者的survivin衍生肽疫苗的I期临床试验。然而,这种仅含有源自survivin的肽的疫苗并没有显示出任何明显的临床效果。根据Jaeger等人的研究,肿瘤疫苗使用了酪氨酸酶、与黑素瘤相关的Melan A/MART-1肽、gp100/Pme117和流感病毒矩阵肽。自组装肽递送系统中的肽序列或修饰可以诱导超分子组装。例如,可以设计两亲性肽形成胶束、纳米颗粒、类似蠕虫的胶束、纤维状结构或水凝胶网络。刘等人开发了使用来自黑色素瘤的TRP2或来自HPV-16的E7肽的两亲性肽疫苗。这些疫苗与佐剂CpG结合时,有效地抑制了黑色素瘤肿瘤的进展,并分别诱导了大型TC-1肿瘤的持续消退。与它们的母体化合物相比,这些疫苗对身体的危害较小,并显示出增强的抗肿瘤效果。朱等人利用内源性白蛋白和自组装外源疫苗组分(CpG和SIINFEKL)生成了白蛋白/疫苗纳米复合物。这些纳米复合物显著增强了CpG和抗原在淋巴结中的积累。在他们的研究中,王等人得出结论,白蛋白提高了酸性细胞内隔室中抗原的稳定性,并促进了抗原呈递细胞(APCs)的内化。此外,白蛋白促进了抗原在引流淋巴结中的积累。
3.挑战与发展
尽管取得了许多进展和显著的临床结果,但仍有几个挑战需要解决。这些包括低抗肿瘤效果、昂贵的程序和不良反应。控制载体(CVs)必须具备安全、高效和成本效益的品质。纳米颗粒(NPs)由于其增强的免疫原性、能够靶向树突状细胞(DCs)、安全性、改善的抗原吸收和增加的生物利用度,显著有助于实现这些目标。各种物理和化学特性,如大小、靶向配体、颗粒刚度、zeta电位和内在免疫原性,已被证明对抗原呈递、细胞吸收机制、抗原分布以及免疫反应的类型和强度有显著影响。考虑这些因素对于最大化抗肿瘤反应至关重要。
然而,肿瘤生长涉及宿主免疫系统诱导抗肿瘤反应与免疫系统抑制性微环境之间的微妙平衡。CVs和减少癌症微环境(CME)的治疗方法可以结合使用,以增强免疫治疗效果。在这方面已经进行了临床前和临床研究。治疗选项包括适度的激酶抑制剂、抗体或RNA干扰,这些可以调节抑制性免疫环境,以及添加化疗药物如多柔比星、顺铂和多西他赛。
在本章中,我们描述了各种基于聚合物的系统,旨在增强前面提到的癌症免疫疗法的整体效果。这些系统可以通过使用合适的聚合物来解决上述免疫疗法的限制,进一步改善治疗效果、生物相容性和特异性。聚合物系统为结合免疫配体和装载免疫治疗药物提供了独特的递送策略,具有低毒性、高生物可降解性和可定制的表面及尺寸等优势。值得注意的是,聚合物系统可以保护生物活性分子免受不良免疫反应的影响,或促进有利于身体条件的免疫反应。然而,在这些基于聚合物系统的免疫递送方法在临床设置中实施之前,仍有挑战需要克服,包括治疗效果低、免疫疗法抗性、患者安全问题和高昂的治疗成本。因此,需要进一步的研究来增强当前的分布策略。此外,需要更多的研究来探索纳米医学的治疗潜力,考虑到它们的生物相容性以及不同聚合物系统对各种身体部位的影响。
此外,未来基于聚合物纳米粒子的免疫疗法类别应该是异常多功能的,具备目标定位、智能响应性和便于应用的能力。未来的研究趋势将主要集中在并特别看好利用聚合物纳米粒子的个性化免疫疗法。
基于肽的癌症疫苗可以安全、经济、有效地生产。它们已显示出在针对肿瘤特异性和肿瘤相关抗原方面的潜在效果。肽因其能够被用于多重技术中,针对多个表位并传达产生抗原特异性T细胞所需的最小生化信号而特别吸引人。解决低效力问题是肽药物载体可以解决的主要问题之一,以增强免疫反应刺激。大多数关于先进肽递送系统的临床前研究已经采用了一组经过良好表征的肽表位和癌细胞模型。
在临床和临床前研究中,努力标准化肽剂量可能有助于促进直接比较。
可以合成展示增强TCR结合和MHC结合的新肽变体。利用肽混合物可以引发多个CD8+ T细胞反应以及CD4+反应,从而增强T细胞免疫。在MHC限制方面,可以想象识别更大的肽序列或肽池,以适应更广泛的MHC反应性,可能使更多的患者群体受益。
在不久的将来,我们预计癌症肽疫苗的某些模式将持续存在。通过检查点阻断技术和新抗原靶向的进步,可以促进新型肽疫苗递送系统的发展。目前,有几项I/II期临床试验正在进行中,研究肽疫苗与检查点阻断抑制剂联合使用的情况。
疫苗递送系统的进步导致了NPs、自组装肽和无针递送方法的发展。在我们的I期临床试验中,SCIB1是使用EP给药的,以前的癌症和传染病疫苗也是如此。这些更近期的递送技术提供了优越的替代方案,尽管它们的实施受到EP给药不适和需要特定疫苗给药系统的限制。
由于其灵活性、高安全档案以及能够储存微小药物分子或RNA或肽抗原的能力,脂质体被用作递送载体。优化脂质体是必要的,以实现正确的电荷和粒径,以便有效地整合为载体并穿过细胞膜。可以通过各种方法针对癌症抗原,例如向佐剂中添加肽、将抗原封装在NPs中或修改遗传载体以增强局部免疫反应并增加流向LN的交通。
另一个关键的技术挑战是抗原疫苗递送的纳米载体的大规模生产。目前,大多数纳米载体在实验室中以小批量生产,然后扩大到更大的工业产能。鉴于扩大规模过程的高成本,必须密切评估直接影响治疗效果的规模依赖变量。此外,仔细评估扩大规模过程的经济可行性,以防止任何质量危机。
除了配方挑战外,重大的监管障碍阻碍了遗传疫苗在癌症治疗中的使用。要获得监管批准,解决与用于生成用于管理遗传疫苗的纳米系统的辅料相关的主要配方问题及其毒性概况至关重要。
4.结论
基因治疗的主要目标是开发高效且安全的基因载体,能够将外源性基因组分送入特定细胞类型,特别是肿瘤组织。开发和评估向癌细胞传递治疗基因的载体包括病毒和非病毒方法。各种病毒,如逆转录病毒、痘病毒、单纯疱疹病毒、腺病毒和腺相关病毒,已被修改以消除毒性,同时保持它们强大的基因转移能力。由于与病毒载体相关的局限性,非病毒载体作为一种替代品受到了关注。可生物降解的阳离子聚合物如PEI、PLL、MPs、NPs、肽和脂质体是非病毒载体的例子。
为了提高转染效率,已经开发了几种创新的运输技术和对现有递送系统的改进。疫苗接种的给药方法也可以影响疫苗与注射部位不同抗原呈递细胞之间的相互作用,从而影响免疫系统反应的发展。
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
疫苗免疫疗法
2024-11-05
CAMBRIDGE, Mass.--(
BUSINESS WIRE
)--
Obsidian Therapeutics, Inc.
, a clinical-stage biotechnology company pioneering engineered cell and gene therapies, today announced the publication of 3 abstracts for poster presentations at the SITC Annual Meeting 2024, including sharing preclinical data supporting the potential of its cytoDRiVE platform to enable a more patient-centric, core needle biopsy tumor tissue procurement procedure for OBX-115 manufacturing in non-small cell lung cancer (NSCLC) and to potentially expand the therapeutic window and application of potent, immune-modulating cytokines for armored cell therapies.
Obsidian will present preclinical data supporting a more patient-centric tumor tissue procurement procedure using core needle biopsy for OBX-115 manufacturing in patients with NSCLC, which is enabled by Obsidian’s proprietary and optimized manufacturing process, including IL15-driven tumor-infiltrating lymphocyte (TIL) expansion. This poster for abstract 444 provides evidence that, as observed with melanoma,
1
core needle biopsy can be used in NSCLC to successfully generate OBX-115 product that is phenotypically and functionally similar to product manufactured using surgical excision, maintaining similar TCR clonotype repertoire and predominantly effector-memory, stem-like phenotype with low PD-1 expression. Obsidian has previously presented clinical data demonstrating clinical efficacy in patients with advanced melanoma receiving OBX-115 where tumor tissue was obtained with a core needle biopsy.
2
Core needle biopsy is minimally invasive and typically completed as a routine outpatient procedure, reducing time, logistical complexity and total cost of care compared to surgical excision, and has the potential to increase access to care.
Obsidian is presenting two additional posters showcasing the ability of its novel cytoDRiVE regulation platform to unlock the therapeutic window of potent cytokines and broaden the reach of armored cell therapies. The poster for abstract 463 demonstrates the application of Obsidian’s drug-inducible cytoDRiVE platform to enhance antigen-responsive promoter-induced (“spatial”) activation by adding a critical pharmacologically regulatable second (“temporal”) signal to exert tight “spatiotemporal” control over IL12 expression, resulting in a positive impact on safety and tumor control in physiologically relevant animal models relative to methods from previous clinical experience.
3
This abstract has been selected by the SITC Communications Committee to be presented at the SITC 2024 Annual Meeting Press Conference, scheduled for Wednesday Nov. 6, 2024, from 12:00-1:30pm CT. To attend this press briefing, you must register as a member of the press for SITC 2024. To register, please visit
https://www.sitcancer.org/2024/press/press-registration
. After registration is confirmed, press will receive instructions for the briefing.
The poster for abstract 457 demonstrates that cytoDRiVE can bring two potent cytokines, membrane-bound IL15 (mbIL15) and LIGHT (TNFSF14), a potent immune mediator that is part of the tumor necrosis factor family, under pharmacologic regulation using a single drug-responsive domain (DRD)-ligand pairing (the same pairing used in OBX-115). The engineered mbIL15-LIGHT cell therapy demonstrated in vivo antitumor activity and evidence of tumor microenvironment (TME) remodeling in fibroblast-rich models, supporting the potential for cytoDRiVE to address solid tumors marked with an immunosuppressive TME.
Obsidian is also presenting at the Tumor Infiltrating Lymphocytes (TIL) Symposium on Wednesday November 6. Dr. Parameswaran Hari will deliver a talk titled, “
OBX-115: An engineered, pharmacologically regulatable membrane-bound IL15 TIL cell therapy for advanced solid tumors” at 9:40 am CT.
Obsidian Posters at SITC 2024:
Potential feasibility of core needle biopsy tumor tissue procurement method for TIL cell therapy with OBX-115 in non-small cell lung cancer (NSCLC)
(Abstract 444)
Presenting Authors: Matthew Bott, Memorial Sloan Kettering Cancer Center; Zheng Ao, Obsidian Therapeutics
Poster: Thursday, Nov 7, 3:10-5:00 pm CT (Immune Engineering Workshop Poster Session) and Saturday, Nov 9 (Annual Meeting Poster Session)
Antigen-responsive promoters coupled with cytoDRiVE® technology provide tight spatiotemporal regulation for tumor-infiltrating lymphocytes (TIL) expressing membrane-bound IL12
(Abstract 463)
Presenting Author: Sean Smith, Obsidian Therapeutics
Poster: Thursday, Nov 7, 3:10-5:00 pm CT (Immune Engineering Workshop Poster Session) and Friday, Nov 8 (Annual Meeting Poster Session)
Engineered tumor-infiltrating lymphocytes (TIL) with co-regulated membrane-bound IL15 (mbIL15) and LIGHT (TNFSF14) generate significant antitumor efficacy in fibrotic tumor models
(Abstract 457)
Presenting Author: Benjamin Primack, Obsidian Therapeutics
Poster: Friday, Nov 8 (Annual Meeting Poster Session)
1
Bernatchez et al., ISCT 2024 (Abstract 909).
2
Amaria et al., ASCO 2024 (Abstract 9515).
3
Zhang et al.,
Clin Cancer Res
(2015) 21 (10): 2278–2288.
About OBX-115
Obsidian’s lead investigational cytoTIL15™ program, OBX-115, is a novel engineered tumor-derived autologous T cell immunotherapy (tumor-infiltrating lymphocyte [TIL] cell therapy) armored with pharmacologically regulatable membrane-bound IL15 (mbIL15). OBX-115 has the potential to become a meaningful therapeutic option for patients with advanced or metastatic melanoma and other solid tumors by leveraging the expected benefits of mbIL15 and Obsidian’s proprietary, differentiated manufacturing process to enhance persistence, antitumor activity, and clinical safety of TIL cell therapy. Obsidian is investigating OBX-115 in the phase 1/2 Agni-01 multicenter trial in patients with advanced solid tumors (
NCT06060613
).
About Obsidian Therapeutics
Obsidian Therapeutics, Inc. is a clinical-stage biotechnology company pioneering engineered cell and gene therapies to deliver transformative outcomes for patients with intractable diseases. Obsidian’s proprietary cytoDRiVE® technology is designed to precisely regulate the timing and level of protein function by using FDA-approved small-molecule drugs. Obsidian is headquartered in Cambridge, MA. The Company has collaborations with Bristol Myers Squibb and Vertex Pharmaceuticals. For more information, please visit
www.obsidiantx.com
and follow us on LinkedIn.
免疫疗法细胞疗法临床研究基因疗法AACR会议
2024-09-24
·生物探索
引言
自身免疫病(autoimmune diseases)是机体免疫系统对自身组织器官攻击导致的炎症性疾病。自身免疫病的发病具有隐匿性、遗传倾向、难治性和复发性。常见的自身免疫病包括系统性红斑狼疮、I型糖尿病、类风湿性关节炎等。自身免疫病的发生与自身免疫耐受的打破进而引起自身反应抗体和细胞毒细胞的产生有关。然而,有意思的是,部分健康人群即使存在自身抗体,但并没有进一步发展为疾病状态,表明自身耐受的打破本身并不足以引起全面的炎症和组织损伤【1】。因此,一个关键的问题是炎症信号在自身免疫病中如何启动以及进一步放大,最终导致疾病的启始和恶化,这对于自身免疫病的治疗具有重要意义。
近日,德国柏林夏里特医学院Antigoni Triantafyllopoulou研究团队在Nature上发表了文章Amplification of autoimmune organ damage by NKp46-activated ILC1的研究文章。这项研究揭示NKp46调节ILC1-巨噬细胞-肾实质细胞轴,在不影响自身免疫条件下促进肾脏炎性级联反应放大导致组织损伤,为自身免疫宿主易感的分子机制提供深层次理解以及对慢性炎症性疾病的免疫治疗有重要意义。
作者首先在雌性NZB/W F1代小鼠中监测免疫细胞浸润情况。使用静脉注射CD45荧光抗体标记血管相关CD45+免疫细胞(CD45i.v.+)以区分组织浸润CD45+免疫细胞(CD45i.v.-)。NKp46作为激活型免疫受体常表达在ILC1、NK和部分黏膜ILC3(NCR+ILC3),这里统称为NKp46+ILC。流式分析发现组织NKp46+ILC在狼疮肾炎肾组织中显著增加。NK细胞表达而CD49b-ILC1和ILC3细胞并不表达CD49b和Eomes。在狼疮肾炎(lupus nephritis,LN)中,血管相关免疫细胞表型为Eomes+CD49b+,表明NK细胞;而组织浸润细胞为Eomes-CD49b-,表明CD49b-ILC1和ILC3细胞。鉴于NK细胞依赖于Eomes,而ILC1和NKp46+ILC3依赖于GATA3。作者分别在Ncr1cre/+;Eomesfl/fl小鼠观察到CD49b+细胞显著降低,而CD49b+CD45i.v.-细胞不受影响,在Ncr1cre/+;GATA3fl/fl小鼠观察到CD49b+NK细胞比例不变,而CD49b+CD45i.v.-细胞显著降低。与此同时,作者在人肾炎组织中同样观察到NKp46+ILC1和ILC3样细胞。总之,上述数据表明CD49b+NKp46+ILC是NK细胞,而组织CD49b-NKp46+ILC是ILC1或NKp46+ILC3。
随后,作者探索NKp46+ILC在狼疮肾炎中的作用。虽然短期anti-asialoGM1注射有效删除组织和血管相关NKp46+ILC,但长期anti-asialoGM1注射显著降低组织而非血管相关NKp46+ILC。体内结果显示,长期anti-asialoGM1注射有效改善狼疮肾炎症状,如降低蛋白尿和血尿素氮但并不影响anti-dsDNA滴度。另外,作者发现使用NKp46封闭抗体(mNCR1.15)虽然不能清除NKp46+ILC,但杀伤和结合实验表明其可以有效阻断NKp46功能。体内结果同样显示mNCR1.15在不影响anti-dsDNA滴度条件下有效改善狼疮肾炎症状。scRNA-seq分析表明阻断NKp46逆转肾炎中足细胞的丢失和毛细血管内皮损伤。总之,上述数据表明自身免疫性组织损伤需要NKp46+ILC和NKp46信号。
随后,作者分析肾组织内NKp46+ILC,包括tILC(ILC1和NKp46+ILC3)和tNK。tILC高表达ILC1基因(Thy1、Cxcr6、Cd226和Tbx21)而低表达NK相关基因(Eomes、granzymes和Klra)。肾炎中两种NK细胞富集,包括Tcf7+NK和Tigit+NK,分别代表早期分化和失能状态。tILC则主要包括Zfp683+tILC、Il7r+tILC和Il2+tILC,分别代表成熟、未成熟ILC1以及活化增殖ILC状态。值得注意的是,作者发现一种Tnfrsf9+tILC,高表达Il2ra和TNF超家族基因(例如Tnfrsf1b、Tnfrsf9、Lta和Tnfsf14)、黏附分子Icam1、趋化因子Ccl1和生长因子Csf1以及Csf2。Tnfrsf9+tILC而非其他NKp46+ILC,富集NKp46激活相关基因且在肾炎中以NKp46依赖方式增加浸润。为了确定Tnfrsf9+tILC是ILC1还是ILC3,作者分析RORγt-fate map(FM)小鼠发现Tnfrsf9+tILC大部分来源于RORγt-FM-细胞,表明NKp46刺激调控的主要是ILC1,但也会NKp46+ILC1短暂激活RORγt表达。
由于NKp46+tILC低细胞毒性和前述其可以产生Csf2以及肾炎单核巨噬细胞的显著改变,作者推测NKp46+tILC的组织损伤能力可能依赖于Csf2介导的单核巨噬调节作用。首先,作者发现Tnfrsf9+tILC是肾组织唯一产生Csf2的tILC和tNK细胞,且Csf2的产生依赖于NKp46信号。其次,Csf2-tdTomato报告小鼠发现在肾小球附近,NKp46+ILC是最主要的CSF2表达细胞。另外,CSF2封闭抗体显著减轻肾炎相关的蛋白尿、尿素氮和近端肾小管上皮损伤。最后,疾病相关的巨噬细胞大部分来源于外周血单核细胞,且CSF1R封闭删除巨噬细胞抑制肾损伤。因此,上述数据表明NKp46+tILC来源的CSF2募集外周单核细胞来源的巨噬细胞介导自身免疫组织损伤。
正常肾组织巨噬细胞为CD11blowMHC-IIhigh,而肾炎肾组织巨噬细胞为CD11bhighMHC-IIhigh/low。那么NKp46信号阻断如何影响疾病相关巨噬细胞呢?作者发现NKp46阻断虽然减轻肾炎症状,但没有再次恢复CD11blowMHC-IIhigh的巨噬细胞稳态表型,而只是大量减少疾病相关巨噬细胞浸润,表明NKp46+ILC通过CSF2调节疾病相关巨噬细胞扩增。随后,转录组测序分析发现狼疮肾炎相关一群TREM2+巨噬细胞,TREM2与巨噬细胞胞葬正相关,而与促炎基因负相关,表明TREM2+巨噬细胞是组织损伤的反应细胞。后续实验发现TREM2缺失导致肾小球毛细血管结构紊乱,表明TREM2在促进巨噬细胞向抗炎分化发挥作用。
综上所述,这项研究通过肾脏免疫细胞和实质细胞scRNA-seq结合抗体阻断和基因敲除实验,揭示NKp46+ILC1细胞通过Csf2介导单核巨噬细胞调节放大自身免疫组织损伤,对炎症性病理损伤及其治疗具有重要意义。
参考文献
1. Mahasish, Shome., Yunro, Chung., Ramani, Chavan., Jin G, Park., Ji, Qiu., Joshua, LaBaer.(2022). Serum autoantibodyome reveals that healthy individuals share common autoantibodies. Cell Rep, 39(9), 0. doi:10.1016/j.celrep.2022.110873
https://doi-org.libproxy1.nus.edu.sg/10.1038/s41586-024-07907-x
责编|探索君
排版|探索君
文章来源|“BioArt”
End
往期精选
围观
一文读透细胞死亡(Cell Death) | 24年Cell重磅综述(长文收藏版)
热文
Cell | 是什么决定了细胞的大小?
热文
Nature | 2024年值得关注的七项技术
热文
Nature | 自身免疫性疾病能被治愈吗?科学家们终于看到了希望
热文
CRISPR技术进化史 | 24年Cell综述
免疫疗法细胞疗法
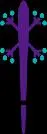
分析
对领域进行一次全面的分析。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用