Molecular Cancer: 科学家们揭示了CDK9i诱导表观遗传格局的重新编程
2023-04-18
临床1期
细胞周期蛋白依赖性激酶(CDK)家族在调节细胞周期进程(如CDK1/2/4/6)和RNA转录(如CDK7/8/9/11)中起着不可或缺的作用。
细胞周期蛋白依赖性激酶(CDK)家族在调节细胞周期进程(如CDK1/2/4/6)和RNA转录(如CDK7/8/9/11)中起着不可或缺的作用。由于染色体区域或基因扩增易位而导致的CDKs表达失调与肿瘤的发生有关,使CDKs成为有吸引力的治疗靶点。

Preview
来源: 生物谷
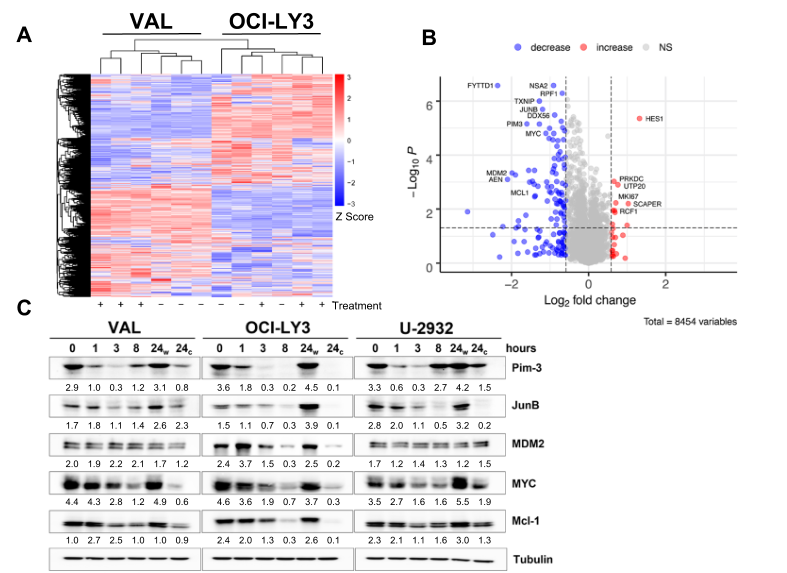
图片来源:https://doi-org.libproxy1.nus.edu.sg/10.1186/s12943-023-01762-6
弥漫性大B细胞淋巴瘤(DLBCL)表现出明显的遗传异质性,导致耐药,迫切需要开发新的治疗方法。细胞周期蛋白依赖性激酶(CDK)的药物抑制剂在DLBCL中显示出临床前的活性,但许多药物在临床开发中停滞不前。
Preview
来源: 生物谷
CDK9抑制对启动子和增强子格局的重新编程
图片来源:https://doi-org.libproxy1.nus.edu.sg/10.1186/s12943-023-01762-6
参考文献
Elana Thieme et al. CDK9 inhibition induces epigenetic reprogramming revealing strategies to circumvent resistance in lymphoma. Mol Cancer. 2023 Mar 30;22(1):64. doi: 10.1186/s12943-023-01762-6.
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
-来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


