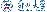《细胞》子刊:中科院联合郑大破解肠道神经促进肠癌形成的机制
2022-07-05
蛋白降解靶向嵌合体微生物疗法

Preview
来源: 生物谷
论文首页截图
Preview
来源: 生物谷
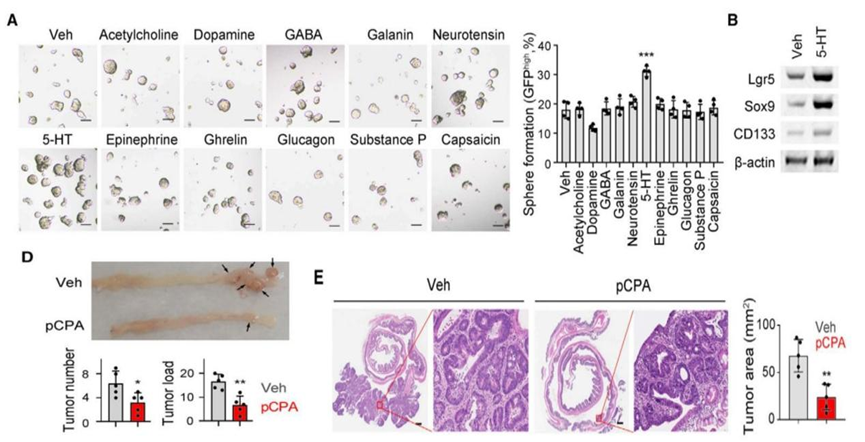
结直肠癌干细胞表达的5-羟色胺受体多达14种,5-羟色胺是通过结合哪种受体来发挥作用的呢?
Preview
来源: 生物谷
Preview
来源: 生物谷
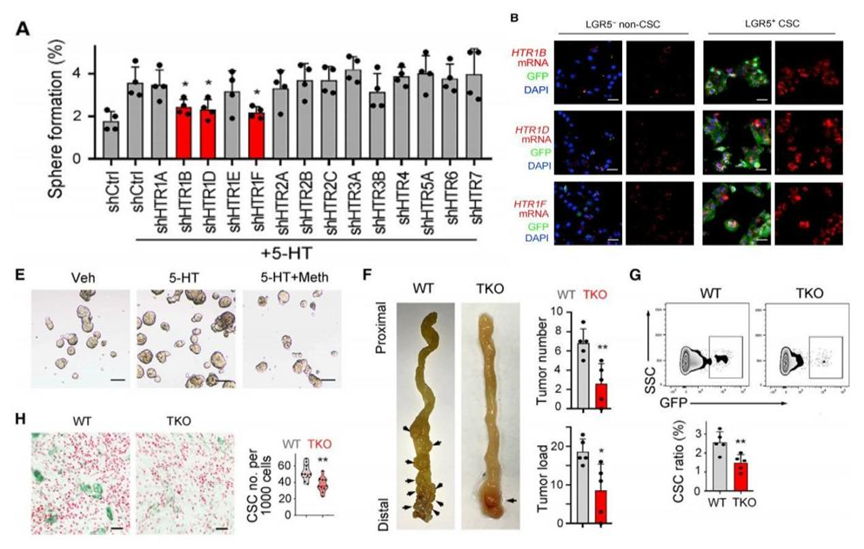
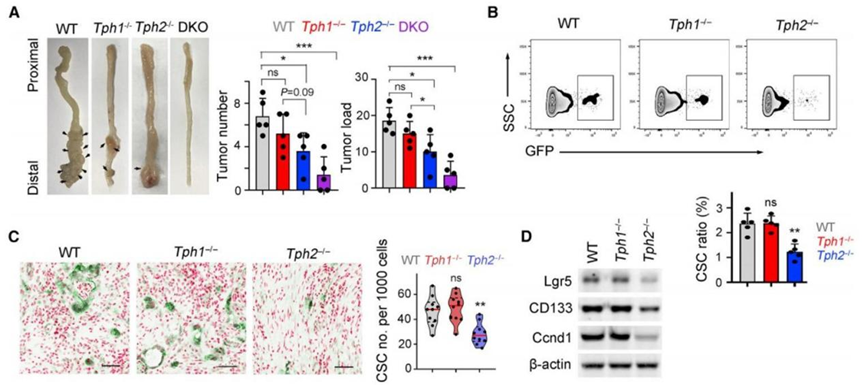
然而,在肠道内,又是什么促进血清素能神经元分泌5-羟色胺,从而刺激结直肠癌干细胞增殖的呢?
由于肠道细胞暴露在数量惊人、种类繁多的肠道菌群中,肠道菌群通过神经、代谢和免疫等途径影响肠道健康,与肠道肿瘤的发生发展密切有关[5]。因此,研究人员把目光聚焦在肠道菌群上。
Preview
来源: 生物谷
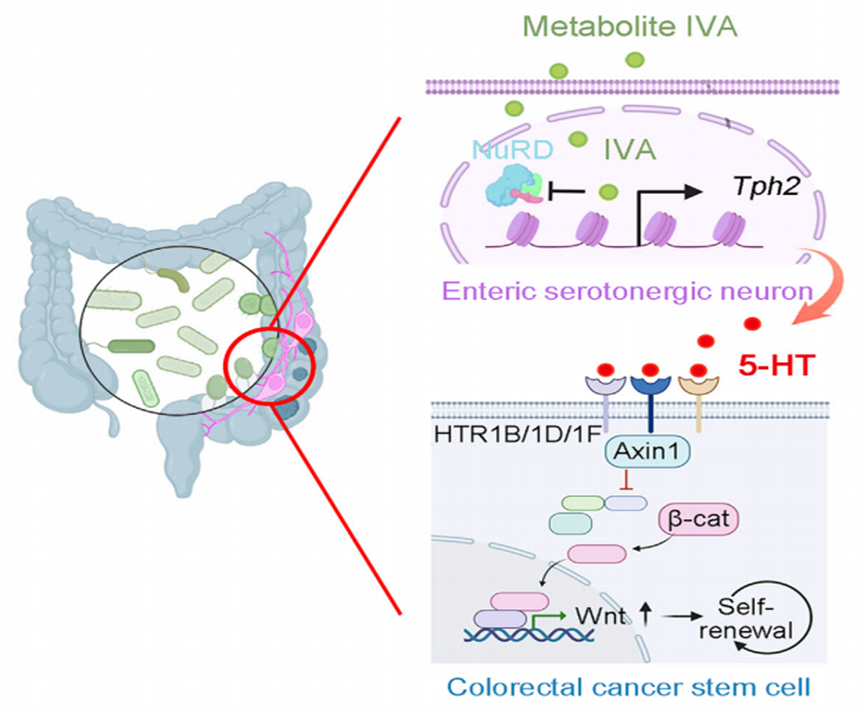
本研究机制示意图
参考文献
[1] Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021;71(3):209-249. doi:10.3322/caac.21660
[2] Drokhlyansky E, Smillie CS, Van Wittenberghe N, et al. The Human and Mouse Enteric Nervous System at Single-Cell Resolution. Cell. 2020;182(6):1606-1622.e23. doi:10.1016/j.cell.2020.08.003
[3] Zhu P, Lu T, Chen Z, et al. 5-hydroxytryptamine produced by enteric serotonergic neurons initiates colorectal cancer stem cell self-renewal and tumorigenesis [published online ahead of print, 2022 May 7]. Neuron. 2022;S0896-6273(22)00369-5. doi:10.1016/j.neuron.2022.04.024
[4] Bian J, Dannappel M, Wan C, Firestein R. Transcriptional Regulation of Wnt/β-连环蛋白 Pathway in Colorectal Cancer. Cells. 2020;9(9):2125. Published 2020 Sep 19. doi:10.3390/cells9092125
[5] Fan Y, Pedersen O. Gut microbiota in human metabolic health and disease. Nat Rev Microbiol. 2021;19(1):55-71. doi:10.1038/s41579-020-0433-9
[6] Silva YP, Bernardi A, Frozza RL. The Role of Short-Chain Fatty Acids From Gut Microbiota in Gut-Brain Communication. Front Endocrinol (Lausanne). 2020;11:25. Published 2020 Jan 31. doi:10.3389/fendo.2020.00025
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。