突破自体炎症治疗新途径:口服IL-23R和IL-17拮抗剂微蛋白显现卓越疗效
临床研究临床结果
引言
IL-23R和IL-17是自体炎症性疾病的关键治疗靶点,特别是在炎症性肠病(IBD)和银屑病的治疗中,抑制IL-23和IL-17的信号通路能够显著减轻炎症反应。然而,现有的抗体疗法存在不少局限。仅约30%的IBD患者在接受抗IL-23单克隆抗体(如Stelara)治疗后可达到缓解状态,且约20%的初始响应者会由于产生抗药抗体而逐渐失去响应。此外,系统性免疫抑制增加了患者患上恶性肿瘤和严重感染的风险。由于抗体分子较大且渗透性差,无法口服,只能通过静脉注射或皮下注射,这对患者而言既不方便又容易产生压力。生产和运输抗体也相对昂贵,因为需要在哺乳动物表达系统中生产,并进行复杂的纯化过程以达到适合注射的纯度,同时还需冷藏储存和运输。
6月26日Cell报道的研究“Preclinical proof of principle for orally delivered Th17 antagonist miniproteins”旨在开发可口服的IL-23R和IL-17拮抗剂小蛋白,以应对自体炎症性疾病中的治疗需求。研究团队通过计算设计,成功设计出具有抗体水平的低皮摩尔亲和力和极高稳定性的IL-23R和IL-17微结合蛋白,这些小蛋白不仅能够有效阻断细胞信号传导,而且在加热、酸和蛋白水解条件下表现出极强的抵抗力。
设计的IL-23R和IL-17小蛋白结合剂不仅具备低成本和易制造的优势,还可以通过口服途径达到治疗效果。在小鼠结肠炎模型中,口服的IL-23R微结合蛋白的疗效甚至优于临床使用的抗IL-23抗体。该研究展示了口服给药的去新设计微结合蛋白能够穿越肠上皮屏障并达到治疗靶点,具有高效力、肠道稳定性和简便制造的优点,为口服生物制剂提供了一种新的潜在模式。
总的来说,该研究证明了口服IL-23R和IL-17拮抗剂小蛋白在治疗自体炎症性疾病中的巨大潜力,展示了其作为口服生物制剂的可行性和优势,为未来相关药物的开发和应用提供了重要参考。

Preview
来源: 生物探索
自体炎症性疾病(autoinflammatory diseases)是由自身免疫系统异常引发的疾病,如炎症性肠病(IBD)和银屑病(psoriasis)。研究发现,细胞因子IL-23和IL-17在这些疾病的发病机制中起着关键作用。IL-23由抗原呈递细胞产生,促进T辅助细胞17型(Th17 cells)的分化和维持,而IL-17则由循环中的Th17细胞和组织驻留的先天淋巴细胞(ILCs)以及γδT细胞产生,具有强烈的促炎作用。因此,靶向抑制IL-23和IL-17的信号通路已成为治疗自体炎症性疾病的重要策略。
尽管现有的抗体治疗(如针对IL-23的单克隆抗体Stelara)在临床上显示出一定的疗效,但这些疗法存在诸多限制,如高成本、安全风险、疗效不持久以及给药不便(需注射)。因此,该研究旨在通过计算设计,开发能够口服的IL-23R和IL-17拮抗剂微蛋白,这些微蛋白不仅具有抗体水平的高亲和力,还具备极高的稳定性和低成本的制造优势,从而为自体炎症性疾病的治疗提供一种新型的、更加方便和安全的治疗方式。
计算设计与筛选
研究团队首先利用计算设计方法,设计出具有低纳摩尔亲和力和高稳定性的IL-23R和IL-17微结合蛋白。这一过程从目标蛋白的晶体或冷冻电镜(cryo-EM)结构开始,结合关键结合位点(hotspots)的信息,通过Rosetta分子建模套件优化蛋白的氨基酸序列和构象。最终,研究人员获得了数千个潜在的微结合蛋白,并将编码这些蛋白的基因转入酵母细胞,通过多轮荧光激活细胞分选(FACS)筛选出最优的结合蛋白。
体外生化特性分析
筛选出的微结合蛋白在大肠杆菌中表达并纯化,研究人员通过生物层干涉技术(BLI)和细胞信号传导抑制实验,定量测定这些蛋白的结合亲和力和抑制效力。结果显示,这些微结合蛋白均能以低纳摩尔的亲和力结合其目标蛋白,并在热、酸和蛋白水解条件下表现出极高的稳定性。
体内实验验证
在小鼠结肠炎模型中,研究团队评估了口服IL-23R微结合蛋白的疗效。实验结果表明,口服的IL-23R微结合蛋白在缓解小鼠结肠炎症状方面优于临床使用的抗IL-23抗体。此外,通过药代动力学和生物分布研究,发现这些微结合蛋白在大鼠体内具有良好的药代动力学特性和分布特点,能够穿越肠上皮屏障并到达目标组织。
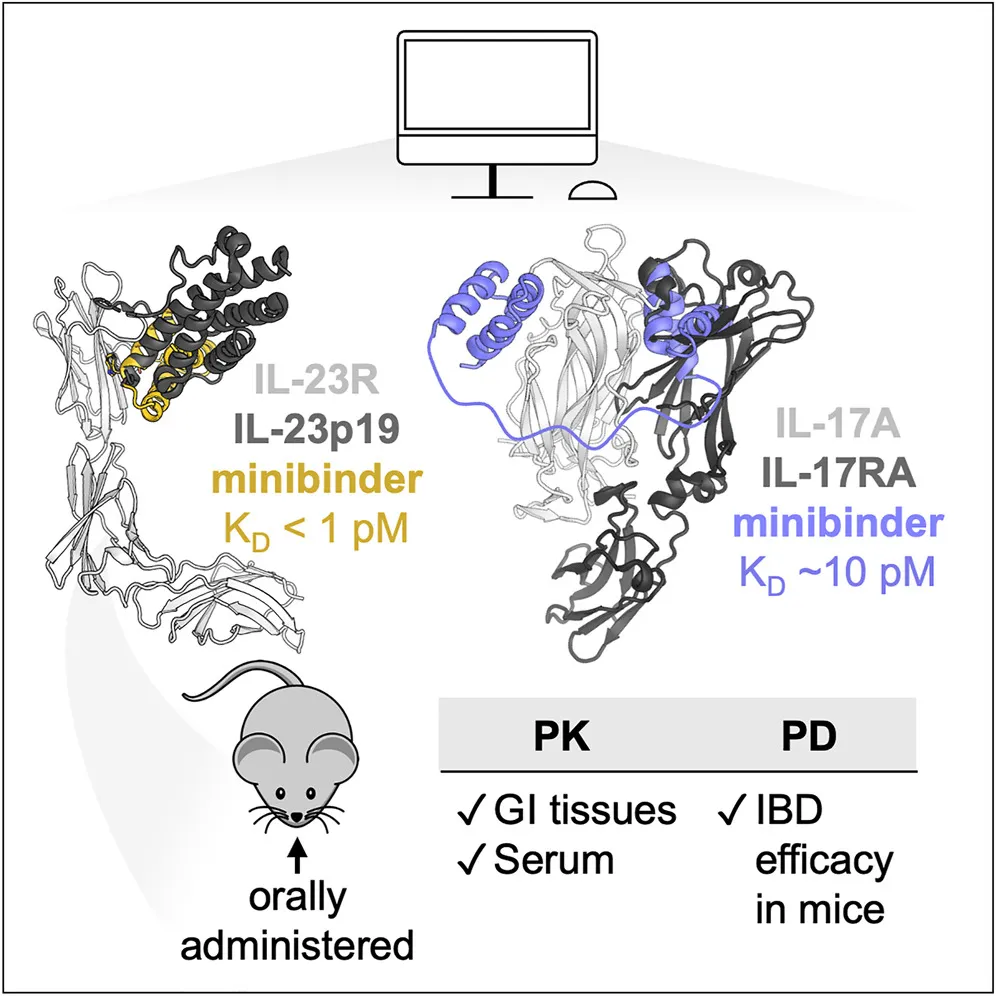
通过计算设计,研究团队成功设计出具有高亲和力和高稳定性的IL-23R和IL-17微结合蛋白。其中,IL-23R微结合蛋白23R-1和23R-2分别包含55和54个氨基酸残基,形成三个螺旋束结构,能够有效结合IL-23R。IL-17微结合蛋白17-1、17-2和17-3则分别包含43和61个氨基酸残基,能够有效结合IL-17A。
体外实验结果显示,所设计的微结合蛋白能够以低纳摩尔的亲和力结合其目标蛋白。在圆二色光谱(CD)实验中,IL-23R微结合蛋白23R-1和23R-2的变性温度(Tm)分别超过95°C和极高的化学变性中点浓度(5 M Gdn for 23R-1,>6 M for 23R-2)。IL-17A微结合蛋白17-1的Tm约为90°C,化学变性中点为4 M。IL-17A微结合蛋白17-2的稳定性最弱,其Tm约为70°C,化学变性中点为2 M。
Preview
来源: 生物探索
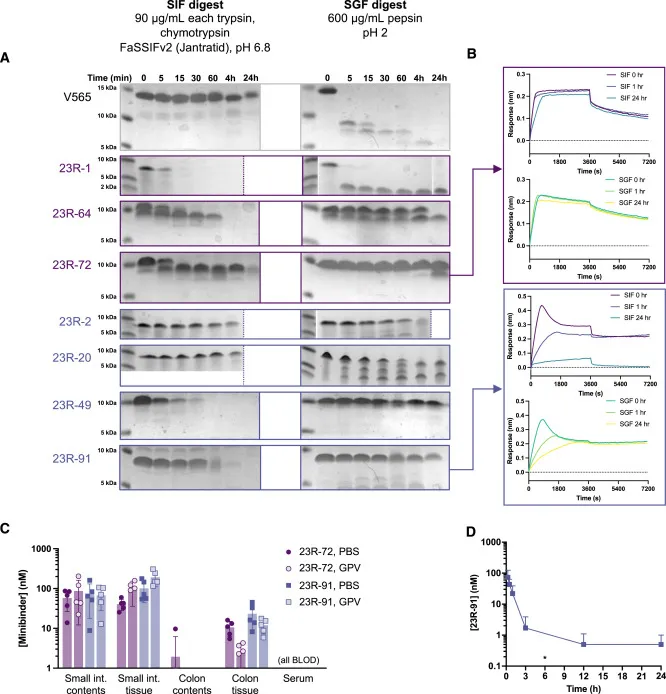
体外蛋白水解稳定性:实验将每种微结合蛋白或作为对照的V565纳米抗体(目前正在开发用于IBD的口服纳米抗体)在模拟肠液(SIF)或模拟胃液(SGF)中于37°C下消化长达24小时。结果显示,部分微结合蛋白在SGF或SIF中的稳定性较好,而有些则在较短时间内降解。
残余结合活性:SIF和SGF消化后的样品在不同时间点被稀释至10 nM的微结合蛋白浓度,并通过BLI(生物层干涉技术)测量其对人IL-23R的残余结合活性。结果表明,经过SGF和SIF消化后,部分微结合蛋白仍然保留对IL-23R的结合能力。
大鼠体内药代动力学研究:在健康大鼠中,单剂量口服20 mg/kg的23R-72或23R-91,采用PBS或胃肠保护性载体(GPV)配方,6小时后测量血清和目标组织中的微结合蛋白浓度。结果显示,无论是PBS还是GPV配方,这些微结合蛋白在小肠内容物中的浓度为50-100 nM,在小肠组织中的浓度为40-200 nM,而在结肠组织中的浓度较低,为2-20 nM。在大鼠血清中未检测到显著浓度的微结合蛋白。
血清浓度时间曲线:健康大鼠单剂量口服140 mg/kg的23R-91,在不同时间点测量血清中微结合蛋白的浓度。结果表明,微结合蛋白在15分钟后达到血清峰值浓度73 nM,随后迅速下降,半衰期约为15分钟,6小时后的浓度低于检测限。
在小鼠结肠炎模型中,口服的IL-23R微结合蛋白在缓解结肠炎症状方面表现出显著的疗效。药代动力学研究表明,这些微结合蛋白在大鼠体内具有良好的药代动力学特性和分布特点,能够穿越肠上皮屏障并到达目标组织。具体数据如下:单剂量口服20 mg/kg的23R-91在健康大鼠的肠道组织和内容物中的浓度分别为50-100 nM和40-200 nM,而在结肠组织中的浓度为2-20 nM。此外,在给予单剂量140 mg/kg的23R-91后,其在大鼠血清中的浓度在15分钟后达到峰值73 nM,随后迅速下降,半衰期约为15分钟。
研究团队还评估了微结合蛋白的免疫原性。23R-91具有高度的溶解性和稳定性,预计其免疫原性较低。在人体临床试验中,口服的23R-91未引发强烈的抗药反应。进一步的生物信息学分析显示,23R-91片段与多种主要组织相容性复合体(MHC)II类分子的结合亲和力较低,这与低免疫原性相关。
Preview
来源: 生物探索
通过计算设计开发的IL-23R和IL-17拮抗剂微蛋白展现了作为口服生物制剂的巨大潜力。相比传统的抗体疗法,这些微蛋白不仅具有高效力、低成本和易制造的优势,还能通过口服途径方便地给药,极大地提高了患者的治疗体验。该研究为自体炎症性疾病的治疗提供了一种全新的思路,展示了计算设计蛋白在生物医药领域的广泛应用前景。未来,随着更多临床前和临床研究的深入开展,这些微结合蛋白有望为广大患者带来更加安全、有效和便捷的治疗选择。
参考文献
Berger S, Seeger F, Yu TY, Aydin M, Yang H, Rosenblum D, Guenin-Macé L, Glassman C, Arguinchona L, Sniezek C, Blackstone A, Carter L, Ravichandran R, Ahlrichs M, Murphy M, Pultz IS, Kang A, Bera AK, Stewart L, Garcia KC, Naik S, Spangler JB, Beigel F, Siebeck M, Gropp R, Baker D. Preclinical proof of principle for orally delivered Th17 antagonist miniproteins. Cell. 2024 Jun 23:S0092-8674(24)00631-7. doi: 10.1016/j.cell.2024.05.052. Epub ahead of print. PMID: 38936360.
https://doi-org.libproxy1.nus.edu.sg/10.1016/j.cell.2024.05.052
<br>
内容来源于网络,如有侵权,请联系删除。
机构
-药物
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


