基于CRISPR的现货型细胞治疗公司Caribou,获辉瑞2500万美元投资
2023-07-11
细胞疗法基因疗法免疫疗法临床1期快速通道
近日,辉瑞公司宣布向 Caribou Biosciences 提供2500万美元股权投资,支持其开发治疗多发性骨髓瘤的“现货型”CAR-T细胞疗法。
2017年10月,FDA批准了首款CAR-T细胞疗法上市,人类进入细胞治疗时代,CAR-T细胞疗法在血液类癌症中取得了很好的临床效果。由于CAR-T细胞改造自患者的自体 T 细胞,因此能够在患者体内长时间发挥作用,且不产生排异反应。
如今,CAR-T细胞疗法已经成为儿童B细胞急性淋巴细胞白血病(B-ALL)的标准疗法。然而,对患者的自体T细胞进行基因工程改造,这种个性化操作耗时长,一些急性白血病患者没有足够时间等待。此外,许多严重患者已经没有足够的T细胞用于工程化改造。
因此,由健康捐赠者来源的T细胞构建的CAR-T可以避免上述问题,并可能开发出“现货型”CAR-T产品。但这需要对CAR-T细胞进行额外的基因修饰,以防止移植物抗宿主病(GvHD)以及身体对CAR-T细胞的排斥。
近日,辉瑞公司宣布向 Caribou Biosciences 提供2500万美元股权投资,支持其开发治疗多发性骨髓瘤的“现货型”CAR-T细胞疗法。

Preview
来源: 生物谷
Caribou Biosciences 由2020年诺贝尔化学奖得主、CRISPR基因编辑技术奠基人之一的 Jennifer Doudna 教授和她的学生 Rachel Haurwitz 创立,后者担任公司CEO。

Preview
来源: 生物谷
Jennifer Doudna教授(左),Rachel Haurwitz(右)
Caribou Biosciences致力于通过CRISPR基因编辑技术开发下一代“现货型”CAR-T和CAR-NK细胞疗法,解决宿主免疫系统对异体细胞疗法的排异反应,让更多癌症患者受益。
据悉,Caribou将这笔资金投入到了CB-011疗法的开发中,这是一种同种异体CAR-T细胞疗法,目前正在复发或难治性多发性骨髓瘤患者中进行1期临床试验。Caribou表示,该疗法已获得FDA的快速通道认定,是首批进入临床的同种异体CAR-T细胞疗法之一,旨在通过免疫隐身策略提高抗肿瘤活性。该疗法针对BCMA靶点,旨在去除B2M蛋白并插入B2M-HLA-E融合蛋白,以防止免疫介导的排斥反应。
2022年5月12日,Caribou公布了首个人体临床试验数据,其开发的基于CRISPR基因编辑的现货型CAR-T疗法CB-010CB-010,在治疗复发难治性B细胞非霍奇金淋巴瘤的1期临床试验中效果积极。在可评估的5名患者中,总缓解率(ORR)达100%,完全缓解率(CR)达80%。
实际上,治疗效果的持久性已经成为现货型CAR-T面临的行业难题,此前Allogene、CRISPR Therapeutics、Precision Biosciences等公司都出现了相当比例的癌症患者在治疗后6个月内复发的问题。
目前,Caribou 共有4款自研管线,以及2款与艾伯维(AbbVie)合作研发管线。
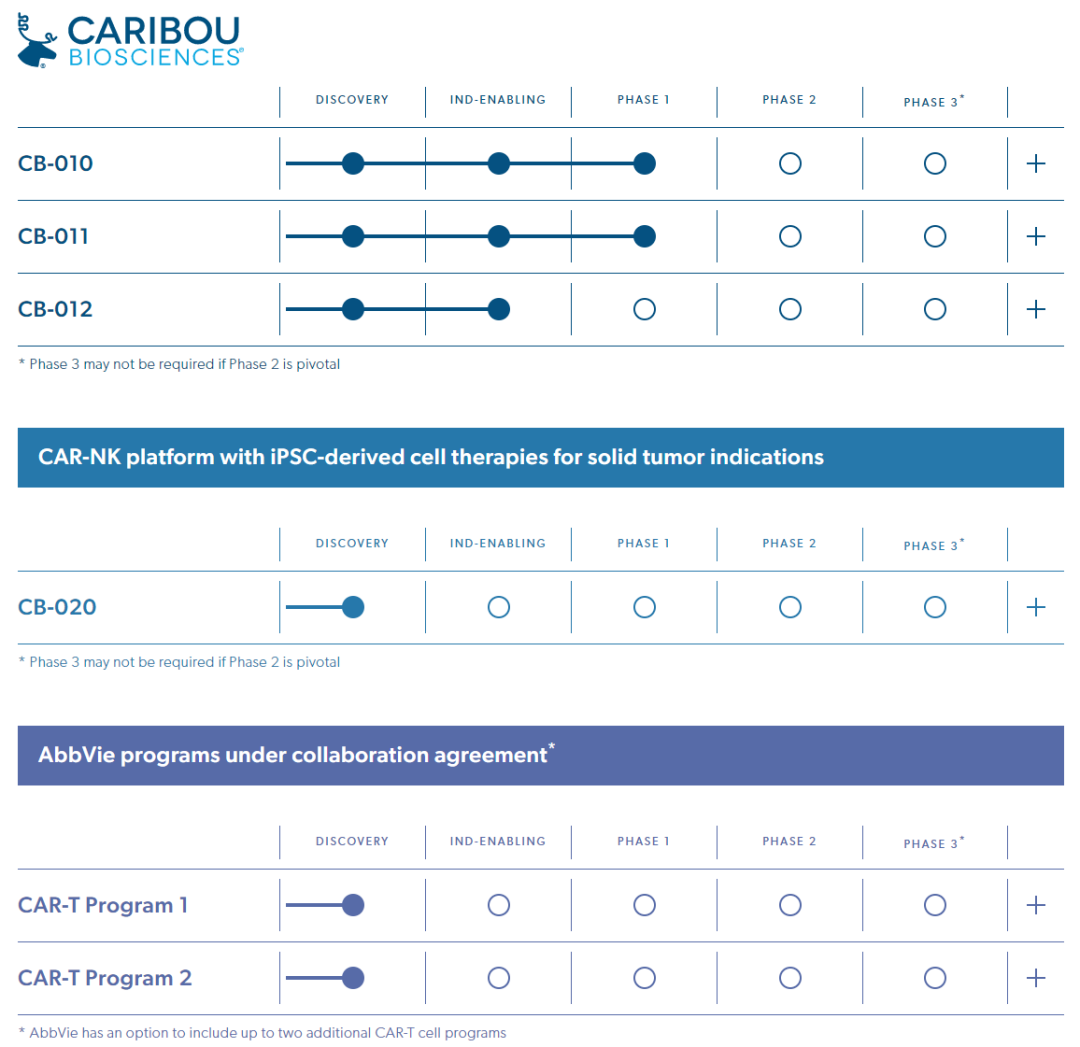
Preview
来源: 生物谷
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。




