治疗痴呆症,潜在“first-in-class”疗法获FDA突破性疗法认定
2024-02-09
孤儿药突破性疗法快速通道
Alector Therapeutics公司和GSK今日宣布,美国FDA已授予在研抗体疗法latozinemab突破性疗法认定。这款潜在“first-in-class“人源化单克隆抗体旨在抑制名为sortilin的受体蛋白,从而提高颗粒蛋白前体(PGRN)的水平,目前正用于治疗带有编码PGRN的GRN基因突变的额颞叶痴呆(FTD)患者。

Preview
来源: 药明康德
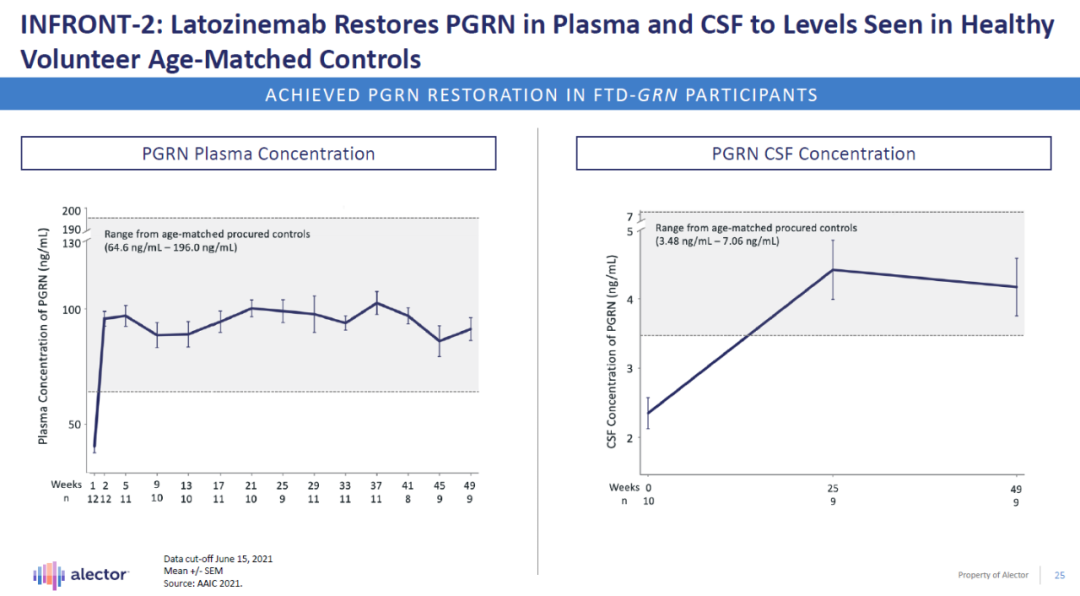
这一突破性疗法认定是基于名为INFRONT-2的2期临床试验结果。试验数据显示,latozinemab将患者血浆和脑脊液中PGRN水平恢复到年龄相当的健康志愿者的水平。
Preview
来源: 药明康德
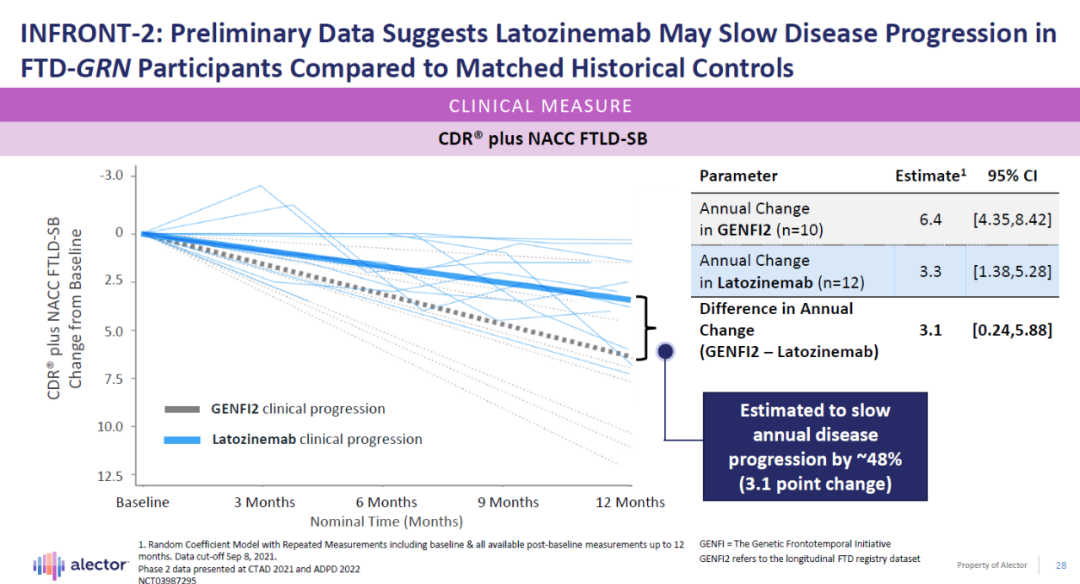
同时,初步评估数据显示,与历史对照相比,latozinemab可能减缓患者的疾病进展。
Preview
来源: 药明康德
Latozinemab(AL001)是一种针对PGRN的单克隆抗体。PGRN是大脑内免疫反应的关键调节因子,与多种神经退行性疾病(包括FTD、阿尔茨海默病和帕金森病)相关。Latozinemab的作用机制涉及抑制sortilin,这是介导PGRN降解的受体,目的是提高患者的PGRN水平。它已经获得FDA授予的孤儿药资格、快速通道资格和突破性疗法认定。GSK与Alector在2021年达成研发合作,共同开发这款抗体。
FTD代表一组罕见的神经退行性疾病,是年轻人中痴呆的主要原因之一。FTD包括多种遗传形式,5%至10%的FTD病例与GRN基因的突变有关。症状通常在40到50岁时出现,表现为行为变化、判断力下降和语言能力减退。目前,美国FDA尚未批准任何形式的FTD治疗方法。
参考资料:
[1] FDA Grants Latozinemab Breakthrough Therapy Designation for Frontotemporal Dementia Due to a Progranulin Gene Mutation (FTD-GRN). Retrieved February 7, 2024, from https://www.globenewswire.com/news-release/2024/02/07/2825041/0/en/FDA-Grants-Latozinemab-Breakthrough-Therapy-Designation-for-Frontotemporal-Dementia-Due-to-a-Progranulin-Gene-Mutation-FTD-GRN.html
[2] Alector Corporate Presentation. Retrieved February 7, 2024, from https://investors.alector.com/static-files/70f1e5de-e44d-43a7-9500-8af6a1ea80a5
内容来源于网络,如有侵权,请联系删除。
热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。



