颜宁最新论文:发现抗癫痫药物拉莫三嗪对钠离子通道的双口袋抑制作用,为下一代抗癫痫和止痛药物开发奠定基础
2023-10-09
临床2期
以Nav通道为靶点的药理学研究已证明其在治疗多种疾病方面具有巨大价值,开发以Nav通道为靶点的新药是药物化学研究的一个活跃领域。该领域药物开发的一个特殊挑战是精确地靶向Nav通道的特定亚型或状态,以尽
颜宁教授团队在《美国国家科学院院刊》(PNAS)发表了题为:Dual-pocket inhibition of Nav channels by the antiepileptic drug lamotrigine 的研究论文。

Preview
来源: 生物谷
Nav通道对肌肉收缩、感觉知觉和神经递质释放等多种生理过程至关重要,这些通道由一个成孔的α亚基(包括1个离子传导孔结构域和4个电压感应结构域)以及调节通道功能和定位的辅助β亚基组成。
拉莫三嗪(Lamotrigine,LTG),商品名为利必通(Lamictal),由葛兰素史克公司(GSK)开发,是FDA批准的用于癫痫和双相情感障碍一线治疗的药物。
利鲁唑(Riluzole,RLZ),商品名为力如太(Rilutek),由赛诺菲公司(Sanofi)开发,是FDA批准的用于渐冻症(ALS)和其他运动神经元疾病的治疗药物。
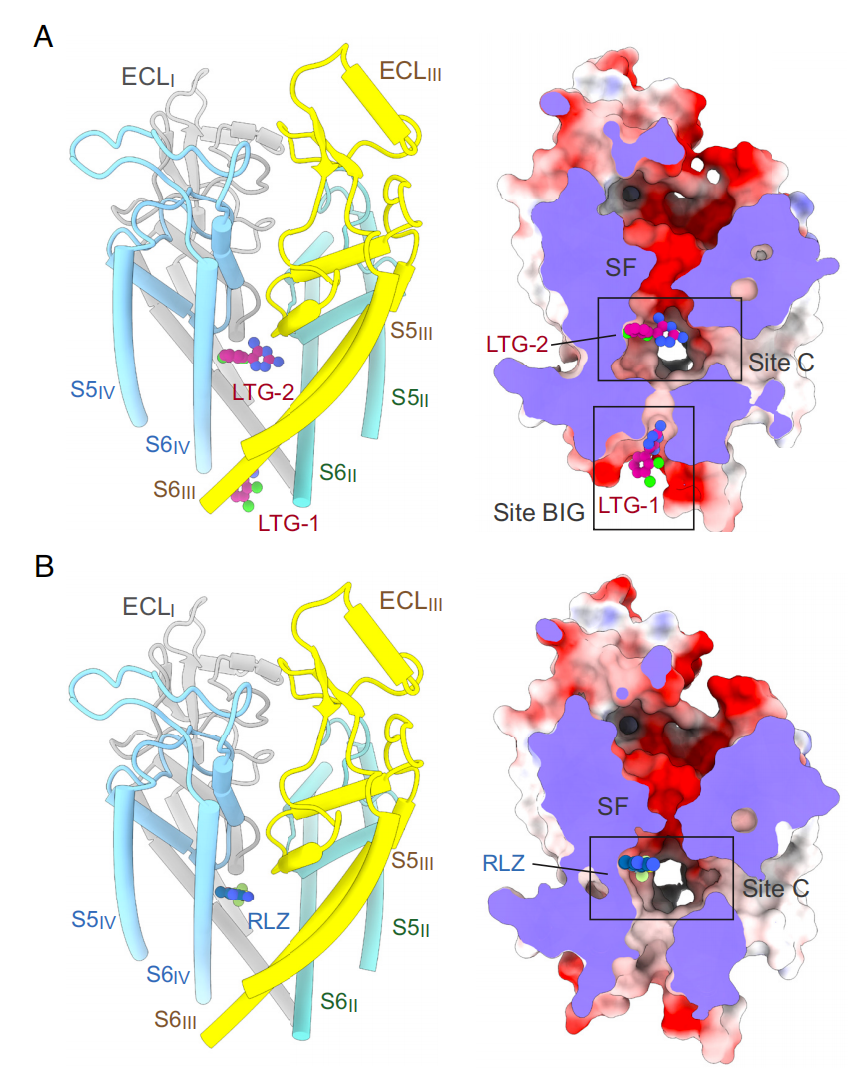
尽管已经对LTG和RLZ作为非选择性Nav阻断剂进行了广泛研究,但这两款药物与Nav通道的结合细节仍不清楚。
Nav通道的高分辨率结构与这些临床药物的复合物将提供深入了解其作用机制(MOA)的化学基础,并有助于开发下一代抗癫痫药物和止痛药。
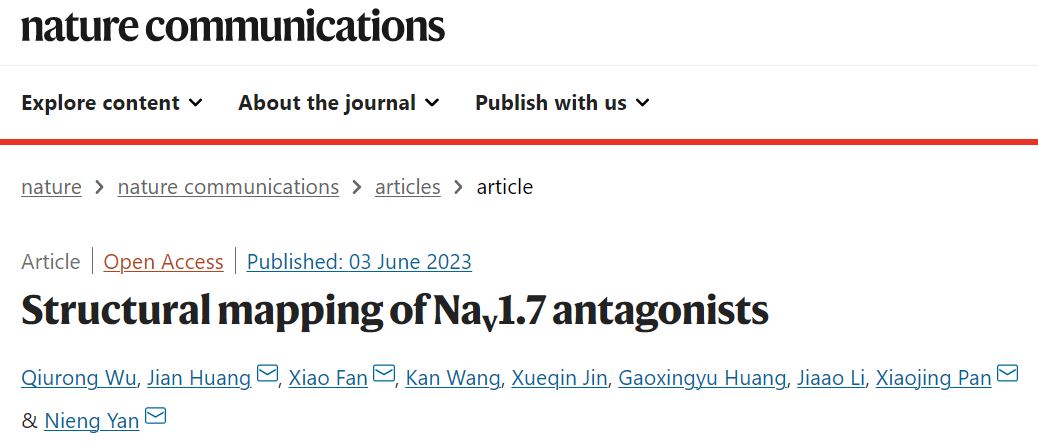
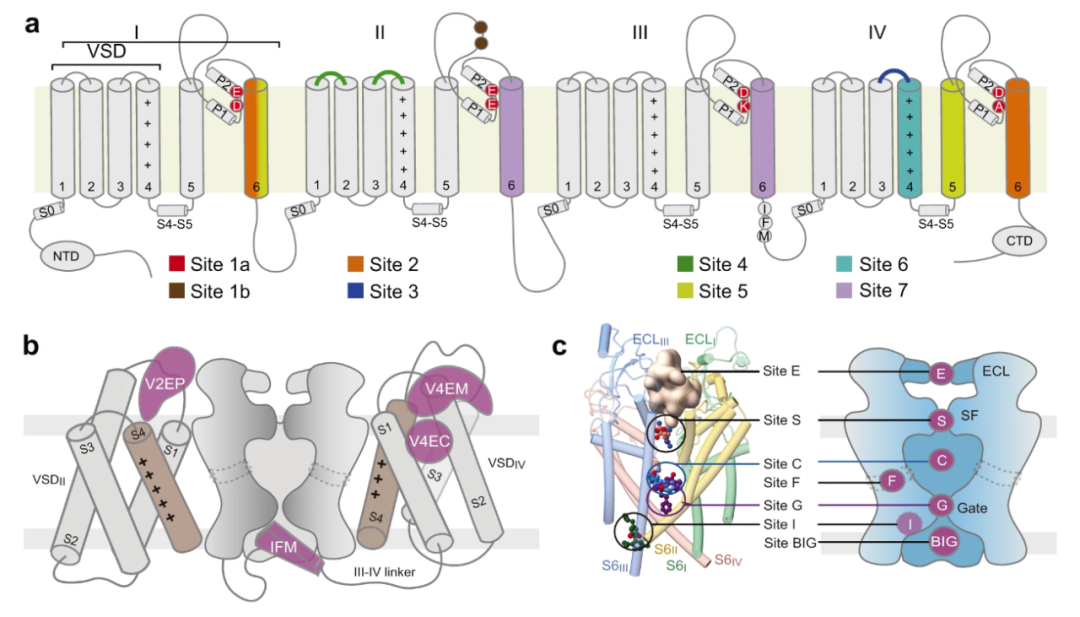
2023年6月,颜宁团队在 Nature Communications 期刊发表论文【2】,其中绘制了Nav通道上药物结合位点的结构图。
Preview
来源: 生物谷
Preview
来源: 生物谷
Preview
来源: 生物谷
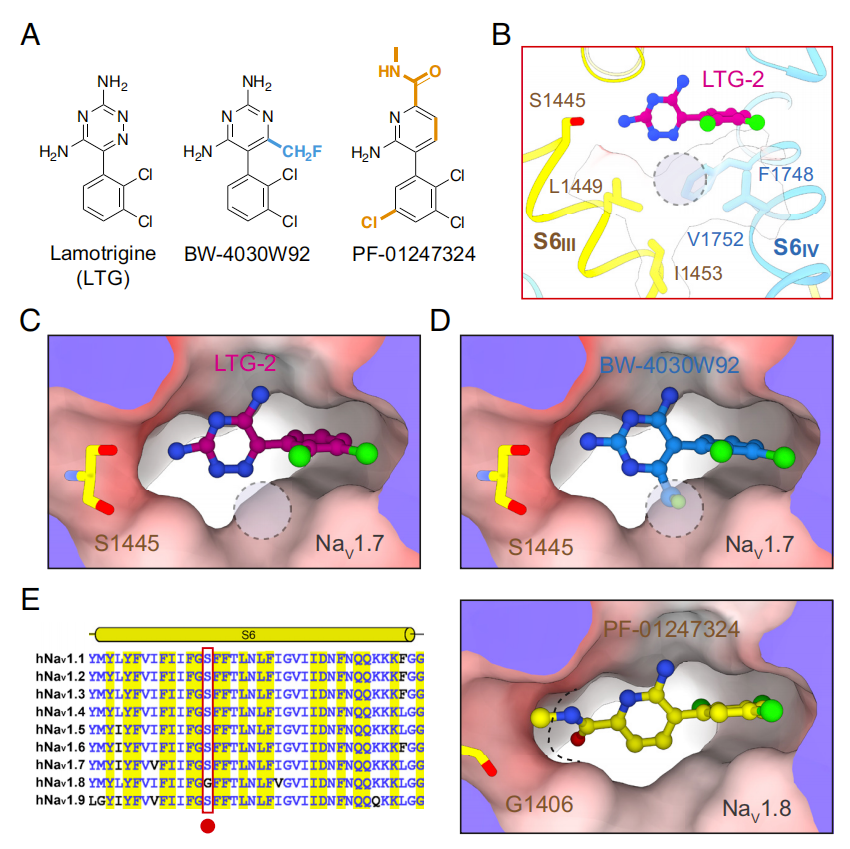
在过去几十年里,研究人员开发出了许多以拉莫三嗪(LTG)为基础骨架的LTG相关线性6,6系列化合物作为潜在的抗癫痫和止痛候选药物。对LTG的杂环核心和芳基取代模式的化学修饰,会提高对对Nav通道的疗效(例如BW-4030W92)和亚型特异性(PF-01247324)。
Preview
来源: 生物谷
该研究通过对结构解析,辅以对接和突变分析,解释了LTG相关线性6,6系列的结构活性关系,揭示了这些候选药物作用机制的分子基础,从而有助于开发新型抗癫痫药物和止痛药物。
以Nav通道为靶点的药理学研究已证明其在治疗多种疾病方面具有巨大价值,开发以Nav通道为靶点的新药是药物化学研究的一个活跃领域。该领域药物开发的一个特殊挑战是精确地靶向Nav通道的特定亚型或状态,以尽量减少脱靶效应。
但长期以来,由于缺乏精确的结构,阻碍了靶向Nav通道药物的合理设计。近年来Nav通道的结构研究蓬勃发展,但人工智能(AI)促进的药物发现仍然受到训练数据库有限的限制,其中配体结合结构的数量仍然很少。此外,构象动力学超出了目前结构预测的能力,因此,与配体结合的靶蛋白的实验结构解析对于药物发现是必不可少的。
颜宁团队通过阐明与原型药物结合的各种人类Nav通道的高分辨率结构来应对这一挑战。这项研究不仅解释了各种临床和研究药物不同作用机制的分子基础,而且为基于结构的理性设计下一代更具疗效和选择性的抗癫痫药物和非成瘾性止痛药物建立了框架。
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。




