中国科学院研究者们揭示了出生后神经发生以维持适当的前脑功能的关键机制
2023-07-26
神经干细胞/祖细胞(NSPC)是一种自我更新的多潜能细胞,在胎儿发育过程中形成大脑皮层,并持续存在于成年前脑中。神经发生中NSPC产生新神经元的过程是正常大脑发育和功能所必需的。
神经干细胞/祖细胞(NSPC)是一种自我更新的多潜能细胞,在胎儿发育过程中形成大脑皮层,并持续存在于成年前脑中。神经发生中NSPC产生新神经元的过程是正常大脑发育和功能所必需的。
终生持续的神经发生发生在海马齿状回的颗粒下带(SGZ),并被认为与认知过程和神经系统疾病有关。然而,关于NSPC在出生后神经发生过程中决定命运和功能的调控机制,仍有许多需要了解。
NSPC在出生后阶段的维持和分化受到复杂的分子网络的严格控制。更好地理解这些在出生后神经发生中的调控机制可能会为深入阐明大脑的可塑性提供更多的线索,为实现NSPC治疗神经系统疾病的潜力提供更多的线索。

Preview
来源: 生物谷
图片来源: https://doi-org.libproxy1.nus.edu.sg/10.1038/s41418-023-01189-y
近日,来自中国科学院的研究者们在Cell Death & Differentiation杂志上发表了题为“ASH2L regulates postnatal neurogenesis through Onecut2-mediated inhibition of TGF-β signaling pathway”的文章,该研究揭示了ASH_2通过抑制转化生长因子-β信号通路调控生后神经发生。
在本研究中,研究者报告了组蛋白甲基转移酶多聚体复合体的核心成分Ash21(缺失的、小的或同源异型盘样2)在出生后神经发生过程中对NSPC命运的决定是必不可少的。NSPC中Ash21基因的缺失会损害NSPC的增殖和分化能力,导致成年出生的海马神经元树突状突起的简化和认知能力的下降。
重要的是,研究者发现ONECKUT 2在NSPC中调节转化生长因子-β信号,并且用转化生长因子-β抑制剂治疗可以纠正缺乏Ash21的NSPC的表型。总而言之,本研究发现揭示了ASH2L-ONECUT2-转化生长因子-β信号轴,它介导了出生后神经发生以维持适当的前脑功能。
Preview
来源: 生物谷
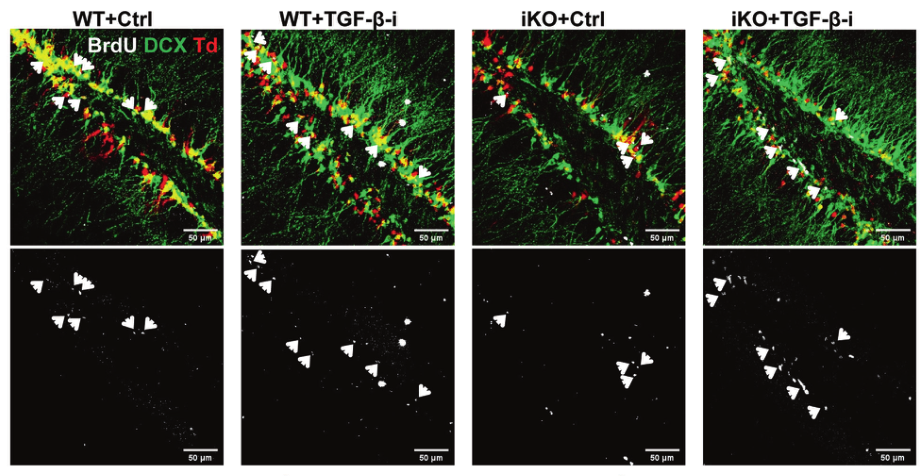
抑制转化生长因子-β信号通路恢复Ash21基因缺陷小鼠成体神经发生缺陷
图片来源: https://doi-org.libproxy1.nus.edu.sg/10.1038/s41418-023-01189-y
综上所述,本研究揭示了Ash21是调节NSPC增殖和分化以及正常认知功能的关键调节因子。研究者表明,Ash21、OC2和转化生长因子-β形成了一个调控网络,控制着NSPC细胞命运的决定。这些发现代表着朝着揭开NSPC生物学基础的分子机制迈出的重要一步,并可能为干细胞治疗修复受损的大脑提供新的再生潜力。(生物谷 Bioon.com)
参考文献
Ya-Jie Xu et al. ASH2L regulates postnatal neurogenesis through Onecut2-mediated inhibition of TGF-β signaling pathway. Cell Death Differ. 2023 Jul 11. doi: 10.1038/s41418-023-01189-y.
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
机构
药物
-热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。



