更新于:2024-06-20
TROP2 ADC(luzsana)
更新于:2024-06-20
概要
基本信息
非在研机构- |
最高研发阶段临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
结构
使用我们的XDC技术数据为新药研发加速。
登录
或

关联
100 项与 TROP2 ADC(luzsana) 相关的临床结果
登录后查看更多信息
100 项与 TROP2 ADC(luzsana) 相关的转化医学
登录后查看更多信息
100 项与 TROP2 ADC(luzsana) 相关的专利(医药)
登录后查看更多信息
13
项与 TROP2 ADC(luzsana) 相关的新闻(医药)2024-06-18
·米内网
精彩内容
6月18日,科伦药业发布公告称,注射用SKB518获批临床,该产品是公司今年首个获批临床的1类新药。在抗肿瘤和免疫调节剂这个千亿市场,科伦药业有3款1类新药正在冲刺上市,6款1类新药在开展临床。
公告中提到,注射用SKB518是一款创新抗体偶联药物,在临床前展现了良好的有效性和安全窗,拟用于治疗晚期实体瘤。
近几年,科伦药业的新药研发不断迎来好消息,目前3款生物药1类新药正在冲刺上市,均属于抗肿瘤和免疫调节剂。
图1:科伦药业申报上市并在审的1类新药情况来源:米内网中国申报进度(MED)数据库
塔戈利单抗注射液是一款PD-L1单抗,在2021年11月首次提交上市申请,用于治疗鼻咽癌,该新药有望成为公司首款获批的生物药1类新药。
注射用A166是一款靶向HER2的创新抗体偶联药物,也是科伦药业首个提交上市申请的ADC药物。该新药在2023年5月提交了用于既往经二线及以上抗HER2治疗失败的HER2阳性不可切除的局部晚期、复发或转移性乳腺癌的上市申请。
注射用SKB264是一款靶向TROP2的创新ADC,该新药在2023年12月提交了用于既往至少接受过2种系统治疗(其中至少1种治疗针对晚期或转移性阶段)的不可切除的局部晚期或转移性三阴性乳腺癌(TNBC)成人患者的上市申请。该新药有望成为中国首个获批上市的国产创新TROP2-ADC。
图2:中国三大终端六大市场抗肿瘤和免疫调节剂的销售情况(单位:万元)来源:米内网格局数据库
米内网数据显示,2023年在中国三大终端六大市场(统计范围见文末)抗肿瘤和免疫调节剂的合计市场规模已超过了2200亿元,近三年保持正增长态势,潜力不容小觑。
表1:科伦药业已开展临床的1类新药情况注:已终止项目不纳入统计来源:米内网中国临床试验数据库
目前,科伦药业在研的1类新药中有多个涉及抗肿瘤领域,包括了化药1类新药KL590586胶囊和KL340399注射液,生物药1类新药注射用SKB410、注射用SKB315、SKB337注射液、KL-A289注射液,上述新药均在I期临床阶段,后续有望为公司抢攻千亿市场添新动力。
资料来源:公司公告、米内网数据库注:米内网《中国三大终端六大市场药品竞争格局》,统计范围是:城市公立医院和县级公立医院、城市社区中心和乡镇卫生院、城市实体药店和网上药店,不含民营医院、私人诊所、村卫生室,不含县乡村药店;上述销售额以产品在终端的平均零售价计算。数据统计截至6月18日,如有疏漏,欢迎指正!
本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。投稿及报料请发邮件到872470254@qq.com稿件要求详询米内微信首页菜单栏商务及内容合作可联系QQ:412539092
【分享、点赞、在看】点一点不失联哦
抗体药物偶联物申请上市临床1期引进/卖出上市批准
2024-06-07
·药智网
尽管靶向治疗和免疫疗法在非小细胞肺癌(NSCLC)领域取得了快速进展,但耐药、疗效有限等问题让NSCLC仍是值得研究的癌种。
近年来抗体偶联药物(ADC)在肺癌领域蓬勃发展,展现出了较好的临床应用前景。在近日召开的2024年美国临床肿瘤学会(ASCO)大会上,诸多非小细胞肺癌领域的ADC药物研究成果公布。其中备受关注的药物包括第一三共的Dato-Axd以及科伦博泰的Sacituzumab Tirumotecan等。
多靶点ADC
治疗NSCLC展现优势
NSCLC中可药物靶向治疗的靶点众多,针对NSCLC的ADC药物靶点也呈百花齐放之态,包括HER2、TROP2、IB6、c-MET等。其中HER2靶点最为成熟,已有罗氏的T-DM1和第一三共的T-DXd两个ADC药物获批上市,目前这两款药物年销售额都超过了20亿美元。
在研药物中TROP2靶点备受关注,其中又以进展最快的Dato-DXd为关注重点。
Dato-DXd是第一三共开发的一款TROP2靶向ADC药物,由重组人源化的IgG1抗体MAAP-9001a、拓扑异构酶I抑制剂Dxd和可裂解连接子构成。在NSCLC患者中,高达64% 的肺腺癌患者具有TROP2高表达,且与腺癌的不良预后直接相关。此外,TROP2高表达也与PD-L1抑制剂治疗后进展有关,因此TROP2成为近年来肺癌领域ADC研发的热门靶点之一。
Dato-DXd在2023年欧洲肿瘤内科学会(ESMO)上公布的TROPION-Lung 01研究是ADC在肺癌领域首个获得阳性结果的Ⅲ期临床研究。在此次ASCO第一三共又公布了ICARUS-LUNG01的研究结果(口头报告#8501)。
ICARUS-LUNG01是一项多中心、单臂的Ⅱ期临床研究,针对经靶向治疗、免疫治疗和铂类化疗失败后的晚期NSCLC患者,通过连续组织活检和生物标记物分析来预测治疗效果。累计100例患者接受Dato-DXd 治疗,其中82%为非鳞癌患者。每3周给予受试患者6mg/kg的Dato-DXd静脉注射治疗,受试者在基线、治疗中和治疗后接受活检,主要研究终点为经评估确认的客观缓解率(ORR)。
图1. ICARUS-LUNG01研究结果
图片来源:ASCO 2024口头报告
有效性方面
截至2024年4月18日,94%的患者终止治疗,77%的患者出现疾病进展。
总人群中,全组患者ORR为26%,非鳞癌和鳞癌患者ORR分别为30.0%和5.6%;
全组中位PFS为3.6个月,非鳞癌和鳞癌患者的中位PFS分别为4.8个月和2.9个月;
全组患者中位OS为11.9个月,非鳞癌和鳞癌患者的中位OS分别为12.6个月和6.3个月。
在多线治疗的患者人群中,Dato-Dxd展示了与之前TROPION-Lung01研究相似的疗效及安全性,对于非鳞状NSCLC患者获益明显更大。
安全性方面
入组患者3级以上治疗相关不良反应(TRAE)发生率为25%,较常见的为口腔黏膜炎和恶心,1例患者出现间质性肺改变。
这一点上,与第一三共另一款畅销的德曲妥珠单抗(T-DXd)可能具有相同的安全风险。
基因表达改变方面
通过对收集到的97例基线肿瘤样本分析,78例有TROP2表达,71例存在疗效或耐药相关基因的改变。在治疗第三周或第六周收集了81例样本,66例出现基因表达改变;治疗结束后收集的15例样本中,5例出现基因表达改变。
ICARUS-LUNG01最大的特点在于,为了探究基因改变与Dato-DXd治疗疗效及耐药性的潜在关联,研究人群包含了伴AGA人群与non-AGA人群,对患者类型进行了更广泛的探索。
生物标志物与疗效方面
TROP2表达组织化学评分结果显示,从 Dato-Dxd单药治疗获益的TROP2表达范围较广。研究结果显示,肿瘤驱动基因的改变与Dato-Dxd治疗疗效或耐药之间没有显著关联。通过对治疗无应答患者的基线和治疗期间组织活检的样本进行RNA-seq分析,研究者发现DNA修复、激活和免疫相关途径的抑制可能与Dato-Dxd耐药有关(p < 0.05)。
图2:TROP2表达结果与PFS关联性分析
图片来源:ASCO 2024口头报告
该研究验证了Dato-DXd在经治晚期NSCLC的治疗价值,或为晚期NSCLC患者提供后线治疗新选择。同时,该研究也揭示了生物标志物与疗效间的关系,选择合适的生物标志物或有助于提高ADC药物的疗效。
除了TROP2 ADC,其他靶点ADC也在NSCLC治疗中展现潜力,例如辉瑞的IB6靶向ADC药物Sigvotatug vedotin(SV)、艾伯维的c-MET靶向ADC药物Teliso-V。未来ADC药物有望成为NSCLC治疗的重要药物类型。
表1:其他ADC针对NSCLC的试验结果
药物名称
Sigvotatug vedotin (SV)
Teliso-V
试验名称
SGNB6A-001
LUMINOSITY
靶点
整合素β6(IB6)
c-MET
试验阶段
Ⅰ期
单臂Ⅱ期
入组患者
C 部分:Sigvotatug vedotin与帕博利珠单抗联合治疗 NSCLC
c-Met蛋白过度表达、EGFR野生型、晚期/转移性非鳞状NSCLC患者
入组病例数
113例
172例
ORR
整体:19.5%未接受过紫杉烷治疗的非鳞状NSCLC患者:32.5%
整体:28.6%;c-Met 高表达:34.6%;c-Met 中表达:22.9%
主要终点
根据RECIST v1.1进行独立中心审查的总体缓解率(ORR)
根据RECIST v1.1进行独立中心审查的总体缓解率(ORR)
结论
Sigvotatug vedotin在NSCLC患者中继续显示出令人鼓舞的抗肿瘤活性和可控的安全性。目前辉瑞已经启动关键性3期临床试验,评估这款ADC作为二线或三线疗法,治疗非鳞状NSCLC患者的效果。
Teliso-V 在c-Met蛋白过度表达、EGFR野生型、晚期/转移性非鳞状NSCLC患者中显示出积极的反应,尤其是在 c-Met 高表达的患者中。
安全性
NSCLC患者中大于3级的TEAE比例为46.0%,导致停药的TEAE比例为13.3%。最常见的大于3级的TEAE是呼吸困难(9.7%)、疲劳(7.1%)和中性粒细胞减少症(5.3%)。一名NSCLC患者出现治疗相关死亡(肺炎)。
最常见TRAE是周围感觉神经病变 (30%)、外周水肿 (16%) 和疲劳 (14%),5级 TRAE发生2例(间质性肺病、呼吸衰竭)。
PD-1+ADC
有望改变NSCLC一线治疗格局
今年ASCO,晚期NSCLC治疗领域,PD-1+ADC成为关注热点。两个热门ADC:Dato-Dxd和SKB264都公布了其与PD-(L)1联用的数据。
Dato-Dxd + Keytruda
第一三共还公布了Dato-Dxd联合PD-1抗体一线治疗晚期NSCLC的1b期临床试验TROPION-Lung02的亚组更新数据,这是目前PD-1+ADC联合一线治疗NSCLC的最大研究。
结果显示,Keytruda联合Dato-Dxd一线治疗,对于PD-L1≥50%的患者ORR高达100%。该研究为PD-1联合ADC取代目前PD-1加化疗的一线治疗注入了信心。
图3:TROPION-Lung02的亚组更新数据
图片来源:ASCO 2024海报
SKB264+KL-A167
科伦博泰报告了SKB264联合PD-L1单抗KL-A167在晚期NSCLC患者(OptiTROP-Lung01,NCT05351788)中的Ⅱ期研究的初步结果(口头报告#8502)。
Sacituzumab Tirumotecan (SKB264/MK-2870,芦康沙妥珠单抗)是由科伦博泰与默沙东联合开发的新型ADC,也是一种 TROP2 ADC,由人源化TROP2单抗SKB264、经优化的CL2A连接子与自研小分子T030组成。T030活性与Dxd相当,且具有旁观者效应。
图4:SKB264结构
图片来源:科伦博泰
截至2024年1月2日,共纳入103例未曾接受过治疗的、驱动基因突变阴性的晚期NSCLC患者,并按非随机方式分为1A组和1B组。1A组入组40人,治疗方案为SKB264 5 mg/kg Q3W + KL-A167 1200 mg Q3W;1B队列入组63例患者,治疗方案为SKB264 5 mg/kg Q2W + KL-A167 900 mg Q2W,直至疾病进展或无法耐受治疗,试验中按照RECIST 1.1 标准每6周进行评估。
表2:SKB264治疗患者PD-L1表达情况
分组
<1%
1%-49%
≥50%
1A
30.00%
32.50%
37.50%
1B
33.30%
30.20%
36.50%
研究结果如下:
药物名称
1A组
1B组
入组人数
40
63
治疗方案
SKB264 5mg/kg Q3W + KL-A167 1200 mg Q3W
SKB264 5mg/kg Q2W + KL-A167 900 mg Q2W
ORR
48.6%(18/37, 2例待确认)
77.6%(45/58, 5例待确认)
DCR
94.60%
100%
mPFS
15.4个月(95% CI: 6.7, NE)
未达到
6月PFS率
69.20%
84.60%
安全性方面,最常见的3级以上TRAE为中性粒细胞计数降低(30.0% /30.2%)、WBC降低(5.0% /17.5%)、贫血(5.0% /15.9%)、皮疹(5.0% /6.3%)及药疹(7.5% /0)。1B队列的1名患者因出现超敏反应导致停药的治疗相关不良事件,但并无出现治疗相关死亡事件。
SKB264联合KL-A167在初治晚期NSCLC中显示出良好的疗效,安全性可控。三项由默沙东主导的SKB264联合帕博利珠单抗的全球3期研究也正在进行,适应症分别为一线治疗转移性鳞状NSCLC患者(NCT06422143)、PD-L1表达≥50%的转移性NSCLC患者(NCT06170788)以及未获得病理完全缓解的可切除NSCLC患者(NCT06312137)。
结语
近年来,ADC在NSCLC治疗领域开始崭露头角,部分药物已进入上市申报阶段,未来进展值得期待。
TROPION-Lung 01是ADC药物在肺癌领域对比多西他赛首个取得阳性试验结果的研究,给ADC在NSCLC治疗领域的全面铺开吹响了号角,也为NSCLC免疫靶向耐药后的治疗提供了一个潜在的解决方案。基于TROPION-Lung 01的试验结果,Dato-Dxd生物制品许可申请于2024年2月19日获得美国FDA受理。而科伦博泰的SKB264作为国内自主研发的TROP2-ADC,获得了CDE的两项突破性疗法认定,有望成为首个在国内上市的TROP2-ADC。
此外,Dato-Dxd和SKB264联合免疫抑制剂治疗非鳞癌NSCLC的积极成果或将改变晚期NSCLC的治疗格局。
来源 | 博药(药智网获取授权转载)
撰稿 | 泠然
责任编辑 | 八角
声明:本文系药智网转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。
商务合作 | 王存星 19922864877(同微信)
阅读原文,是受欢迎的文章哦
ASCO会议抗体药物偶联物临床结果免疫疗法临床3期
2024-06-04
·米内网
精彩内容
近日,科伦药业的骨化三醇软胶囊获批上市、塔戈利单抗一线适应症申报NDA、芦康沙妥珠单抗最新研究结果公布……今年以来,科伦药业已有6个品种获批上市,累计137个品种过评(45个首家),26个品种备战第十批集采。目前公司有35款新药(21款1类新药)处于申报临床及以上研发阶段;66个新分类报产品种在审,18个暂无首仿获批。
拿下6大重磅品种,137个品种过评
5月27日,NMPA官网显示,科伦药业以仿制4类报产的骨化三醇软胶囊获批生产并视同过评,为国产第6家。骨化三醇软胶囊是一种活性维生素D3类似物,为国家医保乙类品种。米内网数据显示,2023年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端骨化三醇软胶囊销售额超过7亿元。
今年以来,科伦药业已有6个品种获批生产并视同过评,包括骨化三醇软胶囊、复方氨基酸注射液(18AA-Ⅶ)、吡拉西坦注射液、奥拉帕利片、艾曲泊帕乙醇胺片、ω-3甘油三酯(2%)中/长链脂肪乳/氨基酸(16)/葡萄糖(16%)注射液。
2024年至今科伦药业获批品种来源:米内网中国申报进度(MED)数据库
6个品种中,多个品种为国内首批上市,彰显了公司的研发实力。其中,艾曲泊帕乙醇胺片、ω-3甘油三酯(2%)中/长链脂肪乳/氨基酸(16)/葡萄糖(16%)注射液为国内首仿,奥拉帕利片为国产第2家,复方氨基酸注射液(18AA-Ⅶ)为国产第4家,骨化三醇软胶囊为国产第6家。
截至目前,科伦药业已有137个品种通过/视同通过一致性评价。其中,45个品种为国内首家过评,阿奇霉素分散片、氨基酸葡萄糖注射液、钆特醇注射液、琥珀酸曲格列汀片、泊沙康唑口服混悬液、氢溴酸替格列汀片、氢溴酸西酞普兰胶囊等16个品种为独家过评。
科伦药业通过/视同通过一致性评价品种
第十批集采即将启动,科伦药业已有26个过评品种满足集采门槛,符合申报资格企业数达5家及以上。26个品种涉及15个注射剂、9个口服常释剂型,多个品种为2023年以来新获批品种,若被纳入第十批集采,有望借助集采中标快速打开市场。
21款1类新药在研,4款新药上市可期
近年来科伦药业持续推进“创新驱动”战略,加大力度支持药品研发创新,2022年研发费用17.95亿元,同比增长3.37%;2023年研发费用19.44亿元,同比增长8.27%。
科伦药业研发费用情况(单位:亿元)
今年以来,科伦药业有一款1类新药塔戈利单抗注射液(一线治疗鼻咽癌)申报上市,此前该新药的三线治疗鼻咽癌适应症已申报上市;2款1类新药注射用SKB501、注射用SKB518相继申报临床。
国际化方面,SKB264/MK2870项目(TROP2-ADC,芦康沙妥珠单抗)大放异彩:合作伙伴MSD启动该药非小细胞肺癌及子宫内膜癌等三项全球三期临床试验,公司收到里程碑款7500万美金;一线治疗PD-L1阴性TNBC获国家药监局突破性疗法认定;分别在2024 AACR和2024 ASCO年会上公布研究成果。此外,KL590586(RET抑制剂)获美国FDA授予快速通道资格认定。
目前科伦药业主要有35款新药处于申报临床及以上阶段,涉及21款1类新药、12款2类改良型新药、2款生物类似药,聚焦肿瘤、精神神经、心血管、肝病等疾病领域,涵盖小分子、单抗、双抗、ADC等药物形式。
科伦药业主要在研新药
35款新药中,3款1类新药A167/塔戈利单抗注射液(PD-L1单抗)、注射用A166(HER2-ADC)、注射用SKB264(TROP2-ADC)及生物类似药西妥昔单抗注射液(A140注射液)已申报NDA,上市可期。
值得一提的是,A167是公司首个申报上市的1类新药,也是全球首个针对鼻咽癌适应症申报NDA的PD-L1单抗,有望于今年获批上市,实现1类新药“零”的突破。A140注射液是国内首款申报上市的西妥昔单抗生物类似药,有望拿下首仿。
66个新品抢攻230亿市场,18个首仿冲刺
在仿制药方面,目前科伦药业还有66个新注册分类品种上市申请在审,形成了梯度丰富的研发管线。66个品种获批生产后将视同通过一致性评价,主要集中在血液和造血系统药物(14个)、消化系统及代谢药(12个)、全身用抗感染药物(8个)、抗肿瘤和免疫调节剂(8个)。
66个品种2023年在中国公立医疗机构终端的销售额合计接近230亿元。其中,结构脂肪乳注射液(C6-24)、罗沙司他胶囊、碘普罗胺注射液、地屈孕酮片、麦考酚钠肠溶片、盐酸乌拉地尔注射液等6个品种的销售额均超过10亿元。
科伦药业新注册分类在审且暂无首仿获批的品种
18个品种暂无首仿(含剂型首仿)获批上市,包括恩扎卢胺片、罗替高汀贴片、阿帕他胺片、黄体酮阴道缓释凝胶、芦曲泊帕片、丁酸氯维地平脂肪乳注射液、奈妥匹坦帕洛诺司琼胶囊、西尼莫德片等,科伦药业将与多家企业竞争国内首仿。
此外,棕榈酸帕利哌酮注射液、阿戈美拉汀片、布比卡因脂质体注射液、达可替尼片等13个品种获批国产企业数均只有1家,他克莫司缓释胶囊、阿瑞匹坦注射液、麦考酚钠肠溶片等9个品种获批国产企业数均只有2家,公司有望实现国内首批上市。
资料来源:米内网数据库、公司公告注:米内网《中国公立医疗机构药品终端竞争格局》,统计范围是:中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院,不含民营医院、私人诊所、村卫生室;上述销售额以产品在终端的平均零售价计算。
本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。投稿及报料请发邮件到872470254@qq.com稿件要求详询米内微信首页菜单栏商务及内容合作可联系QQ:412539092
【分享、点赞、在看】点一点不失联哦
一致性评价上市批准带量采购
100 项与 TROP2 ADC(luzsana) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肿瘤 | 临床前 | 美国 | 2024-03-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
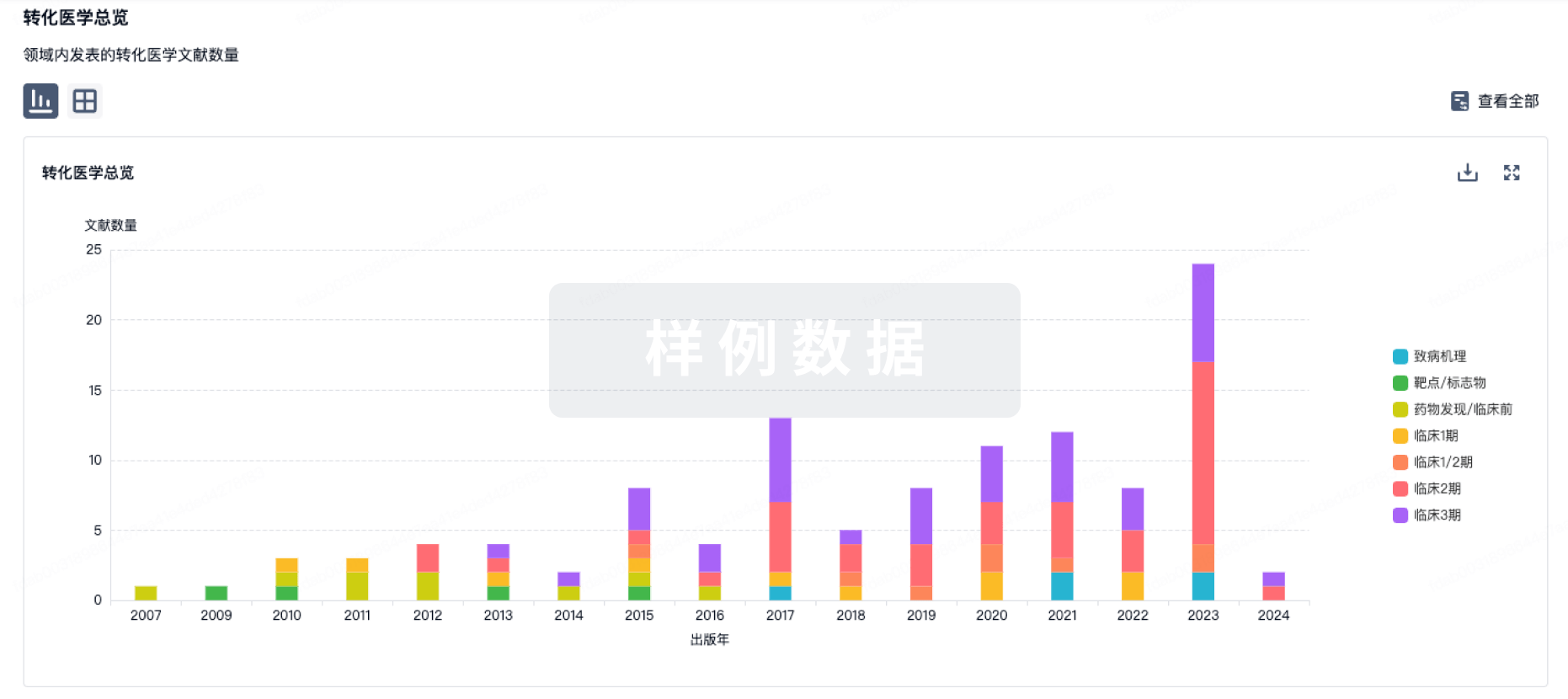
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
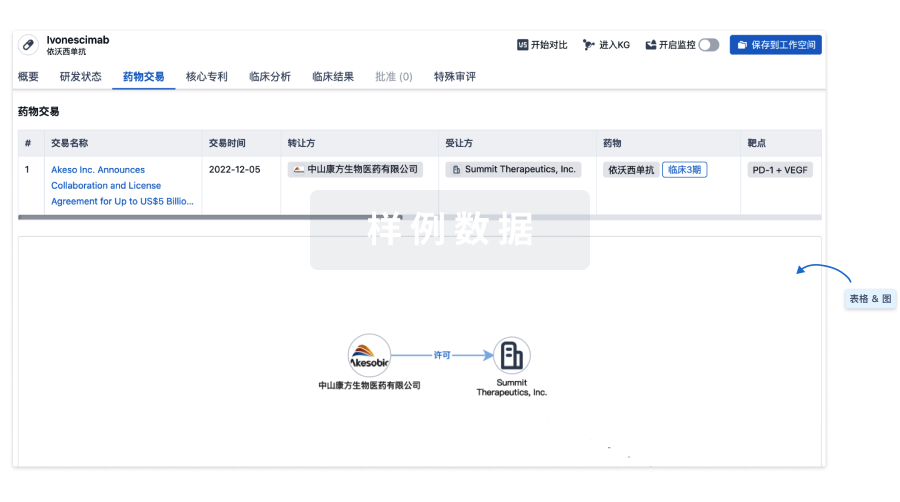
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
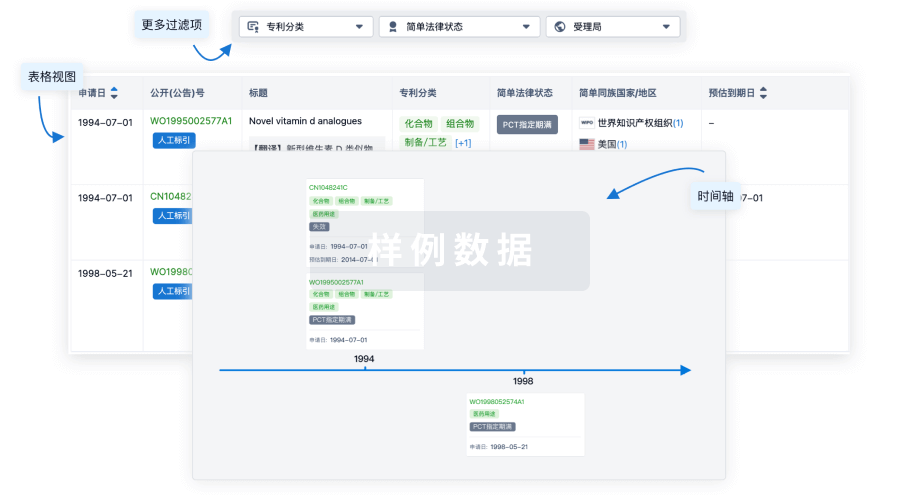
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
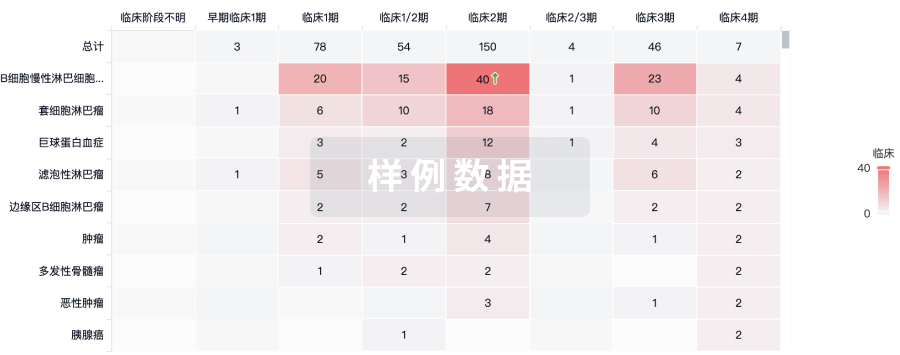
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
