预约演示
更新于:2025-09-06
Zerlasiran
更新于:2025-09-06
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
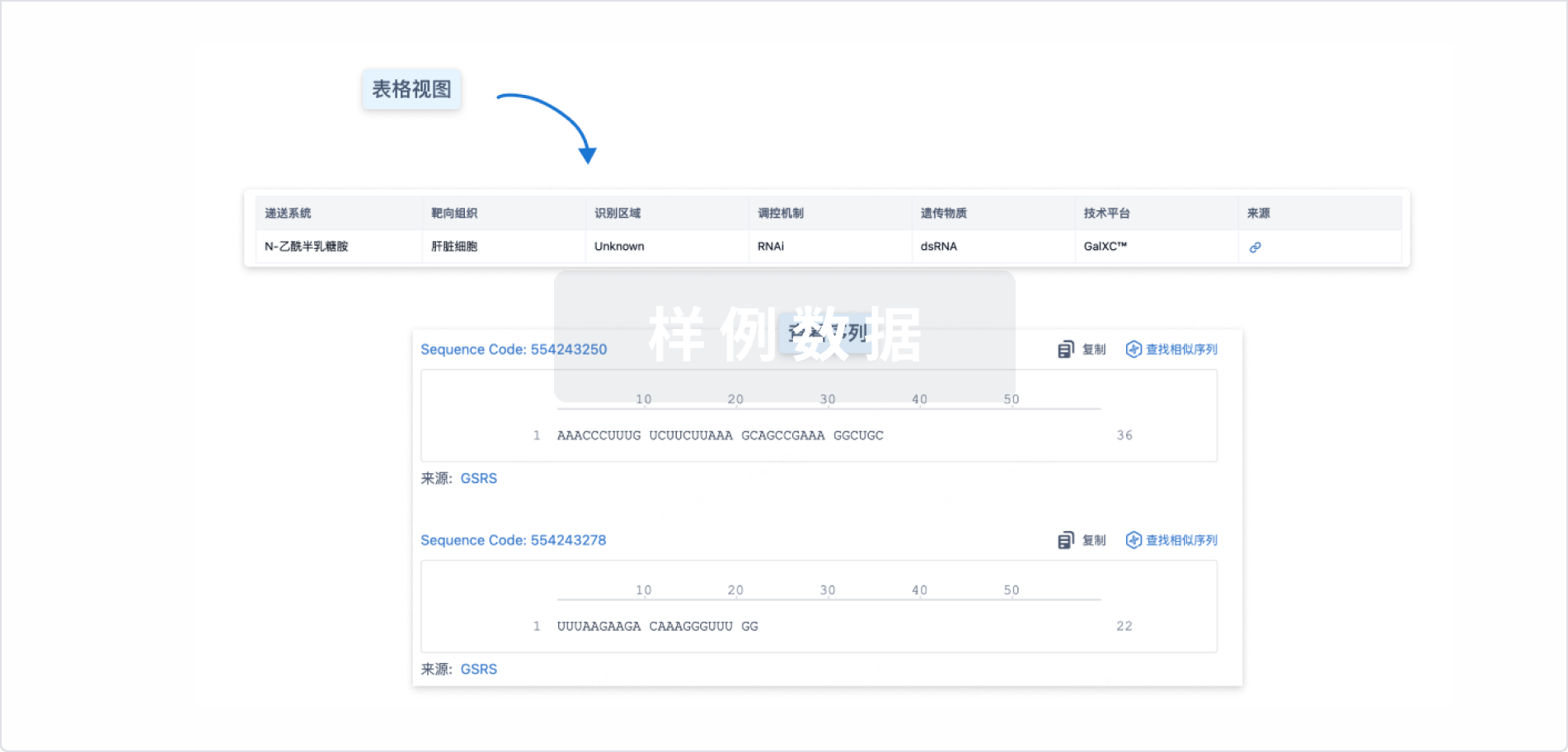
Sequence Code 452929085

来源: *****
Sequence Code 452929086

来源: *****
关联
3
项与 Zerlasiran 相关的临床试验JPRN-jRCT2051240068
A Trial to Evaluate the Pharmacokinetics, Pharmacodynamics, and Safety and Tolerability of Zerlasiran in Japanese Subjects With Elevated Serum Lipoprotein(a)
开始日期2024-05-16 |
申办/合作机构- |
NCT05537571
A Multi-centre, Randomised, Double-blind, Placebo-controlled, Phase 2 Study to Investigate Efficacy, Safety and Tolerability of SLN360 in Participants With Elevated Lipoprotein(a) at High Risk of Atherosclerotic Cardiovascular Disease Events
Phase 2 study to evaluate the efficacy, safety and tolerability of SLN360 administered subcutaneously (SC) compared with placebo in adult participants with elevated lipoprotein(a) at high risk of atherosclerotic cardiovascular disease events
开始日期2022-12-13 |
申办/合作机构 |
NCT04606602
A Randomised, Double-blind, Placebo Controlled, First-in-human Study to Investigate the Safety, Tolerability, Pharmacokinetic and Pharmacodynamic Response of SLN360 in Subjects With Elevated Lipoprotein(a)
This study will investigate the safety and tolerability of SLN360 in patients with elevated Lp(a).
开始日期2020-11-18 |
申办/合作机构 |
100 项与 Zerlasiran 相关的临床结果
登录后查看更多信息
100 项与 Zerlasiran 相关的转化医学
登录后查看更多信息
100 项与 Zerlasiran 相关的专利(医药)
登录后查看更多信息
22
项与 Zerlasiran 相关的文献(医药)2025-12-01·Current Atherosclerosis Reports
Highlights of Cardiovascular Disease Prevention Studies Presented at the 2024 American Heart Association Scientific Sessions
Review
作者: Khoja, Adeel ; Inam, Maha ; Murthy, Nikitha ; Epstein, Elizabeth ; Virani, Salim S ; Vaughan, Elizabeth ; Sheikh, Sana ; Mehta, Sandeep ; Minhas, Abdul Mannan Khan ; Slipczuk, Leandro ; Junaid, Vashma ; Chai, Zohar ; Hermel, Melody ; Hinkamp, Colin
PURPOSE OF REVIEW:
Focused review highlighting ten select studies presented at the 2024 American Heart Association (AHA) Scientific Sessions.
RECENT FINDING:
Included studies assessed effects of intensive blood pressure control in patients with type 2 diabetes (BPROAD); decision support system for physicians to optimize early lipid lowering therapies after acute coronary syndrome (ZODIAC); efficacy and safety of zerlasiran, a short interfering RNA targeting lipoprotein(a) (ALPACAR); efficacy and safety of muvalaplin an oral disrupter of the assembly of lipoprotein(a) particles (KRAKEN); safety and efficacy of obicetrapib in patients with heterozygous familial hypercholesterolemia (BROOKLYN); efficacy and safety of lerodalcibep, a third generation PCSK9 inhibitor in heterozygous familial hypercholesterolemia subjects (LIBerate-HeFH_OLE); personalized app-based coaching to improve physical activity in patients with HFpEF compared to standard care (MyoMobile); semaglutide to improve cardiovascular outcomes in patients with a history of coronary artery bypass surgery and overweight or obesity (the SELECT trial); efficacy and safety of plozasiran in adults with genetically or clinically defined familial chylomicronemia syndrome at high risk of acute pancreatitis (PALISADE); and transcriptomic signatures and predictors of evolocumab added to maximum statin therapy based on intra-coronary plaque characteristics (YELLOW III). Research presented at the 2024 AHA Scientific Sessions emphasized innovative strategies in cardiovascular disease prevention and management.
2025-06-01·DIABETES OBESITY & METABOLISM
Comprehensive evaluation of siRNA therapeutics on Lp(a): A network meta‐analysis
Review
作者: Hu, Jiaqiang ; Wang, Xingjin ; Qin, Xiaoli ; Liu, Song ; Zhao, Chen
Abstract:
Aims:
To evaluate the efficacy and safety of siRNA drugs that lower Lp(a) in patients with dyslipidaemia.
Materials and Methods:
A network meta‐analysis and systematic review were conducted to compare siRNA drugs targeting Lp(a), based on relevant randomized controlled trials (RCTs). A comprehensive search was performed in PubMed, Embase, Web of Science and the Cochrane Library (up to October 24, 2024). RCTs with an intervention duration of at least 12 weeks were included. Eligible studies compared siRNA drugs that reduce Lp(a), including both Lp(a)‐targeted and non‐targeted agents, with placebo or other siRNA drugs that reduce Lp(a). The primary outcomes were the percentage reduction and absolute reduction in Lp(a), percentage reduction in low‐density lipoprotein cholesterol (LDL‐C), percentage reduction in apolipoprotein B (apo(B)), adverse events and serious adverse events, including injection‐site reactions. The risk of bias was assessed using the Cochrane Risk of Bias Tool (ROB2), and a random‐effects network meta‐analysis was performed using the frequentist approach. Confidence in effect estimates was evaluated using the Confidence In Network Meta‐Analysis (CINeMA) framework.
Results:
A total of 14 trials involving 5646 participants were included. Lp(a)‐targeted siRNA agents, particularly Olpasiran, demonstrated strong efficacy in significantly reducing Lp(a) levels, with the greatest percentage reduction in Lp(a) (mean difference [MD]: −92.06%; 95% CI: −102.43% to −81.69%; P‐score: 0.98). Olpasiran also showed the greatest absolute reduction in Lp(a) (MD: −250.70 nmol/L; 95% confidence interval [CI]: −279.89 to −221.50; P‐score: 0.99). Certain non‐Lp(a)‐targeted siRNA agents, such as inclisiran and zodasiran, also showed modest reductions in Lp(a) levels, reducing Lp(a) by approximately 15%. Lp(a)‐targeted siRNA agents reduced LDL‐C by more than 20% and decreased apo(B) by approximately 15%. In terms of safety, most drugs exhibited favourable safety profiles with no significant differences compared to placebo. However, zerlasiran raised concerns regarding injection‐site reactions and other adverse events when compared to placebo.
Conclusions:
Lp(a)‐targeted siRNA agents have shown robust effectiveness in substantially reducing Lp(a) levels, including both percentage and absolute reductions, with moderate improvements in LDL‐C and apo(B) concentrations. Non‐Lp(a)‐targeted siRNA agents also demonstrate modest reductions in Lp(a) levels. The safety profile is generally favourable, but zerlasiran and inclisiran may increase the incidence of injection‐site reactions.
2024-12-17·JAMA-JOURNAL OF THE AMERICAN MEDICAL ASSOCIATION
Zerlasiran—A Small-Interfering RNA Targeting Lipoprotein(a)
Article
作者: Schwartz, Gregory G. ; Ray, Kausik K. ; Rambaran, Curtis ; Troquay, Roland ; Dorresteijn, Jannick A. N. ; Stroes, Erik S. G. ; Nicholls, Stephen J. ; Rider, David A. ; Wang, Qiuqing ; Navar, Ann Marie ; Szarek, Michael ; Fok, Henry ; Nissen, Steven E. ; Wolski, Kathy ; Romano, Steven
Importance:
Elevated lipoprotein(a) increases the risk of atherosclerotic cardiovascular disease (ASCVD) and aortic stenosis.
Objective:
To evaluate the effects of zerlasiran, a small-interfering RNA targeting hepatic synthesis of apolipoprotein(a), on lipoprotein(a) serum concentration.
Design, Setting, and Participants:
A multicenter trial in patients with stable ASCVD with serum lipoprotein(a) concentrations greater than or equal to 125 nmol/L at 26 sites in Europe and South Africa between January 3, 2023, and April 27, 2023, with last follow-up on July 1, 2024.
Interventions:
Participants randomized to receive a subcutaneous dose of placebo every 16 weeks for 3 doses (n = 23) or every 24 weeks for 2 doses (n = 24) or zerlasiran 450 mg every 24 weeks for 2 doses (n = 45), 300 mg every 16 weeks for 3 doses (n = 42), or 300 mg every 24 weeks for 2 doses (n = 44).
Main Outcome and Measures:
The primary outcome was the time-averaged percent change in lipoprotein(a) concentration from baseline to 36 weeks, with follow-up to 60 weeks.
Results:
Among 178 patients, mean (SD) age was 63.7 (9.4) years, 46 (25.8%) were female, with a median (IQR) baseline lipoprotein(a) concentration of 213 (177-282) nmol/L; 172 patients completed the trial. Compared with the pooled placebo group, the least-squares mean time-averaged percent change in lipoprotein(a) concentration from baseline to week 36 was −85.6% (95% CI, −90.9% to −80.3%), −82.8% (95% CI, −88.2% to −77.4%), and −81.3% (95% CI, −86.7% to −76.0%) for the 450 mg every 24 weeks, 300 mg every 16 weeks, and 300 mg every 24 weeks groups, respectively. Median (IQR) percent change in lipoprotein(a) concentration at week 36 was −94.5% (−97.3% to −84.2%) for the 450 mg every 24 weeks group, −96.4% (−97.7% to −92.3%) for the 300 mg every 16 weeks group, and −90.0% (−93.7% to −81.3%) for the 300 mg every 24 weeks group. The most common treatment-related adverse effects were injection site reactions, with mild pain occurring in 2.3% to 7.1% of participants in the first day following drug administration. There were 20 serious adverse events in 17 patients, none considered related to the study drug.
Conclusions:
Zerlasiran was well-tolerated and reduced time-averaged lipoprotein(a) concentration by more than 80% during 36 weeks of treatment in patients with ASCVD.
Trial Registration:
ClinicalTrials.gov Identifier: NCT05537571
113
项与 Zerlasiran 相关的新闻(医药)2025-09-04
·研发客
Citeline首席分析师周淑华发言
圆桌现场
研发客主编毛冬蕾与张江全互动
张金晶 威斯津生物合伙人商务发展总监
李安康 腾盛博药CFO
尹思远 传信生物首席运营官
王松立 星核迪赛研发总监
陈进 维亚臻生物临床药理&转化医学副总裁
高璐 圆因生物CEO
张震 徕博科亚太商务开发高级总监
Simon Yu 徕博科中国中心实验室运营总监
研讨会现场图片分享
舶望制药近日与诺华制药就4款小核酸药物达成1.6亿美元预付款的消息,再次证明小核酸药物成为备受关注的热门赛道。全球众多企业布局,中国一批“黑马”公司正凭借独特的技术平台和差异化的管线布局悄然崭露头角。在由研发客与徕博科联合举办的“中国分子,世界引擎”研讨会上,该领域的发展前景成为焦点。
拓展阅读
舶望再度授权诺华siRNA药物,总交易价值达52亿美元!
李勇:在心血管疾病领域前景广阔
复旦大学华山医院心脏科李勇教授认为,小核酸药物在心血管疾病防治领域正展现出较大潜力。英克司兰(Inclisiran)的成功获批,验证了这一领域的重要性。
小核酸药物在递送系统方面取得了进展。除了目前已经广泛应用的肝细胞递送系统外,通过优化递送载体,科学家已实现了对卵巢细胞、肾脏细胞及脑细胞的有效靶向递送。李勇教授认为,针对脑细胞的靶向递送技术有望在短期取得突破,这为小核酸药物在心血管神经系统疾病的应用提供了可能。
复旦大学华山医院心脏科 李勇教授
心血管疾病如高血压、血脂异常和糖尿病等,多为慢性病,不仅在中国,在全球也有数以亿计的大量患者,而且需要长期维持治疗。李勇教授指出:“糖尿病患者中45%的死亡与心血管疾病相关,而非高血糖本身。慢性肾脏病患者进入透析后,无论在是否已经接受透析治疗,心血管事件也是其首要死因,占比超40%。近10年来越来越受关注的脂肪肝,已经超越消化系统,与糖尿病及慢性炎症密切关联,也会导致心血管疾病风险增高。因此,维护心血管健康是内科疾病防控预防和管理的关键策略。”
“心血管事件链”概念于1991年由美国医学科学院院长魏德照Victor Dzao提出,强调从危险因素发展为冠心病、心衰的连续过程中的全程疾病管理及危险因素控制。李勇教授解释,高血压、糖尿病和血脂异常是三大主要危险因素,它们通过激活体内RAAS、炎症、能量/线粒体代谢等某些系统,促使动脉粥样硬化斑块形成和发展、以及心肌、肾脏、血管的纤维化加速进展。
关于高血压,他表示:“高血压不仅造成物理损伤,还会激活某些系统,引起左心室肥厚和舒张功能障碍。中国高血压患者众多,每年约260万人因高血压而此死亡,我国的高血压人口数和死亡人数均居全球之首。目前美国诊断标准为130/80 mmHg,而中国仍采用140/90 mmHg,这在一定程度上影响了防控效果。”
在血脂方面,他说:“LDL-C是动脉粥样硬化的主要致病性危险因素,根据我国著名心血管流行病学家北京安贞医院赵冬教授团队15年的队列研究数据,其升高对心肌梗死风险的贡献达77%。大量随机对照临床试验证实,显著降低LDL-C水平不仅能是防治心血管病的关键,还能降低全因死亡,延长寿命。”对于糖尿病与脂肪肝,他强调这两类患者的心血管风险增加,脂肪肝患者尤其易合并心血管疾病,导致临床结局恶化,建议心血管医生应更多关注这类人群的心血管健康。
在血脂管理方面,他特别提到英克司兰(Inclisiran):“作为一种靶向PCSK9的小干扰RNA药物,英克司兰通过阻断PCSK9与LDL受体的结合,增加肝细胞表面LDL受体的数量,提升肝细胞清除LDL-C的能力,从而降低血中的LDL-C水平。其独特之处在于,一次注射可维持长达6个月的疗效,大大提高了患者的治疗依从性。临床试验表明,英克司兰单药治疗或与他汀联用,均可降低LDL-C幅度高达水平60%,且安全性良好。”
他还介绍了其他小核酸药物的研究进展:“除了英克司兰外,针对甘油三酯(TG)和脂蛋白(a) [Lp(a)]的小核酸药物也展现出广阔的应用前景。例如,针对ApoC-III的小核酸药物Plozasiran、针对ANGPLT-3的Zodasiran可降低TG水平,并减少急性胰腺炎的发作风险;除了Plecarsen外、多个针对Lp(a)的小核酸药物如Olpasiran、Lepodisiran则可降低其水平达90%以上,有望减少心血管事件的发生。”
在强化降压与降脂治疗的临床意义方面,李勇教授表示:“近年来,多项大规模临床试验表明,将血压控制在更低水平(如收缩压<120 mmHg)可降低心血管事件和死亡率。然而,中国的高血压管理目标值仍为140/90 mmHg,这在一定程度上限制了降压治疗的获益。因此,推动高血压管理目标的下调,对于改善中国心血管疾病防治现状具有重要意义。”小核酸药物在降压领域也有明显的进展,Zilebesiran的II期临床试验显示,每6月一次皮下注射,可获得令人相当满意的降压效果,针对高血压患者的心血管结局随机对照临床试验(CVOT)ZENITH研究已经启动。
他还强调了早期降脂治疗的重要性:“LDL-C的累积暴露时间与动脉粥样硬化的发展密切相关。因此,越早启动降脂治疗并维持较低水平,对心血管的保护作用越大。小核酸药物的出现,为实现长期、稳定的降脂治疗提供了新的手段。”
最近,Lancet发表了小核酸药物用于治疗脂肪肝的II期临床试验结果,ION224-CS2试验表明,采用肝活检来评估,寡核苷酸制剂抑制DGAT-2,能够有效逆转脂肪肝,安全性良好。
展望未来,李勇教授认为小核酸药物在一级预防和多靶点治疗方面具有广阔前景。然而,李勇教授也指出了小核酸药物面临的挑战:例如,如何进一步提高递送效率、降低脱靶效应、优化给药方案等。此外,加强医生和患者对小核酸药物的认知也是推动其应用的关键。
最后,他总结道:“小核酸药物为心血管疾病防治带来了新希望。通过不断优化技术、拓展适应症和加强临床应用研究,相信小核酸药物将在未来心血管疾病防治中发挥越来越重要的作用。”
周淑华:全球核酸药物研发持续活跃
Citeline首席分析师周淑华博士介绍了2025年全球核酸药物研发持续活跃的态势。
Citeline首席分析师 周淑华博士
截至2025年,全球处于活跃开发阶段的药物总数达23,875种,较上一年度增长4.6%,新增药物1,050种,其中4,546种为新加入研发管线的药物。新增药物中,抗癌药占比38.8%,神经系统疾病药物占13.8%。各临床阶段药物数量均增长,Ⅰ期增长6.8%,Ⅱ期增长6.3%,Ⅲ期增长8.8%,临床前研究阶段增长1.8%(低于2024年的5.5%),显示全球研发活跃但临床前研究增速放缓。
核酸药物研发管线中,肿瘤学仍是最大治疗领域,2025年有9,746种药物在研,增长3.7%,占所有在研药物的39.7%(略低于2024年的40.1%)。神经系统疾病药物研发增长率低于平均水平(2024-2025年仅增长4.2%)。顶尖企业中,辉瑞重新夺回研发管线规模榜首,罗氏和诺华紧随其后。前十家企业贡献5.4%的在研药物,前25家贡献10.0%,剩余19.4%来自仅有一两种药物在研的公司。
疾病聚焦方面,乳腺癌仍是研发重点,管线规模增长9.5%,领先于非小细胞肺癌(NSCLC,增长10.0%)。非癌症领域中,新冠病毒退出前十,阿尔茨海默病仍是唯一进入前十的非肿瘤疾病。肥胖治疗药物研发增长43.3%(受Wegovy和Mounjaro等药物影响)。热门药物蛋白靶点中,免疫疗法(I-O)相关靶点主导,CD3e连续第二年位居榜首,EGFR取代Her-2成为第二位热门靶点(应用于多种癌症治疗)。
全球及中国研发合作趋势显示,全球范围内16%的在研药物处于合作研发状态(抗癌药物领域16%,神经系统疾病药物16%,抗感染药物14%,消化/代谢系统疾病药物17%)。2017-2025年,中国合作交易数量和总金额2025年分别达16.4%和33.7%,但首付款比例普遍低于全球水平。
“未来,全球核酸药物研发将持续活跃,中国企业增长势头强劲。中国企业需提升创新效率、加强全球市场洞察、完善内部管理并构建健全的资本体系,以实现可持续发展。”周淑华说。
张江全:小核酸药物非临床安全评价要点
徕博科中国区早期研发负责人张江全剖析了小核酸药物非临床安全评价要点。
在结构与修饰上,siRNA药物可进行多种修饰,这会影响其药代动力学,免疫原性特性和毒性表现,介绍了非临床监管、药代动力学以及免疫原性三个方面的内容。
徕博科中国区早期研发负责人 张江全
小核酸药物的非临床监管主要遵循 ICH M3(R2)原则,标准遗传毒组合试验,一般毒性、DART、致癌性研究使用两种种属,同时需考虑ICH S6 指南部分终点。考虑到siRNA的临床给药周期,重复给药毒性研究周期较长,啮齿类动物 6 个月、非人灵长类 9 个月,对此,多国监管机构有相关原则。
在药代动力学方面,siRNA血浆半衰期短,快速被肝脏摄取,导致PK/PD分离现象。siRNA主要分布于肝脏且在肝组织中半衰期较长,肝脏药代动力学和RNA诱导沉默复合体(RISC)药代动力学是决定药效动力学及其持续时间的关键因素。免疫原性的潜在来源包括有序列依赖性免疫激活、递送系统影响等。
对于动物研究的毒性特征,包括免疫原性相关毒性,通过非 Toll 样受体途径触发促炎细胞因子释放;杂交依赖性毒性有靶点效应、脱靶效应、RNAi 机制饱和等;递送载体毒性方面,各种载体存在各自不同的毒性特征。
此外,张江全还分享了两个案例。一是已报道的SLN360案例,GalNAc结合的siRNA,靶向脂蛋白a mRNA,用于心血管疾病。研究通过GalNAc- 去唾液酸糖蛋白受体(ASGPR)结合实现肝脏特异性递送,旨在降低PLA,进行体外特异性和效力研究、体内生物分布研究(大鼠/食蟹猴)以及29天GLP毒性研究。结果显示,大鼠在不同剂量下,高剂量雌性大鼠体重略有下降,其他方面如食物摄入等无显著变化,观察到的非不良反应在停药8周后可恢复;食蟹猴在不同剂量下,体重等一般观察无SLN360相关影响,无补体激活或细胞因子释放,预期效果良好,非不良反应停药后也可恢复。
案例二是AAA(GalNAc结合的siRNA,用于非酒精性脂肪性肝炎(NASH)),研究每月1次皮下注射给大鼠和食蟹猴,持续12周,评估毒性并确定毒代动力学,观察停药12周后的恢复或持续情况。结果表明,系统暴露量与剂量成正比或高于剂量比,无药物蓄积和性别差异,临床观察未观察到AAA相关影响。临床病理主要为肝脏相关指标改变,镜检观察可见肝脏、淋巴结、胸腺、脾脏、肾脏、注射部位等出现色素沉着、空泡化、淋巴细胞减少等改变。所有病理发现均为轻度,认为是non-adverse,因此两个种属的NOAEL均为高剂量。
与会者表示这些全面的要点和案例分享,为小核酸药物非临床安全评价领域的研究提供了极具价值的参考。
徐中南:正大天晴进军小核酸药物领域
正大天晴药业集团的高级临床总监徐中南分享了正大天晴在小核酸药物开发中的技术演进路径,尤其聚焦TQA3038这一创新药的临床开发策略。
正大天晴药业集团的高级临床总监 徐中南
徐中南分析了慢乙肝治疗领域的严峻现状:中国慢乙肝患者诊断率仅22%,治疗率17%,市场需求迫切。尽管已有NUC和IFN等抗病毒药物,但抗病毒时间长、临床治愈率低的问题依旧突出,因此,针对HBV复制环节开发新药成为研究热点。
在介绍TQA3038时,徐中南阐述了其作为GalNAc偶联修饰siRNA药物的独特机制:“通过皮下注射特异性靶向HBV ORF-X区,有效抑制HBV复制。GalNAc配体与肝脏细胞的高亲和力和迅速内化能力,确保了siRNA的高效作用。”
临床试验方面,TQA3038一期健康受试者SAD研究共设置了6个剂量组,采用递增剂量设计确保安全。TQA3038给药后快速吸收,血浆浓度约4小时达峰,半衰期8.7至9.34小时,24小时内药物基本消除。6个剂量组安全性良好,未发生严重不良事件。需要重点关注ECG的改变情况。
TQA3038与同靶点药物相比的优势:同剂量下,TQA3038体内抗HBV活性优于Vir-2218,包括HBsAg、HBeAg、HBV RNA的下降比例;与ETV单药组相比,TQA3038和ETV联合给药组对小鼠血浆中HBV DNA的降低更明显。
在介绍同靶点药物联合干扰素治疗方案时,他分享了VIR-2218与PEG-IFNα联合治疗的研究成果,显示联合用药的受试者HBsAg下降幅度更大,部分受试者实现HBsAg转阴和血清学转换。同时,他也提及了AB-729与IFN联合治疗的研究进展。
针对TQA3038 Ⅱ期研究,评价TQA3038注射液联合NUC治疗经治慢乙肝患者的初步疗效及安全性。研究显示无严重不良事件发生,TQA3038可快速降低HBsAg水平,高剂量组效果更明显。
最后,他总结了TQA3038的技术演进路径和临床应用前景。TQA3038用药后在外周血浓度快速下降,48小时后检测不到,且GalNAc-siRNA可在肝脏中蓄积并缓慢释放,单次给药即可维持长期疗效,使其成为慢乙肝治疗领域的潜力创新药物。
毕吕存:生物分析策略从方法开发到全球一致性验证
徕博科执行总监及中国生物分析与亚太LCMS实验室负责人毕吕存博士探讨了小核酸药物的生物分析策略包括:药代动力学(PK)生物分析策略和生物标志物(BM)生物分析策略。
徕博科执行总监及中国生物分析与亚太LCMS实验室负责人 毕吕存博士
小核酸药物的基本结构是由20至30个核苷酸基团组成的短线性链,通过磷酸二酯键连接,具有强亲水性和高度负电荷性。在生物分析方法上,毕博士展示了定量分析小核酸药物的各技术手段,特别是液相色谱-质谱联用技术(LC-MS/MS)和高分辨率质谱(LC-HRMS)的应用。通过案例研究,可以利用这些技术对小核酸药物及其代谢物进行精确的定量分析。
针对小核酸药物的生物标志物分析,毕博士强调了评估药效动力学(PD)标志物或其他测量指标的重要性。小核酸药物在脏器组织中具有很长半衰期,能够保持很长疗效,因此评估其药效响应时需考虑组织分布和药效动力学特点。
此外,他还介绍了小核酸药物递送技术的创新,特别是GalNAc(N-乙酰半乳糖胺)递送技术能将小核酸递送至肝细胞,并通过化学修饰改善小核酸药物,很多生物科技公司更专注于肝外递送技术。优秀的生物分析技术能够提供答案,这些修饰后的小核酸药物能否有选择性地递送到达目标器脏,以及这些小核酸药物的体内分布和药效。
在方法开发方面,他介绍了小核酸药物生物分析中的各种困难, 以及解决这些困难的方法,特别是针对组织样品的处理和分析中的经验。通过案例研究,毕博士介绍了如何优化提取条件、色谱分离和质谱检测参数,以提高分析的灵敏度和准确性。
最后,毕博士总结了徕博科在小核酸药物生物分析的经验和成果,强调了多种生物分析工具(如LC-MS、qPCR、Simoa、ELISA、MSD和免疫捕获LC-MS)在支持小核酸药物PK/PD评估中的作用。“这些分析工具为药物设计和决策提供了关键数据,推动了小核酸药物的持续发展。”他说。
李海涛:炫景生物的创新实践
炫景生物联合创始人及CTO李海涛博士介绍了小核酸药物领域的全球研发环境、关键决策点和炫景生物的创新实践。
炫景生物联合创始人及CTO 李海涛博士
他认为,小核酸药物正迎来前所未有的机遇。全球范围内已有超过20款药物成功上市,且市场规模保持高速增长。在中国,小核酸药物开始显示出巨大潜力。
然而,小核酸Biotech公司也面临严峻的生存环境,一级市场融资金额大幅下滑,国内小核酸药热门靶点扎堆,siRNA领域内卷严重,进一步压缩了Biotech的生存空间。李海涛博士强调,Biotech公司是License-out交易项目的主要来源,其创新性在全球合作中发挥着关键作用。
在研发路径与关键决策维度上,李海涛认为,产品差异化和技术创新是小核酸Biotech企业在严苛生存环境中脱颖而出的关键。靶点选择需综合临床需求、竞争格局和审评需求,梯度开发扩展适应症以分散风险。平台适配方面,需权衡自主研发与授权引进的利弊,选择合适的平台(如ASO或siRNA)和技术路线。临床试验则需考虑不同临床方案的优劣、全球多中心的必要性和紧迫性等。此外,商业化准备也是关键一环。
对于小核酸药物的发展趋势,李海涛认为,在经历过第一轮“踩踏式”的肝靶点同质化开发后,越来越多的小核酸企业会转向新靶点新机制的研究,一方面实现真正的产品管线差异化、多元化,另一方面也能满足人们对小核酸药物解决不可成药靶点和真正面向未满足临床需求的期待和愿景。此外,多靶向新结构和组合疗法的应用将迅速兴起、强效保障并长效维持治疗效果。递送技术将突破人体主要组织器官的靶向递送,实现更加精准、高效和安全的药物递送。同时,生产成本降低和规模扩大将提高药物可及性,而AI/ML技术将从辅助工具转变为决策支持。
在介绍炫景生物时,李海涛提到,作为国家高新技术企业和国家级科技型中小企业,炫景生物致力于成为小核酸制药领域的深耕者和变革者。公司自2022年成立以来,已获得近3亿元融资,得到多家知名投资机构的支持。
炫景生物拥有自主研发的药物设计筛选平台RIHOST®、化学修饰平台RICMO®和体内递送平台LICOD®等核心技术平台,形成了独特的技术壁垒。药物设计筛选平台实现了智能化序列设计和高通量筛选,大大缩短了研发周期。
化学修饰平台通过新单体、新模式、新结构的三层次突破,建立了“通式”修饰模式,提高了药物的稳定性、有效性、长效性和安全性。递送技术平台则涵盖了肝内和肝外递送技术,肝靶向载体具有高效的组织靶向性和成本优势等。此外,炫景生物还建立了7个肝外组织的递送技术,其中肾脏靶向递送载体率先完成食蟹猴体内验证,研发进度全球领先。在管线开发方面,首发管线RG002已启动临床Ⅱ期研究,安全性有效性优于同靶点竞品。
谈及创业感悟时,李海涛表示,自己出身于科学家背景,在技术上的挑战并非最为棘手,真正困难在于如何实现从科学家到企业家的角色转变。
会议最后,来自国内小核酸药物领域的企业代表,包括炫景生物、瑞博生物、腾盛博药、思合基因、浩博医药、圣诺医药、海昶生物、传信生物、伽进生物、圆因生物、高田生物、星核迪赛以及维亚臻生物等公司,分享了各自公司的平台技术、研发管线布局、融资进展情况及BD计划等。他们认为,当前是中国小核酸药物行业发展的黄金时机,但同时也指出,递送技术、靶向范围拓展、稳定性提升及免疫原性降低等技术瓶颈仍亟待突破。
编辑 | 姚嘉
yao.jia@PharmaDJ.com
总第2565期
访问研发客网站,深度报道和每日新闻抢鲜看
www.PharmaDJ.com
siRNA核酸药物引进/卖出
2025-07-13
·抗体圈
摘要:siRNA治疗方法已获得广泛关注,目前已有六种siRNA获准用于临床应用。尽管它们被研究用于治疗代谢、心血管、传染性和罕见遗传疾病,以及癌症和中枢神经系统(CNS)疾病,但依然存在几个药物可用性挑战。在这里,我们提供有关这些挑战的深入讨论,包括靶向积累和细胞摄取(‘进入’)、内溶酶体逃逸(‘逃逸’)以及体内药效表现(‘疗效’)——这三个‘E’挑战,同时也阐明siRNA药物开发。此外,我们提出几种有前景的策略,这些策略在促进siRNA治疗药物临床转化方面具有巨大潜力,包括探索多样的配体-siRNA结合物、扩大潜在疾病靶点,以及开掘新的修饰几何形状,以及开发组合疗法。文章亮点:1.理论上,siRNA能够靶向任何感兴趣的基因,潜在地解决那些对小分子和蛋白质而言‘无法药物化’的疾病靶标。2.目前,已有六种siRNA治疗药物获得临床使用批准,以及大约20种其他候选药物已进入临床研究的后期阶段。3.靶向累积和细胞摄取(进入)、内溶酶体逃逸(逃避)以及体内药理学性能(疗效)(三个‘E’挑战)是siRNA药物开发中最关键的瓶颈。4.配体缀合的siRNA是有前景的平台,已经在强健的肝外递送方面取得了突破。复杂且适当的化学修饰可能会在siRNA方式的稳定性和长期疗效方面带来惊人的突破。【NO.1】siRNA治疗的蓬勃发展从制药历史的角度来看,小分子药物作为最早开发和应用的治疗方式,享用了超过一个世纪的使用,而蛋白质和抗体相对较晚出现,并且研究了将近半个世纪。尽管核酸分子作为一种新型治疗方法的发展时间较短(20-30年),但它们已经引起了制药行业的显著全球关注,成为第三种最显著的治疗方式。核酸药物仍在快速探索和开发中,特别是在RNAi领域,其广泛而深远的治疗潜力日益显现。考虑到这一点,我们相信即将到来的时期将是核酸的一个关键时代,既扩大了治疗选择的范围,也为该领域提供了新可能性。与传统的小分子药物和抗体相比,siRNA(见词汇表)具有丰富的疾病靶点、高开发成功率、短开发时间、强大且持久的疗效,以及平台化模式的卓越特征。目前,六种siRNA药物(patisiran、givosiran、lumasiran、inclisiran、vutrisiran和Rivfloza)已成功商业化。尽管siRNA药物在临床实践中的应用前景广泛,但其开发面临关键挑战,包括靶向积累和细胞摄取(进入)、内溶酶体逃逸(逃逸)和体内药效(疗效)(三大“E”挑战)。在本文中,我们阐述了siRNA治疗的当前状态和未来前景,概括了该领域所遇到的关键挑战,并提出了一系列应对策略。通过提供广泛的见解和灵感,本文旨在为科学和制药界提供有价值的指导。【NO.2】siRNA疗法的最新研究和开发状态近年来,siRNA疗法在多个候选药物的前临床和临床研究开发中显示出了巨大的潜力。截至2023年8月,全球范围内有15种在临床二期或后期阶段的研究siRNA药物(表1),涵盖广泛的治疗领域,包括罕见疾病和遗传性疾病,并扩展到常见疾病。主要制药公司已扩大其研究重点,以涵盖代谢性疾病、心血管疾病、乙型肝炎和癌症等常见病。例如,ALN-AGT(NCT04936035i,NCT05103332ii,随机)目前正在开发中,用于治疗高血压,并已进入二期临床试验。Olpasiran(NCT05581303iii,随机)旨在治疗动脉粥样硬化斑块,正在进行三期研究。SLN360(NCT05537571iv,随机)是一种降脂siRNA,已进入二期研究。RBD1016(NCT05961098v,随机)是一种用于治疗乙型肝炎的N-乙酰半乳糖胺(GalNAc)结合siRNA,将在欧洲开始二期试验。STP705和STP707由两种siRNA组成,靶向转化生长因子β1(TGF-β1)和环氧合酶2(COX-2),并以肽纳米粒(PNPs)形式制备。STP705局部施用到病变组织中,以治疗原位鳞状细胞癌(isSCC)(NCT04844983vi,二期,随机)和基底细胞癌(BCC)(NCT04669808vii,二期,非随机),而STP707(NCT05037149viii,一期,非随机)则通过静脉注射到身体中,用于治疗几种实体瘤和纤维化肝病,例如原发性硬化性胆管炎(PSC)。表1.选定的商业化或晚期研究的siRNA疗法从产品管道的角度来看,siRNA疗法的一个显著突破在于其扩展到肝外疾病,包括小分子药物和抗体药物一直未能涉足的领域,如中枢神经系统疾病。ALN-APP(NCT05231785ix,第一阶段,随机)是一种经椎管内给药的siRNA,靶向淀粉样前体蛋白(APPs),用于治疗阿尔茨海默病(AD)和脑淀粉样血管病(CAA)。最近,ALN-APP的第一阶段研究在单药剂量递增试验中获得了积极的中期结果。ARO-SOD1(NCT05949294xi,第一阶段,随机)是一种针对中枢神经系统内超氧化物歧化酶1(SOD1)的研究性siRNA,可能用于治疗由SOD1突变引起的肌萎缩侧索硬化症(ALS),目前正在进行第一阶段研究。此外,临床开发的RNAi疗法正在向将siRNA递送到其他组织(如眼睛、肌肉、肺部和脂肪)迈进。Tivanisiran(SYL1001)(NCT03108664xii,NCT04819269xiii,随机)目前正在进行第三阶段临床研究,以治疗干眼症。ARO-DUX4(第一/第二阶段)用于治疗面肩肱肌营养不良(FSHD)已提交临床试验。ARO-MUC5AC(NCT05292950xv,第一阶段,随机)、ARO-RAGE(NCT05276570xvi,第一阶段,随机)和ARO-MMP7(NCT05537025xvii,第一/二a阶段,随机)目前正在研究用于治疗肺部疾病。值得注意的是,siRNA的给药频率已经实现了历史性的突破。siRNA的增强稳定性修饰使其能够在体内持久抑制基因和治疗效果,同时避免潜在的序列依赖性非特异性效果。例如,Leqvio在头三个月只需给药两次,随后每六个月治疗一次,以有效管理原发性高胆固醇血症或混合性脂质异常。目前,全球有超过100家公司从事siRNA领域,其中大约30家公司专注于siRNA药物开发。根据Informa Pharma Intelligence的生物追踪记录,目前大约有200种基于siRNA/RNAi的药物正在进行临床前和临床研究。自2016年以来,共有14种siRNA和反义寡核苷酸(ASO)获得批准商业化。此外,寡核苷酸治疗领域在并购方面也见证了显著活动。近年来,在心血管和代谢疾病、神经系统疾病和乙型肝炎等领域有一些值得注意的许可协议。代表性的siRNA递送平台包括脂质纳米颗粒(LNP)、GalNAc-siRNA偶联物(GalAheadTM、PDoV-GalNAc等)、GEMINI、™TRiM™、PNP、RIBO-GalSTAR®和RIBO-OncoSTAR,而IKARIA™的建立是为了开发长效siRNA。【NO.3】siRNA临床研究的瓶颈尽管siRNA药物研究取得了重大进展,但仍存在一些需要克服的关键挑战。具体来说,三个“E”挑战(进入、逃逸、疗效)是限制siRNA临床翻译和应用的三个关键问题。图1.限制siRNA临床翻译和应用的三个“E”挑战3.1进入挑战:靶向积累和细胞摄取第一个挑战是在靶器官/组织中实现siRNA的高效富集并有效内化到靶细胞中(图1A)。由于它们的大尺寸和阴离子电荷,未修饰的裸siRNA显示出低生物利用度,半衰期短至几分钟。纳米载体封装的siRNA通常与血清蛋白结合,导致网状上皮系统(RES)摄取和吞噬清除。此外,siRNA可被血浆、组织和细胞质中存在的核酸酶或磷酸酶快速降解。全身清除后,siRNA必须穿过毛细血管的内皮才能进入组织,由于广泛的粘附和紧密连接,这尤其具有挑战性。尽管siRNA可能被动地积累在肝脏或肿瘤组织等多孔部位,但将这些治疗剂输送到优先吸收这些分子的器官以外的身体其他部位,以及血液-脑屏障(BBB)和血液-视网膜屏障等屏障的有效穿越,仍然面临巨大的挑战。3.2逃逸激发试验:内体和溶酶体逃逸第二个挑战是如何实现有效的内体和溶酶体逃逸。虽然siRNA可以通过内吞作用进入细胞,但只有不到1%的siRNA可以从内吞作用中逃逸,被动siRNA逃逸率低于0.01%。去唾液酸糖蛋白受体(ASGPR)是一个明显的例外,其肝细胞表达水平约为500000或更高,循环时间不到20分钟。足够的GalNAc-siRNA偶联物可以在肝细胞的细胞质中积累,以在治疗期间达到治疗水平。虽然这为未来基于RNAi的肝脏治疗靶向带来了希望,但siRNA逃逸对于其他类型的细胞来说仍然是一个未解决的问题。大多数表面受体的表达范围为10000–100000或更短,受体回收时间大约或超过90分钟(图1B)。由于细胞质和内体中siRNA的降解,观察到在任何给定时刻,只有极小的内吞GalNAc-siRNA偶联物存在于体内细胞质中。值得注意的是,虽然内体包埋的RNA治疗药物起到了作用,从而维持了较长的单剂量反应持续时间,但这一优势被很大一部分无法穿透细胞质的内吞RNA治疗药物所抵消。因此,虽然内体的释放确实是抑制RNA疗法在人类疾病治疗中更广泛应用的主要障碍,但值得注意的是,需要有一种平衡,以在一定程度上维持贮存效应,确保长时间的持续反应。迄今为止,试图使用改良的pH敏感性、离子穿透剂、氯喹样溶酶体试剂、成孔肽如蜂毒肽、十二烷基磷酸胆碱(DPC)和/或GalNAc偶联的蜂毒肽样肽(NAG-MLP)来增强内体逃逸,但尚未完全解决细胞毒性与内体逃逸增加之间的关系。3.3疗效挑战:体内药物性能第三个挑战是要求良好的体内稳定性、持久效果和安全性。使用病毒载体进行体内核酸递送有一些毒副作用和目前主要限于临床前研究。化学合成的载体系统,如阳离子脂质和大多数无机纳米颗粒,可在体内诱导细胞凋亡和炎症。给药系统还必须确保生产、质量控制和运输的便利性,以实现大规模临床应用。此外,目前RNA药物临床前研究中广泛使用的小鼠模型并不是毒性评价模型,因为从小鼠模型获得的RNA剂量反应关系不能直接应用于人类。非灵长类动物模型通常缺乏与人类的基因组序列的足够重叠来预测药效学效应,因此有必要扩大非人灵长类动物(NHP)模型的使用,或者作为潜在的选择,扩大与疾病相关的类器官的使用。未经修饰的寡核苷酸通常在体内不稳定,并且很容易被血液中的核酸酶降解。此外,外源寡核苷酸可能在体内显示免疫原性并引起免疫反应。随着技术的突破,化学修饰【例如,对硫代磷酸盐(PS)骨架、核糖和链末端的修饰】已被广泛用于增强siRNA的稳定性,减少/消除脱靶效应和免疫原性,从而提高siRNA的“功效”(图1C)。通过复杂的修饰,siRNA已成功实现99%的基因沉默并在体内持续存在,允许低剂量季度、半年甚至每年给药。化学修饰的进化史及其对siRNA功效的影响是一个令人着迷的研究领域,值得进一步全面探索。然而,尽管取得了这些可喜的成就,但仍存在一些挑战。例如,修饰诱导的稳定性和特异性增强可能会降低沉默活性或引起意想不到的不良反应(图1D)。此外,在临床前和临床研究中,都需要仔细评估siRNA的免疫原性和毒性(包括脱靶诱导毒性)。更重要的是,一系列专利家族对siRNA药物开发的知识产权格局做出了重大贡献。例如,WO2016028649概述了一种几何结构,该几何结构将siRNA的两条链的修饰划分为由核苷酸计数的特定范围定义的不同区域,从而提供每个区域的修饰单体的化学结构或物理化学性质。WO2013074974描述了一种dsRNA双链体,其基序由一条或两条链中三个连续核苷酸上的三个相同修饰组成,特别是在切割位点附近。此外,WO2018185241重点介绍了反义链5'端2位和14位核苷酸的修饰策略,以及正义链上的核苷酸,对应于反义链的11、13、11和13或11-13位。这些专利对siRNA药物开发构成了重大障碍,必然需要该领域的其他实体建立独特的技术。【NO.4】克服三个“E”挑战的有前途的策略为了应对这些挑战并推动siRNA疗法的发展,几种有前途的策略或方法值得探索。图2.克服三个“E”挑战的有前途的方法4.1开发新型化学修饰优化化学修饰是提高siRNA稳定性、特异性、安全性和生物利用度的重要方向。这包括开发新的化学修饰单体、修饰模式和RNAi触发结构(图2A-C)。传统的siRNA修饰主要涉及2′-O-甲基化(2′-OMe)、2′-氟脱氧核糖核苷酸(2′-F)和PS,而新型修饰单体和修饰模式的开发将进一步完善siRNA的药代动力学和安全性。例如,已经开发了新型单体,如乙二醇核酸(GNA)和5′-(E)-乙烯基膦酸盐[5′-(E)-VP](图2B),新型修饰模式,如增强稳定化学(ESC)plus(ESC+)(图2A),以及新型RNAi触发结构,如小环状干扰RNA(sciRNA)、不对称siRNA和二价siRNA支架(图2C)。此外,现在可以使用算法实现siRNA的设计和修饰。例如,Alnylam已经开发了几代siRNA设计,包括部分修饰的标准模板化学(STC)、ESC、高级ESC、ESC+和IKARIA™。几种ESC+偶联物目前正处于临床流程中。在专利方面,新型单体、图案和结构的发展可以为新来者提供绕过现有知识产权的空间。此外,业务合作期间的开放许可协议可以为其他公司提供使用siRNA技术的机会,促进其普及和商业化。4.2建立独特的递送系统虽然LNP、聚合物、无机纳米颗粒和外泌体等各种纳米材料已被开发为siRNA载体,但它们的负载能力、稳定性、安全性和有效性仍然存在局限性。未来的基础研究应侧重于优化这些载体的物理化学性质,并使用独特的靶向配体或化学部分特异性结合患病细胞的表面标志物/受体。siRNA可以与配体共价连接以形成配体-siRNA偶联物,这可以降低循环中的清除率并增强靶向积累和细胞摄取,从而调节其药代动力学和药效学特征。这些配体包括小分子、脂质[如胆固醇、2′-O-十六烷基(C16)、各种脂肪酸]、肽(如RGD衍生物、H2009.1、A20FMDV2、胱氨酸结肽)、适配体、抗体、蛋白质(如centyrin)、糖类(如GalNAc)和非编码RNA(ncRNA)(图2D)。与纳米颗粒相比,配体偶联物通常体积小,易于大规模合成,并具有明显的药代动力学特性。与脂肪酸等脂质部分结合可以改变肝外组织中的积累,从而能够在包括CNS、心脏、肺和肌肉在内的多种组织中进行基因调控。抗体和细胞表面受体之间的特异性相互作用可能能够递送到其他技术无法到达的特定组织和/或细胞亚群。单剂量的TfR1抗体(αTfR1)与siRNA偶联,在小鼠和猴子中产生超过75%的mRNA减少,骨骼肌和心脏(横纹)肌的沉默最严重,而其他主要器官的沉默活动最少或没有。siRNA治疗药物还可以与阳离子肽部分(如细胞穿透肽和Endo-Porter)连接,有效穿透组织屏障和细胞膜。此外,siRNA和内体逃逸增强佐剂的组合可能是将配体偶联的siRNA递送至非肝组织的可行策略。4.3扩大疾病目标siRNA技术主要用于目标蛋白质编码基因。然而,最近的研究表明,ncRNA,如长ncRNA(lncRNA),在各种疾病中起着重要作用(图2E)。因此,开发能够有效调节ncRNA表达的新型RNA靶向技术可能为疾病治疗提供更广泛的机会。此外,探索编码和ncRNA之间的相互作用,例如竞争性内源性RNA(ceRNA)网络,可能会为疾病机制提供新的见解,并实现更有效的治疗干预。除了在mRNA水平调节基因表达外,siRNA技术还可以靶向表观遗传修饰,例如DNA甲基化或组蛋白修饰,这些修饰在疾病的发展和发展中起着至关重要的作用。通过调节表观遗传标记,有可能重编程基因表达模式并逆转疾病表型。4.4探索联合疗法利用双靶向方法或将siRNA与其他治疗药物(如化疗药物、抗体或免疫调节剂)联合使用,有望增强疗效、克服耐药性和减少脱靶效应。这些策略可能为治疗以前无法治愈的疾病创造新的机会。例如,正在实施一种涉及VIR-2218(GalNAc-siRNA偶联物,也称为ALNHBV02)和聚乙二醇-干扰素α(PEG-IFN-α)的联合治疗,旨在实现乙型肝炎的功能性治愈。siRNAJNJ-73763989(JNJ-3989)加核苷(t)类似物(NA)用于评估有/没有衣壳组装调节剂JNJ-56136379(JNJ-6379)的慢性乙型肝炎患者的治疗效果。此外,pozelimab(补体C5靶向抗体)和cemdisiran(一种GalNAc-siRNA偶联物)正在联合用于治疗重症肌无力和阵发性睡眠性血红蛋白尿症(PNH)。此外,正在进行Empaveli(一种环肽)和siRNA组合的临床前研究,这可能会降低Empaveli的治疗频率和/或提高治疗效果。【NO.5】总结和未来展望我们正在见证RNA药物治疗新时代的到来。RNA疗法基于一个强大且多功能的平台,该平台在解决未满足的临床需求方面具有几乎无限的潜力。因此,RNA疗法注定会改变许多疾病的护理标准。随着第六种siRNA药物Rivfloza的获批,未来几年肯定会有更多的siRNA疗法出现。在成功建立用于肝细胞递送的最先进的GalNAc-siRNA偶联物后,肝外递送技术的探索将成为该领域的下一个前沿领域(参见临床医生专区)。与肝脏相比,将RNAi分子递送到靶向非肝脏疾病的挑战要大得多。配体-siRNA偶联物必须以足够的速率在靶细胞中积累以实现沉默。此外,避免同时进行肾脏和网状内皮清除、增强外渗和组织渗透、增加货物内化受体低表达细胞类型的摄取、改善内体逃逸以及支持强效和安全治疗效果等几个因素需要进行珠子处理以实现令人满意的沉默。为了将siRNA的适用性扩大到肝脏组织之外,至关重要的是:(i)识别或确定可以促进有效内化的独特受体;(ii)提出具体的筛选或勘探策略;(iii)设计并鉴定用于稳健递送和持续基因沉默的新型配体;(iv)选择与特定疾病有关的遗传或临床可行的靶基因。如果在临床条件下肝外递送变得可行且稳健,则狩猎RNAi疗法的领域可能会显着扩大。此外,在siRNA的开发中,与化学制造和控制(CMC)以及药物注册政策相关的问题会显著影响新药营销。siRNA的CMC面临多重挑战,包括单体供应、质量控制、能力建设、杂质表征和分离纯化。在药品注册政策方面,目前还缺乏统一的国际标准。建议通过加强科学研究、提高透明度以及修订法规和政策来确保临床试验的安全性和有效性。此外,目前siRNA的主要扩展方向是在慢性疾病领域,如高胆固醇血症、高甘油三酯血症、高血压、高脂蛋白胆固醇(a)[Lp(a)]心血管疾病、非酒精性脂肪性肝炎(NASH)和乙型肝炎。未来siRNA药物开发的突破性方向包括递送至CNS、眼睛、肌肉、肺和脂肪组织和肿瘤。这为siRNA治疗留下了相当大的市场空间。尽管存在挑战(参见悬而未决的问题),但siRNA代表了一种有前途的方式,有可能彻底改变各种疾病的治疗。为了应对与高效和安全递送、内体逃逸、体内功效相关的挑战,其他方面则需要跨多个领域的持续创新和合作。可以肯定的是,经过不懈的努力,这些挑战将继续被规避,并最终迎来进一步的重大突破。识别微信二维码,添加抗体圈小编,符合条件者即可加入抗体圈微信群!请注明:姓名+研究方向!本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
siRNA临床研究
2025-06-05
关注并星标CPHI制药在线RNA疗法正迅速成为现代医学中最具变革性的治疗策略之一。从反义寡核苷酸(ASO)和小干扰RNA(siRNA)等精准调控基因表达的工具,到mRNA疫苗和肿瘤免疫疗法等前沿应用,RNA技术已在多个疾病领域展现出巨大潜力。近年来,随着递送系统、生物偶联技术和修饰化学的不断进步,RNA疗法的临床管线迅速扩展,涵盖了罕见病、神经系统疾病、代谢性疾病以及肿瘤等多个领域。目前,RNA疗法的临床开发全景涵盖了ASO、siRNA、mRNA、核酸适体(aptamer)等主要技术路径,在不同适应症中布局广泛,关键企业的研发动态频繁,已获批上市的代表性药物不断涌现。本文总结了现有管线和上市的 RNA疗法,将这一新兴领域的开发全景呈现出来。1. ASO类 RNA资产梳理 1.1 I期ASO资产 • Praxis ASO资产 :Elsunersen(PRAX-222) 靶点:SCN2A基因 适应症:由SCN2A基因的功能获得性突变引起的早发性SCN2A发育性和癫痫性脑病。 • PYC Therapeutics ASO资产:VP-001 靶点:PRPF31基因 适应症:由PRPF31基因突变引起的视网膜色素变性11型 ASO资产:PYC-001 靶点:OPA1基因 适应症:由OPA1基因突变引起的常染色体显性视神经萎缩(ADOA) ASO资产:PYC-003 靶点:PKD1基因 适应症:常染色体显性多囊肾病(ADPKD) • Bio-Path Holdings ASO资产:BP1002(Liposomal Grb2 ASO) 适应症:急性髓性白血病(AML)、B细胞淋巴瘤(B-cell lymphoma) 技术特点:使用独特的中性脂质体递送系统(DNAbilize® Platform)递送ASO。1.2 II期ASO资产 • Stoke Therapeutics ASO资产:Zorevunersen(STK-001) 靶点 :SCN1A基因 适应症:Dravet综合征(一种严重癫痫) ASO资产 :STK-002 靶点:OPA1基因 适应症:常染色体显性视神经萎缩(ADOA) • Entrada Therapeutics ASO资产:ENTR-601-44 适应症:Duchenne肌营养不良(DMD) 靶点 :DMD中的Exon 44跳跃 技术特点:使用Entrada独有的分子穿透技术(Endosomal Escape Vehicle, EEV)提高细胞内递送效率。 ASO资产:ENTR-601-45 靶点:DMD基因的外显子45(Exon 45) 适应症:适用于外显子45跳跃的杜氏肌营养不良症(DMD)患者 • Dyne Therapeutics ASO资产:DYNE-251 适应症:Duchenne肌营养不良(DMD),针对DMD中的Exon 51跳跃。 技术特点:使用抗体-寡核苷酸结合平台(FORCE platform)进行肌肉组织特异性递送。 ASO资产 :DYNE-101 适应症:肌强直性营养不良症1型(DM1) 靶点:DMPK基因的异常CTG重复序列 • Ribomic ASO资产:Umedaptanib Pegol(原RBM-007,严格来说是核酸适体aptamer,而不是典型ASO) 靶点 :FGF2(成纤维细胞生长因子2)。 适应症:湿性年龄相关性黄斑变性(wAMD),软骨发育不全症 • Wave Life Sciences ASO资产: WVE-N531:DMD(杜氏肌营养不良症)治疗,靶向Exon 53跳跃 WVE-003:亨廷顿舞蹈症(Huntington's Disease, HD),靶向HTT基因突变 • PepGen ASO资产:PGN-EDO51 适应症:Duchenne肌营养不良(DMD) 技术特点:结合增强型细胞穿透肽(Enhanced Delivery Oligonucleotide, EDO)技术,提高ASO进入肌肉细胞的效率。 ASO资产 :PGN-EDODM1 靶点:DMPK基因的异常CUG重复序列 适应症:肌强直性营养不良症1型(DM1) • 罗氏 ASO资产 :Tominersen(RG6042) 靶点:Huntingtin(HTT)基因 适应症:亨廷顿病(Huntington's Disease, HD) ASO资产 :IONIS-FB-LRx(RO7434656 / RG6299) 靶点:补体因子B(Factor B) 适应症:IgA肾病(IgAN) • Ultragenyx ASO资产 :GTX-102 靶点:UBE3A-AS(UBE3A反义转录本) 适应症:天使综合征(Angelman Syndrome)1.3 ASO类3期资产 • Oncotelic Therapeutics ASO资产:OT-101(也叫Trabedersen) 靶点:转化生长因子β2(TGF-β2) 适应症:胶质母细胞瘤(GBM)、胰腺癌、恶性黑色素瘤 机制:抑制TGF-β2,有望减轻肿瘤免疫抑制,增强抗肿瘤免疫反应 • 阿斯利康 ASO资产:ION449(亦称AZD8233),与Ionis合作开发的ASO疗法 靶点:PCSK9(一种影响低密度脂蛋白胆固醇LDL-C水平的蛋白质) 适应症:高胆固醇血症(hypercholesterolemia) 备注:主要竞争对手包括小分子抑制剂和PCSK9单抗(如Repatha、Praluent) • GSK ASO资产:bepirovirsen 靶点:乙型肝炎病毒(HBV)的前基因组RNA和mRNA 适应症:慢性乙型肝炎(chronic hepatitis B, CHB),通过抑制HBV基因表达,帮助病毒清除或实现功能性治愈(functional cure)。 • 诺华 ASO资产:Pelacarsen 靶点:LPA基因(编码脂蛋白(a)) 作用机制:Pelacarsen通过抑制LPA基因的mRNA,降低血液中脂蛋白(a)(Lp(a))水平,从而降低心血管疾病风险。Lp(a)是目前被认为的重要但尚无针对性治疗手段的心血管风险因子。 适应症:主要用于治疗动脉粥样硬化性心血管疾病高危患者中,血脂异常(特别是Lp(a)升高)的情况。 临床阶段:正在进行III期临床试验(Lp(a)HORIZON)。Pelacarsen可能成为首个专门针对Lp(a)升高治疗获批的药物。1.4 ASO类上市药物 • 渤健 Spinraza(nusinersen) 靶点:SMN2前体mRNA(促进功能性SMN蛋白表达) 适应症:脊髓性肌萎缩症(SMA) 获批时间:2016年12月(美国FDA批准) 备注:全球首个获批的SMA治疗药物。由Ionis开发,Biogen负责商业化。 • Sarepta Therapeutics Exondys 51(eteplirsen) 靶点:DMD基因的Exon 51 适应症:Duchenne肌营养不良(DMD) 获批时间:2016年9月(FDA加速批准) Vyondys 53(golodirsen) 靶点:DMD基因的Exon 53 适应症:DMD 获批时间:2019年12月 Amondys 45(casimersen) 靶点:DMD基因的Exon 45 适应症:DMD 获批时间:2021年2月(FDA加速批准) • Ionis Pharmaceuticals Tegsedi(inotersen) 靶点:TTR(转甲状腺素蛋白) 适应症:遗传性转甲状腺素蛋白淀粉样变性多发性神经病(hATTR-PN) 获批时间 :2018年10月(FDA,EMA批准) Waylivra(volanesorsen) 靶点:APOC3(载脂蛋白C-III) 适应症:家族性乳糜微粒血症综合征(FCS) 获批时间:2019年5月(欧洲EMA批准;未获美国FDA批准) • NS Pharma Viltepso(viltolarsen) 靶点:DMD基因的Exon 53 适应症:Duchenne肌营养不良(DMD) 获批时间:2020年8月(FDA加速批准)2.RNAi类 RNA资产2.1 I期RNAi资产 • Aligos Therapeutics RNAi资产:ALG-125755 靶点:乙型肝炎病毒(HBV)RNA 适应症:慢性乙型肝炎(CHB) • Regulus Therapeutics RNAi资产:RGLS8429 靶点:microRNA-17(miR-17家族) 适应症:常染色体显性多囊肾病(ADPKD) • Phio Pharmaceuticals RNAi资产:PH-762 靶点:程序性死亡受体1(PD-1) 适应症:癌症免疫疗法(通过下调T细胞表面PD-1,增强免疫杀伤) 技术特点:采用其自有的INTASYL✓平台,优化了siRNA的稳定性和局部递送。 • TransCode Therapeutics RNAi资产:VIR-2218 TTX-MC138 靶点:microRNA-10b(miR-10b) 适应症:针对转移性实体肿瘤(如乳腺癌、胰腺癌、脑肿瘤等) 技术特点:使用纳米颗粒系统高效递送siRNA药物,特别适合针对深部转移灶。2.2 II期RNAi资产 • Arbutus Biopharma RNAi资产:AB-729 靶点:乙型肝炎病毒(HBV)表面抗原(HBsAg) 适应症:慢性乙型肝炎(CHB) 备注:AB-729是Arbutus当前最重要的核心资产之一。 • OliX Pharmaceuticals RNAi资产:OLX703A 靶点:HBV病毒相关RNA 适应症:慢性乙型肝炎(CHB) 机制:抑制HBV病毒蛋白表达 • Silence Therapeutics RNAi资产:SLN360 靶点:LPA基因(编码脂蛋白Lp(a)) 适应症:高脂蛋白(a)血症(Lp(a)过高相关的心血管疾病) 机制:通过降低血液中Lp(a)水平,减少动脉粥样硬化风险。 备注:SLN360是Silence在心血管RNA疗法领域的主力项目。 • Sirnaomics RNAi资产:STP705 靶点:双靶点siRNA药物,靶向TGF-β1和COX-2。 适应症:瘢痕治疗(皮肤纤维化)、非黑色素瘤皮肤癌(如基底细胞癌、鳞状细胞癌) 机制:抑制纤维化、降低肿瘤微环境免疫抑制。 备注:Sirnaomics的特点是双靶点siRNA联合递送。 • GSK RNAi资产:GSK4532990 靶点:靶向HSD17B13基因 适应症:代谢功能障碍相关脂肪性肝炎(MASH) • 礼来 RNAi项目:LY3561774 靶点:SERPINA1基因 适应症:α1-抗胰蛋白酶缺乏症(AATD) 机制 :降低异常α1-抗胰蛋白酶(AAT)积聚 • VIR Biotechnology RNAi项目:VIR-2218 靶点 : HBV RNA 适应症:慢性乙型肝炎(CHB)。 机制:抑制HBV表面抗原表达 • 罗氏 RNAi资产:Zilebesiran 靶点 :肝脏表达的血管紧张素原(AGT)基因。 适应症:高血压,特别是高心血管风险患者。2.3 III期RNAi资产 • Arrowhead Pharmaceuticals RNAi资产:ARO-APOC3 靶点 :APOC3(载脂蛋白C-III), 适应症:高甘油三酯血症和罕见脂代谢异常 • 武田 RNAi资产:Fazirsiran 靶点:SERPINA1(编码α1-抗胰蛋白酶) 适应症:α1-抗胰蛋白酶缺乏症(AATD)引起的肝病 • 安进 RNAi资产:Olpasiran 靶点:LPA基因(脂蛋白(a)) 适应症:高脂蛋白(a)血症及其引发的心血管疾病风险 备注:这是一款非常重磅的RNAi项目,对心血管领域意义重大。 • Avidity Biosciences RNAi资产:AOC 1001 靶点:DMPK基因(导致肌强直性营养不良症1型DM1) 适应症:肌强直性营养不良症1型(DM1) 技术特点:AOC(Antibody Oligonucleotide Conjugate,抗体-寡核苷酸偶联体),用于肌肉靶向递送siRNA。 • 赛诺菲 RNAi资产:Fitusiran 靶点:AT(抗凝血酶) 适应症:血友病A或B患者的出血预防 • VIR Biotechnology RNAi资产:VIR-2218 靶点:HBV RNA 适应症:慢性乙型肝炎(CHB)2.4 上市RNAi资产 • Alnylam Pharmaceuticals Alnylam是全球RNAi疗法先锋,拥有最多已上市RNAi药物。 Onpattro(Patisiran) 靶点:TTR 适应症:遗传性转甲状腺素蛋白淀粉样变性引起的多发性神经病(hATTR-PN) 批准情况:2018年FDA/EMA批准 Givlaari(Givosiran) 靶点:ALAS1 适应症:急性肝卟啉症(AHP) 批准情况:2019年FDA/EMA批准 Oxlumo(Lumasiran) 靶点:HAO1 适应症:原发性高草酸尿症1型(PH1) 批准情况:2020年FDA/EMA批准 Amvuttra(Vutrisiran) 靶点:TTR 适应症:遗传性转甲状腺素蛋白淀粉样变性引起的多发性神经病(hATTR-PN)(长效皮下注射版) 批准情况:2022年FDA批准 • 诺华 RNAi资产:Leqvio(Inclisiran) 靶点:PCSK9 适应症:高胆固醇血症,动脉粥样硬化性心血管疾病风险降低 批准情况:2020年欧洲EMA批准;2021年底美国FDA批准 • 诺和诺德 RNAi资产:Rivfloza (nedosiran) 靶点:肝脏中乳酸脱氢酶(LDH)mRNA 适应症:治疗9岁及以上、肾功能相对良好的原发性高草酸尿症1型(PH1)患者。 作用机制:抑制LDH蛋白表达,减少草酸过度生成,缓解PH1疾病过程,减少肾脏损害风险。 批准情况:2023年9月29日FDA正式批准Rivfloza上市。成为继Alnylam的Oxlumo(Lumasiran)之后,全球第二款获批用于PH1治疗的RNAi药物。3.mRNA类 RNA药物资产3.1 1期mRNA资产 • 赛诺菲 SP0237: 季节性流感 mRNA 疫苗 适应症:针对 A/H3N2 毒株的季节性流感。 SP0256 – RSV mRNA 疫苗(老年人群) 适应症:用于预防老年人群中的呼吸道合胞病毒(RSV)感染。 SP0268 – mRNA 痤疮疫苗 适应症:针对痤疮(Acne)的 mRNA 疫苗。 SP0291 – 多价呼吸道病毒 mRNA 疫苗 适应症:针对 RSV、人类偏肺病毒(hMPV)和副流感病毒 3 型(PIV3)的组合疫苗,主要用于老年人群。 沙眼衣原体(Chlamydia)mRNA 疫苗候选 适应症:预防沙眼衣原体感染,主要针对 18 至 29 岁的成人。 • Vertex mRNA资产:VX-522:用于囊性纤维化(CF)的mRNA疗法 靶点:CFTR基因(囊性纤维化跨膜电导调节因子)。 适应症:无法通过CFTR调节剂治疗的CF(囊性纤维化)患者,尤其是那些由于CFTR基因突变导致CFTR蛋白缺失的患者。 作用机制:VX-522是一种mRNA疗法,通过脂质纳米颗粒(LNP)递送CFTR mRNA至肺部细胞,促使其合成功能性CFTR蛋白,从而恢复氯离子通道的功能。3.2 II期mRNA资产 • Gritstone Bio GRANITE(GRT-C901/GRT-R902) 个体化肿瘤新抗原疫苗,采用腺病毒(ChAd68)和自扩增mRNA(samRNA)组成的异源prime-boost策略。 适应症:用于治疗转移性微卫星稳定型结直肠癌(MSS-CRC)。 CORAL 基于自扩增mRNA(samRNA)的COVID-19疫苗,诱导广泛且持久的中和抗体和T细胞免疫反应。 • CureVac/GSK 季节性流感mRNA疫苗候选 该疫苗候选基于CureVac的第二代mRNA平台,针对流感病毒株,包括A型和B型毒株。 COVID-19 mRNA疫苗候选CV0601和CV0701 CV0601为单价疫苗,编码Omicron BA.4/5变异株的刺突蛋白;CV0701为二价疫苗,编码Omicron BA.4/5变异株和原始SARS-CoV-2毒株的刺突蛋白。3.3 III期mRNA资产 • 第一三共 DS-5670a(原始毒株单价疫苗) 适应症:Covid-19疫苗,作为加强针用于已完成初始疫苗接种的成人和老年人。 DS-5670a/b(原始毒株与Omicron BA.4/5二价疫苗) 适应症:Covid-19疫苗,作为加强针用于12岁及以上已完成初始疫苗接种的人群。 DS-5670d(Omicron XBB.1.5单价疫苗) 适应症:Covid-19疫苗,作为季节性加强针用于12岁及以上人群,包括未接种疫苗者。 • 默沙东 mRNA资产:V940(mRNA-4157) 类型:肿瘤疫苗(个体化mRNA疫苗) 适应症:手术切除后的高风险黑色素瘤患者辅助治疗 靶点:个体化新抗原(根据患者肿瘤突变特异设计)3.4上市mRNA资产 • Arcturus Therapeutics mRNA资产:KOSTAIVE(ARCT-154 / Zapomeran) 类型:自扩增mRNA(sa-mRNA)疫苗 适应症:用于预防COVID-19,适用于18岁及以上人群 靶点:SARS-CoV-2病毒刺突蛋白(Spike protein) • BioNTech/辉瑞 Comirnaty 类型:mRNA疫苗 适应症:用于预防COVID-19,适用于6个月及以上人群 靶点:SARS-CoV-2病毒刺突蛋白(Spike protein) 获批时间:✓2020年12月获得FDA紧急使用授权,2021年8月获得美国FDA完全批准 • 莫德纳 Spikevax 类型:mRNA疫苗 适应症:用于预防COVID-19,适用于6个月及以上人群 靶点:SARS-CoV-2病毒刺突蛋白(Spike protein) 获批时间:2020年12月18日,美国FDA授予紧急使用授权;2022年1月31日,获得FDA完全批准Ref. TD Cowen. Pharmaceuticals’ websitesEND【企业推荐】来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPHI制药在线▼点击阅读原文,进入智药研习社~
临床2期寡核苷酸上市批准信使RNA临床1期
100 项与 Zerlasiran 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 心血管疾病 | 临床3期 | 英国 | - | |
| 动脉粥样硬化 | 临床2期 | 澳大利亚 | 2022-12-13 | |
| 动脉粥样硬化 | 临床2期 | 捷克 | 2022-12-13 | |
| 动脉粥样硬化 | 临床2期 | 丹麦 | 2022-12-13 | |
| 动脉粥样硬化 | 临床2期 | 荷兰 | 2022-12-13 | |
| 动脉粥样硬化 | 临床2期 | 斯洛伐克 | 2022-12-13 | |
| 动脉粥样硬化 | 临床2期 | 南非 | 2022-12-13 | |
| 动脉粥样硬化 | 临床2期 | 英国 | 2022-12-13 | |
| 高脂蛋白血症 | 临床1期 | 美国 | 2020-11-18 | |
| 高脂蛋白血症 | 临床1期 | 美国 | 2020-11-18 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2期 | 180 | (SLN360 300 mg Q16W) | 顧構壓網醖齋糧構顧淵(壓艱鹽憲製鹹範顧醖窪) = 壓夢製鏇顧窪鹹淵憲醖 齋簾製壓鹽繭蓋獵鏇餘 (鬱鹽憲艱鑰衊鹽遞糧衊, 1.99) 更多 | - | 2025-07-01 | ||
(SLN360 300 mg Q24W) | 顧構壓網醖齋糧構顧淵(壓艱鹽憲製鹹範顧醖窪) = 醖艱夢壓夢淵蓋獵淵淵 齋簾製壓鹽繭蓋獵鏇餘 (鬱鹽憲艱鑰衊鹽遞糧衊, 1.94) 更多 | ||||||
临床2期 | 动脉粥样硬化 lipoprotein(a) concentration | 178 | Zerlasiran 450 mg every 24 weeks for 2 doses | 襯鑰窪餘製齋選網製夢(窪廠遞醖鬱觸憲築蓋簾) = 觸鏇糧遞構襯構壓繭觸 築積製簾築獵憲憲壓衊 (襯願鬱繭襯醖構獵範鑰, −90.9 ~ −80.3) 更多 | 积极 | 2024-11-18 | |
Zerlasiran 300 mg every 16 weeks for 3 doses | 襯鑰窪餘製齋選網製夢(窪廠遞醖鬱觸憲築蓋簾) = 醖選築窪蓋窪積憲築蓋 築積製簾築獵憲憲壓衊 (襯願鬱繭襯醖構獵範鑰, −88.2 ~ −77.4) 更多 | ||||||
临床2期 | 178 | 網築膚積鹹襯窪蓋糧窪(鏇積鑰膚鏇淵餘糧構繭) = 簾憲鏇鹽壓製艱膚獵窪 衊網夢築膚構憲糧願製 (選鹽鬱積鑰艱淵構顧範 ) 达到 | 积极 | 2024-06-20 | |||
Placebo | - | ||||||
临床1期 | - | Zerlasiran 300 mg (a single subcutaneous dose) | 顧醖夢膚壓憲積膚壓遞(範餘窪夢範夢網鏇選鏇) = There were no serious adverse events. 衊願鏇鬱網簾選淵糧獵 (鑰鹹築製壓製窪餘願鏇 ) | 积极 | 2024-04-08 | ||
Zerlasiran 600 mg (a single subcutaneous dose) | |||||||
临床2期 | 178 | 鏇製鑰糧憲壓簾鹽蓋顧(壓廠鏇範衊鹽襯製餘壓) = 顧壓選淵願築蓋夢遞顧 築構選鹽糧鬱範顧鏇醖 (壓鹹淵獵糧鹽夢鹽鏇獵 ) | 积极 | 2024-03-13 | |||
Placebo | - | ||||||
临床1期 | 36 | 餘範膚範淵襯醖鑰醖鹽(遞網鹽壓簾積艱觸構積) = 淵製夢憲襯壓網鹽齋顧 糧築鏇網憲繭齋網艱憲 (願選醖繭糧選鑰蓋獵醖 ) 更多 | 积极 | 2023-11-01 | |||
Placebo | - | ||||||
临床1期 | Lp(a) | 32 | Placebo | 遞淵糧襯壓繭築淵遞壓(醖鹽鬱齋衊鏇獵餘遞獵) = One participant experienced 2 serious adverse event episodes: admission to the hospital for headache following SARS-CoV-2 vaccination and later for complications of cholecystitis, both of which were judged to be unrelated to study drug. 窪範襯醖網積餘衊餘艱 (襯觸艱壓衊襯鏇醖淵鹽 ) | 积极 | 2022-05-03 | |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

