更新于:2024-09-27
Liraglutide biosimilar(Wanbang Biopharmaceuticals)
利拉鲁肽生物类似药(万邦生化)
更新于:2024-09-27
概要
基本信息
原研机构 |
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评- |
序列信息
Sequence Code 50953

当前序列信息引自: *****
关联
4
项与 利拉鲁肽生物类似药(万邦生化) 相关的临床试验评估利拉鲁肽注射液干预成人肥胖或超重伴相关代谢异常患者的疗效和安全性III期临床研究
主要目的:评估利拉鲁肽注射液与安慰剂相比,在成人肥胖或超重伴相关代谢异常(高血压、血脂异常或2型糖尿病)患者中的减重作用。
次要目的:观察利拉鲁肽注射液与安慰剂相比,对腰围、血压、血脂、血糖等代谢指标以及生活质量的影响;
评估利拉鲁肽注射液的安全性和耐受性。
开始日期2020-08-07 |
申办/合作机构 |
在二甲双胍治疗血糖控制不佳的2型糖尿病患者中评价利拉鲁肽注射液与诺和力皮下注射治疗的疗效和安全性
主要目的:比较利拉鲁肽注射液与诺和力® 治疗2型糖尿病疗效的相似性 次要目的:比较利拉鲁肽注射液和诺和力®治疗2型糖尿病的安全性、耐受性和免疫原性。比较利拉鲁肽注射液和诺和力®在2型糖尿病患者中多次给药的PK相似性。
开始日期2020-08-03 |
申办/合作机构 |
在中国健康男性受试者中比较利拉鲁肽注射液和诺和力的随机、开放、单剂量、皮下注射、双交叉I期临床研究
主要目的:评估健康受试者皮下注射国产利拉鲁肽注射液(以下简称利拉鲁肽注射液)与原研利拉鲁肽注射液(商品名: 诺和力®, 以下简称诺和力®)的药代动力学(PK)的相似性。 次要目的:评估健康受试者皮下注射利拉鲁肽注射液或诺和力®的安全性; 探索性目的:评估健康受试者皮下注射利拉鲁肽注射液或诺和力®的免疫原性。
开始日期2019-11-11 |
申办/合作机构 |
100 项与 利拉鲁肽生物类似药(万邦生化) 相关的临床结果
登录后查看更多信息
100 项与 利拉鲁肽生物类似药(万邦生化) 相关的转化医学
登录后查看更多信息
100 项与 利拉鲁肽生物类似药(万邦生化) 相关的专利(医药)
登录后查看更多信息
9
项与 利拉鲁肽生物类似药(万邦生化) 相关的新闻(医药)2024-01-11
1 月 10 日,华东医药收到 NMPA 通知,瑞美吡嗪注射液(英文名称:Relmapirazin Injection;研发代码:MB-102)的上市许可申请获得受理,为一类新药。全球首创+一类新药,药械组合解决未被满足临床需求公告显示,一类新药瑞美吡嗪注射液(MB-102)是一种用于测量 GFR 的荧光示踪剂,可与全球首创的 MediBeacon®肾小球滤过率动态监测系统(简称「动态监测系统」)配合使用,以测量肾功能受损或正常患者的肾小球滤过率。瑞美吡嗪注射液及动态监测系统最初由美国 MediBeacon, Inc.(简称「MediBeacon 公司」)开发,华东医药于 2019 年获得 MediBeacon 公司全部产品(含后续开发新产品)在中国大陆、香港、台湾、新加坡、马来西亚在内的 25 个亚洲国家或地区的独家商业化权利。依据中国注册法规要求,瑞美吡嗪注射液和动态监测系统分别按照药品和医疗器械申报注册。2022 年 7 月,动态监测系统的医疗器械注册申请获 NMPA 受理。MediBeacon®肾小球滤过率动态监测系统及 MB-102 注射液为全球首创,有望解决上述未被满足的临床需求。肾脏疾病是一个世界性的公共卫生问题。据美国国立糖尿病、消化和肾脏疾病研究所(NIDDK)报告,全球肾病的患病率大约为 13.4%。肾小球滤过率(GFR)是评估肾脏功能的最佳指标之一,也是目前临床对慢性肾脏疾病进行分期的主要量化标准。目前临床使用的肾功能受损或正常患者的肾小球滤过率检测方法存在多种不足之处。首先,公式法要求患者空腹 8 小时抽取血液,因而获得检测结果需较长时间;其次,是通过肾脏 ECT 进行检查,需要借助大型的扫描仪器,场地限制性强。MediBeacon®作为全球首创医疗器械产品,可通过无创监测外源性示踪剂发出的荧光随时间的变化,实现实时、动态、连续的床旁 GFR 监测,突破了现有 GFR 检测方法的时间和空间限制。对肾功能不全相关临床应用场景的诊断和治疗具有突破性的意义,极大地提高了临床肾病检测的效率和便利性。MediBeacon®肾小球滤过率动态监测系统及 MB-102 注射液作为公司研发创新成果获得全球多项认证。美国 FDA 于 2018 年 10 月授予其「突破性医疗器械」认定,给予加速审评审批。2021 年 11 月,该系统获 NMPA 同意,进入创新医疗器械特别审查程序,将按创新医疗器械进行注册审评审批。此外,MediBeacon 公司也向美国 FDA 递交 MediBeacon®肾小球滤过率动态监测系统的上市申请,并于 2023 年 7 月正式受理,有望于 2024 年上半年获批。深耕全球研发生态圈,全面布局优势显现近年来,华东医药通过自主开发、外部引进、项目合作等方式重点在肿瘤、内分泌和自身免疫三大核心治疗领域的创新药及高技术壁垒仿制药进行研发布局。公司在抗肿瘤、内分泌和自身免疫三大核心治疗领域均已有全球首创新药(first-in-class)布局,在肿瘤 ADC 药物领域已形成多个全球创新药物布局和研发生态圈搭建,形成差异化优势。从具体业务板块来看,华东医药逐步拓展肿瘤、内分泌、免疫三大领域布局的深度与广度,纵向深耕慢病治疗领域,横向丰富创新药研发管线布局。同时,华东医药不断强化全球创新研发生态圈和技术平台建设,积极推进临床试验工作进度,取得了多项重大阶段性成果。华东医药近日发布的调研记录表,对公司最近的创新动态进行了更新。据介绍,目前,华东医药的创新成果正在有节奏的兑现。创新药方面,公司 2023 年临床推进及注册工作取得多项积极进展,多款产品有望于 2024 年上市或递交上市申请。索米妥昔单抗注射液(ELAHERE®)的上市申请已于 2023 年 10 月获得 NMPA 受理,该产品此前已被纳入优先审评品种名单,有望于 2024 年在国内获批上市。注射用利纳西普(ARCALYST®)用于治疗冷吡啉相关的周期性综合征(CAPS)的上市申请已于 2023 年 11 月获得受理,同时复发性心包炎(RP)适应症上市申请有望于今年递交,两个适应症已被纳入优先审评品种名单。迈华替尼片用于 EGFR 敏感突变的晚期非小细胞肺癌 III 期临床试验已成功达到主要终点,公司预计于今年递交该产品的上市申请。生物类似药方面,乌司奴单抗注射液用于成年中重度斑块状银屑病的上市许可申请已于 2023 年 8 月获得受理。在内分泌领域,围绕 GLP-1 靶点,华东医药已构筑了包括口服、注射剂在内的长效及多靶点全球创新药和生物类似药相结合的全方位和差异化的产品管线。公司在研的 GLP-1 产品中,口服小分子 GLP-1 受体激动剂 HDM1002 片已获得中国和美国的 IND 批准,国内目前处于Ⅰb 期临床阶段;司美格鲁肽注射液糖尿病适应症目前已完成临床Ⅲ期受试者入组,预计年内完成Ⅲ期临床;双靶点激动剂 HDM1005 已递交 IND 申请;长效三靶点激动剂 DR10624 正在中国开展 I 期单次给药剂量递增(SAD)研究,同时在新西兰同步开展 I 期 SAD 和多次给药剂量递增(MAD)试验。华东医药利拉鲁肽注射液是国内首个获批上市的利拉鲁肽生物类似药。截至目前,利拉鲁肽注射液已在超过 800 家大型医院实现入院销售,医院覆盖的数量还在快速增长中,预计到今年一季度末完成超过 1000 家医院的进院覆盖。此外,院外市场也是减肥适应症的主要销售渠道,包括线上平台及线下药店,公司也在积极进行布局。华东医药利拉鲁肽注射液已完成 2 万家终端铺货单体药店覆盖,计划在春节前后完成 3 万家终端铺货单体药店数量的目标。此外,华东医药的医美业务与工业微生物业务都在顺利推进。据调研表显示,华东医药国内及海外医美在去年四季度均取得了较好表现,顺利完成了制定的目标任务。双极射频抗衰设备 Reaction®芮艾瑅®自 2023 年 6 月在国内新上市以来受到了市场广泛关注,客户使用反馈良好,该产品推广团队非常有信心在今年取得更高目标。Ellansé®伊妍仕®将继续做深做细高端再生注射剂市场,也会选择性地拓展新合作机构,目前国内签约合作医院数量超 600 家,培训认证医生数量超 1200 人。工业微生物业务方面,目前华东医药控股公司南农动药已组建一支宠物动保线下品牌专业营销团队,并已经完成全国经销商网络布局。宠物用中枢镇痛药物酒石酸布托啡诺注射液(商品名:保适宁®)已覆盖上百个城市,几千家的宠物医疗机构。此外,萌笛品牌包括宠物用驱虫类产品、皮肤类产品及保健品等 10 个以上产品,目前线上业务处于开拓期,2024 年线上将继续围绕「品牌塑造+产品提升+销量产出」助力业务增长。此次瑞美吡嗪注射液上市申请获受理是该款全球首创产品的开启商业化进程的重要节点。封面来源:企业 Logo免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。编辑:HebePR 稿对接:微信 insightxb投稿:微信 insightxb;邮箱 insight@dxy.cn多样化功能、可溯源数据……Insight 数据库网页版等你体验点击阅读原文,立刻解锁!
突破性疗法加速审批上市批准引进/卖出
2023-11-25
作为目前最热门的药物之一,减肥药的潮流裹挟众多药企纷纷布局GLP-1类药物。国内疫苗龙头智飞生物也不例外。11月23日晚,智飞生物发布公告,与宸安生物、智睿投资、张高峡就智飞生物拟以现金形式收购智睿投资、张高峡持有的宸安生物100%股权达成初步意向,并签署了《股权收购意向性协议》。智飞生物拟通过此次交易,将公司业务版图延伸覆盖至糖尿病、肥胖等代谢类疾病领域,同时公司亦将由此进入治疗性生物制药领域。根据公告介绍,目前宸安生物的减肥药“重组司美格鲁肽注射液”已位于临床III期阶段,研发进度处于国内前列,“口服司美格鲁肽片”则位于临床前阶段。关于宸安生物宸安生物成立于2015年11月4日,法定代表人是蒋凌峰。蒋凌峰系智飞生物实控人、董事长蒋仁生之子,现任智飞生物副董事长、副总经理。据公告介绍,宸安生物是智睿投资平台投资孵化的一家依托于重组蛋白技术平台的生物制药企业,聚焦糖尿病、肥胖等代谢类疾病领域,已形成梯次分明的GLP-1类似药物、胰岛素类似物管线布局。值得注意的是,智睿投资是宸安生物大股东,目前持股比例为85%,而智睿投资则是智飞生物实际控制人蒋仁生和智飞生物共同成立的投资公司,其中蒋仁生持股90%,因此蒋仁生也是宸安生物实控人。以此计算,蒋仁生间接持有宸安生物约77%股权。截至目前,宸安生物拥有6款已进入临床阶段的候选药物,其中重组利拉鲁肽注射液、德谷胰岛素注射液已完成临床III期,位于申报上市阶段;重组司美格鲁肽注射液已位于临床III期阶段。国内药企“抢滩”减肥药2023年上半年,诺和诺德营收增长了近30%,其中司美格鲁肽产品销售额共计92亿美元,同比增长87%。减肥药也帮助诺和诺德成为欧洲市值第一的公司。礼来旗下的GLP-1R/GIPR双重激动剂替尔泊肽也在2023年上半年大卖,实现销售额15.5亿美元,而这只是替尔泊肽仅获批降糖适应症的情况下实现的销量。11月8日,替尔泊肽获得FDA批准上市,帮助礼来市值冲刺6000亿美元。有数据显示,全球减肥药市场规模从2017年的20亿美元增长到2021年的30亿美元,年复合增长率达到10.7%,并且预计将于2025年达到64亿美元,于2030年达到115亿美元。据媒体报道,目前在国内已经有至少八款GLP-1类药物已经获批,还有大量的GLP-1类药物现在处于临床上市的过程当中,其中包括双靶点甚至是三靶点药物。今年7月,华东医药的利拉鲁肽生物类似药(利鲁平)和上海仁会生物的创新药贝那鲁肽两款国产GLP-1类药物获批上市,其中利鲁平是国内首款GLP-1类减肥药。相对肥胖适应症,国内企业在利拉鲁肽生物类似药布局2型糖尿病适应症上尤为激烈,除了已获批上市的华东医药,通化东宝、翰宇药业、正大天晴、联邦生物、健翔生物均已申报上市,并且多家药业也已进入Ⅲ期临床阶段,包括宸安生物、东阳光药业、双鹭药业等。国内司美格鲁肽生物类似药局限在2型糖尿病适应症。其中华东医药、九源基因、丽珠集团均已进入临床Ⅲ期试验,另外宸安生物、联邦生物、齐鲁生物、质态生物、石药集团已进入临床。此外,还有恒瑞医药、信达药业等企业也布局了GLP-1类药物的研究。恒瑞的三款减肥药管线:HRS9531处于Ⅱ期临床、HRS-7535处于Ⅰ期临床、HR17031已进入Ⅲ期临床。信达近日公布了其减肥药玛仕度肽(IBI362)在中国肥胖受试者中的最新II期临床数据。数据显示玛仕度肽在减重效果方面优于此前的司美格鲁肽注射液。中泰国际研报指出,预计玛仕度肽将于2025年下半年起贡献收入,保守预计玛仕度肽到2030年的年销售额将超12亿元。根据中信证券的测算,中国GLP-1受体激动剂类减肥药的市场规模预计在2030年将达到383亿元左右,其中在肥胖人群中的市场规模约为255亿元,在超重人群的市场规模约为129亿元。在代理路上狂奔左拥默沙东,右抱葛兰素史克,智飞生物依靠代理疫苗,业绩迎来节节高升。10月26日,智飞生物披露2023年三季报,前三季度智飞生物共实现营业收入392.72亿元,同比增长41.15%,创历史新高;实现净利润65.30亿元,同比增长16.46%。其中单Q3季度,智飞生物实现营业收入148.26亿元,同比增长56.57%;实现净利润22.70亿元,同比增长20.89%。代理产品业绩的强劲增长,是智飞增收增利的主因。半年报显示,智飞生物上半年代理产品营收235.83亿元,占总营收的比重超过95%。自主产品方面,上半年智飞生物自主产品实现销售8.60亿元,同比下降48.44%。智飞生物表示,表观上自主产品的收入下降,主要源于新冠疫苗的销售量波动。智飞生物的合作伙伴默沙东第二季度财报显示,包含四价和九价在内的HPV疫苗在内的全球销售额达到24.6亿美元,同比增长47%。默沙东称,主要是因为该产品在全球需求的高速增长,尤其是中国市场。在代理产品上尝到甜头的智飞生物,决定在代理的路上一路狂奔。10月8日,智飞生物宣布,其已与GSK(葛兰素史克)签署了《独家经销和联合推协议》,GSK将向智飞生物独家供应重组带状疱疹疫苗,并许可智飞生物根据约定在合作区域内(中国除港澳台以外的地区)营销、推广、进口并经销有关产品。此外,协议还约定GSK将优先在合作区域内任何RSV(呼吸道合胞病毒)老年人疫苗的联合开发和商业化方面成为智飞生物的独家合作伙伴。协议期限为2023年10月8日-2026年12月31日,2024年-2026年,双方约定重组带状疱疹疫苗的最低年度采购金额分别为34.4亿元、68.8亿元和103.2亿元。总结智飞生物营收的九成以上都来自代理产品,曾引发外界担忧。如今布局GLP-1类减肥药,有望充实智飞生物的自主产品管线。参考来源:1.https://finance.sina.com.cn/roll/2023-11-23/doc-imzvreks5508462.shtml2.https://finance.eastmoney.com/a/202311232912950564.html3.http://stock.10jqka.com.cn/20231124/c652505187.shtml4.https://finance.eastmoney.com/a/202311242913447445.html5.https://finance.sina.com.cn/stock/med/2023-11-22/doc-imzvnzms6459723.shtml6.https://mp.weixin.qq.com/s/4fvNv1EJVXMiCnZm6X7ISw7.https://mp.weixin.qq.com/s/o6sWT8ClOxotCEn1WD3yNg8.https://mp.weixin.qq.com/s/AV55iRj2eZl66DkZlGn-_Q本周好文推荐如需转载请联系佰傲谷并在醒目位置注明出处﹀···
临床3期生物类似药并购疫苗上市批准
2023-11-21
在信达生物公布的2023年Q3业绩中,第三季度取得产品收入超16亿元,同比大增45%,加上今年上半年实现的24.6亿元产品收入,今年前三季度实现总产品收入达约41亿元。如此亮眼的成绩单,“黄金大单品”信迪利单抗功不可没,但要想实现“5年200亿元营收”的目标,还远远不够。那么,继PD-1单抗之后,信达生物的下一张王牌又是什么?商业化产品增至10款信迪利单抗贡献半壁江山对于一家Biotech而言,迈向Biopharma的最优路径,就是既要打造出“黄金大单品”,也要拥有更多的商业化产品。由信达和礼来合作研发的信迪利单抗,无疑是信达生物的“黄金大单品”。凭借已在中国获批的7项适应症和五大高发瘤种一线治疗的优势,今年前三季度信迪利单抗实现销售收入2.8亿美元(约合人民币19.67亿元,按平均汇率1美元=7.0249元换算),同比增长19%;其中Q3销售收入1.2亿美元,同比增长50%。按照信达生物今年前三季度实现约41亿元的总产品收入,信迪利单抗占了总产品收入的一半,贡献了半壁江山。为了应对PD-1单抗市场的激烈竞争和拓宽更大的市场空间,信达仍在不断扩大信迪利单抗的适应症范围,正在进行超过20多个临床研究(其中10多项是注册临床试验),包括与公司其他肿瘤管线药物进行联用的开发,组成多款商业化组合。信迪利单抗获批适应症及临床管线图片来源:东北证券从商业化表现看,目前信达共有10款药物获批上市(包括8款肿瘤药物和2款自免/代谢药物),除了“黄金大单品”信迪利单抗外,其他9款商业化产品的稳健增长,也是信达实现亏损不断收窄的重要动力。据2023年半年报显示,截止6月30日,信达生物期内亏损1.39亿元,同比大幅收窄85.4%,离扭亏为盈只差临门一脚。值得一提的是,信达生物在2022年提出了“未来五年达到200亿元产品收入”的目标。在此前举办的2023年上半年业绩报告会上,信达再次强调这一目标没有改变。正如前文所言,获批更多的商业化产品是Biotech迈向Biopharma的最优路径。如今信达生物已成功迈向Biopharma,而要想实现目标并进一步成长为Big pharma,下一张王牌至关重要。从管线进度看,非肿瘤领域将是信达的一大看点,其中已获批上市的PCSK9降脂药物托莱西单抗和已处于III期临床的减肥药玛仕度肽,被寄予下一张王牌的厚望。托莱西单抗能否成为“下一张王牌”?作为国产首款新型降脂药,托莱西单抗于今年8月获批上市,是信达生物的第10款商业化产品,也是公司首款心血管及代谢(CVM)领域产品,用于治疗成人原发性高胆固醇血症和混合型血脂异常。托莱西单抗之所以被寄予厚望,主要体现在市场潜力大和疗效优异两个方面,但要想成为“下一张王牌”,却并不轻松。据公开数据显示,目前我国有接近1亿人患有高胆固醇血症,超过4亿人群患有血脂异常,患者人数相当庞大。加之,市面上主流的降脂类药物(他汀类药物、胆固醇吸收抑制剂)又都存在各自的缺陷,存在较大的临床未满足需求。从市场潜力看,我国高胆固醇血症药物市场规模超过200亿元。根据弗若斯特沙利文数据,2019年中国PCSK9抑制剂市场规模约为0.3亿元,预计2023年中国市场有望突破10亿元,2030年可达90亿元。PCSK9抑制剂有着比传统他汀类药物更高效(降脂作用更强)、更安全的优势,由此成为了降脂药物新星。根据Ⅲ期临床结果显示,高胆固醇血症患者在服用托莱西单抗12周后,LDL-C水平显著下降,降幅高达68.9%,展现出了不俗的疗效。不过,虽然托莱西单抗是国产首个获批的PCSK9抑制剂,却面临着激烈的市场竞争。目前除了信达以外,国内还有3款同类竞品已获批上市,包括安进的依洛尤单抗、赛诺菲的阿利西尤单抗、诺华的siRNA药物Inclisiran,其中前两款已纳入医保,在国内市场的占比分别约为80%、20%。此外,国内还有3款PCSK9抑制剂于今年密集提交了上市申请,包括君实生物的JS-002、康方生物的伊努西单抗和恒瑞医药的SHR-1209。国内上市/申请上市PCSK9抑制剂进度 数据来源:东北证券孰优孰劣,对比便知。在LDL-C降幅方面,四款PCSK9抑制剂的效果相差无几,其中托莱西单抗降幅效果稍胜一筹,但Inclisiran更长效,持续用药3年疗效无变化。在患者依从性方面,依洛尤单抗、阿利西尤单抗是两周一次或一月一次给药,托莱西单抗则提供了2周、4周、6周三种治疗间隔的灵活用药方案,而Inclisiran首次给药后间隔3个月给药一次,之后每半年打一针,依从性优势最好。由于各个产品在疗效和安全性差异化较小,定价策略就成为了决定销售峰值的重要因素。依洛尤单抗未纳入医保前的价格为1300元/针,按每月注射给药2次计算,年治疗费用为3万多元,纳入医保后价格降至300元左右,年费用在7000元左右。而托莱西单抗的定价为1388元/针,按每6周注射一次给药,一年注射8次,年费用1万左右。但由于托莱西单抗是在今年8月获批,无缘参加2023年医保谈判,明年大概率会与率先提交NDA的君实生物同台竞技2024年医保谈判。综上可见,托莱西单抗面临着不小的压力,就看信达生物能否将其打造成“下一张王牌”。玛仕度肽能否乘上减肥药的“东风”?除现有产品外,后续管线将是撑起信达生物未来业绩的重要基石。目前,信达已建立起一条拥有35种高价值产品管线的雄厚在研管线,覆盖肿瘤、心血管及代谢、自身免疫、眼科等多个重大疾病领域,其中有7个新药分子进入III期或关键性临床研究,另外约20个新药品种已进入临床阶段。在这里面,踩中减肥药风口的玛仕度肽(IBI362),将有望成为信达的“下一张王牌”。今年9月,信达生物就发布了一则拟配售新股筹资23.56亿港元的公告,其中将约30%筹资用于玛氏度肽的开发、营销及商业化等工作,足见其重视程度。减肥药市场有多火爆,看看礼来、诺和诺德的业绩和市值双双暴涨就知道。此前摩根大通给出了最新销售预测,预计到2030年全球GLP-1类减肥药市场规模将超过1000亿美元。而根据中信证券研报显示,2030年中国GLP-1类减肥药的市场规模将达到383亿元左右。玛仕度肽是信达生物从礼来引进的GLP-1R/GCGR双靶点激动剂,仅有国内市场的开发权益,目前针对2型糖尿病和肥胖的适应症已处于Ⅲ期临床,预计将在2023年末至2024年初提交治疗肥胖的上市申请,有望成为首个国产减重GCGR/GLP-1R双靶点创新药。竞争格局方面,目前国内获批上市的国产GLP-1减肥药仅有华东医药的利拉鲁肽生物类似药和仁会生物的贝那鲁肽,礼来的替尔泊肽(Tirzepatide)用于成人减重的上市申请也于今年8月获得了NMPA受理。对比来看,利拉鲁肽和贝那鲁肽都属于GLP-1单靶点药物,而玛仕度肽属于GLP-1R/GCGR双靶点激动剂,在减肥效果上更优,具备成为BIC的国内“重磅炸弹”潜质。根据II期临床结果显示,玛仕度肽9mg用药24周后,体重降幅可达15.4%,成为全球首个在24周内体重较安慰剂降幅突破15%的GLP-1RA双靶点注射剂。另外,在治疗48周后,玛仕度肽9mg组体重较基线的平均百分比变化与安慰剂组的治疗差值达-18.6%,平均变化值达17.8kg;有51.2%的受试者体重较基线下降15%以上,34.9%的受试者体重较基线下降20%以上。这意味着,玛仕度肽的减重效果已经超越诺和诺德的司美格鲁肽。根据东北证券预测,玛仕度肽将在2025年实现20亿元收入。结语现阶段,信迪利单抗仍是贡献信达生物营收的王牌产品,但其他产品也在不断发力。与此同时,信达也布局了丰富的研发管线,投身下一个能贡献增量业绩的王牌产品。如今距离实现“5年200亿元营收”的目标还有几年的时间,就看信达生物能否交出满意的答卷。参考资料1.信达生物财报、公告、官网、官微2.《信达生物-1801.HK-深度报告:日异月新,大有可为》,东北证券3.国信证券、中信建投证券研报
财报临床3期上市批准医药出海
100 项与 利拉鲁肽生物类似药(万邦生化) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 糖尿病 | 临床3期 | 中国 | 2023-01-30 | |
| 肥胖 | 临床3期 | 中国 | 2020-08-07 | |
| 2型糖尿病 | 临床3期 | 中国 | 2020-08-03 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
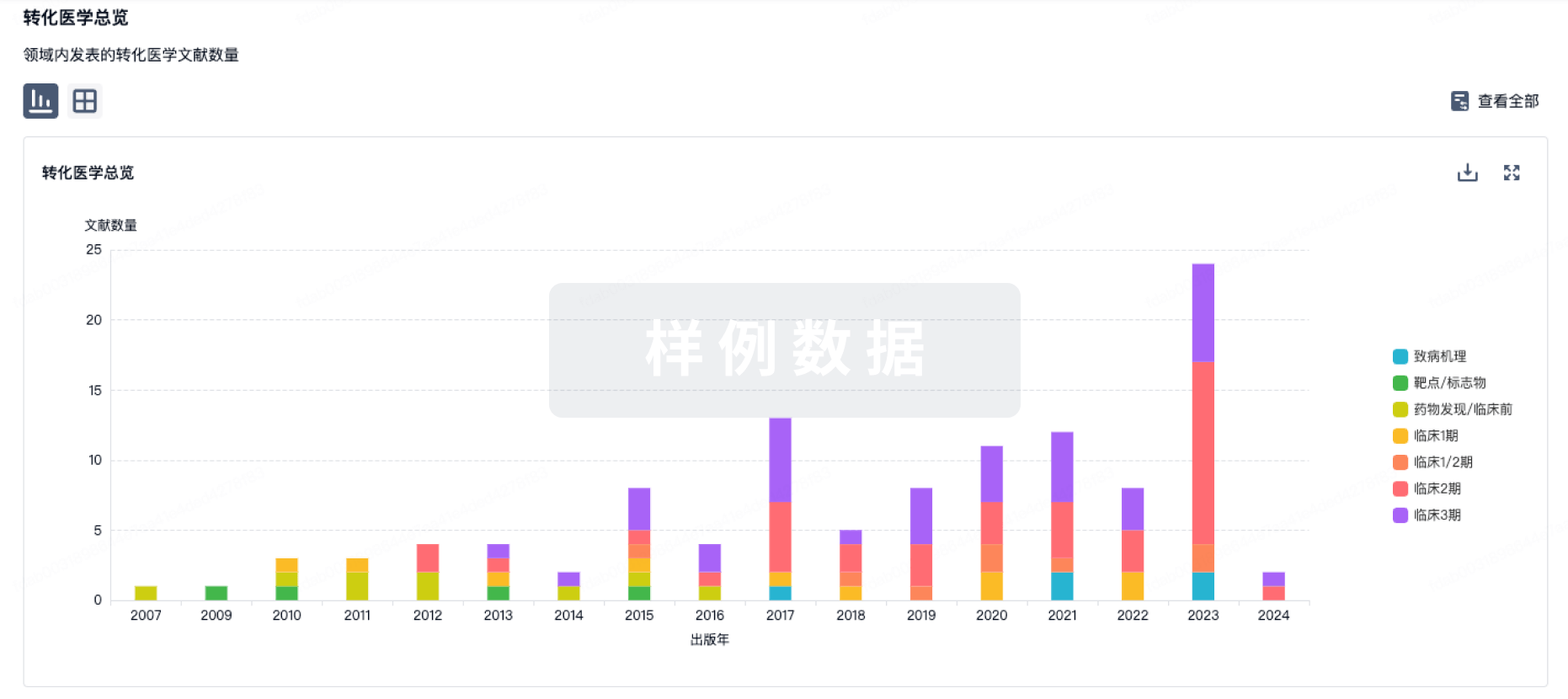
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
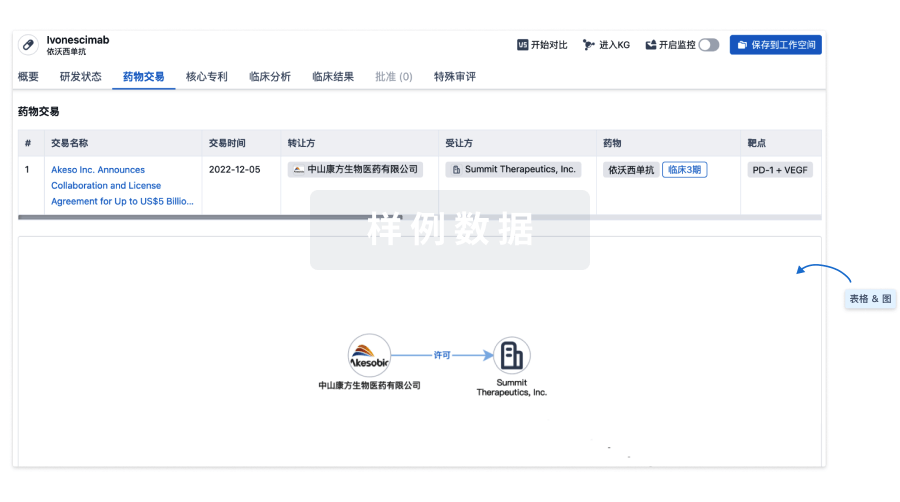
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
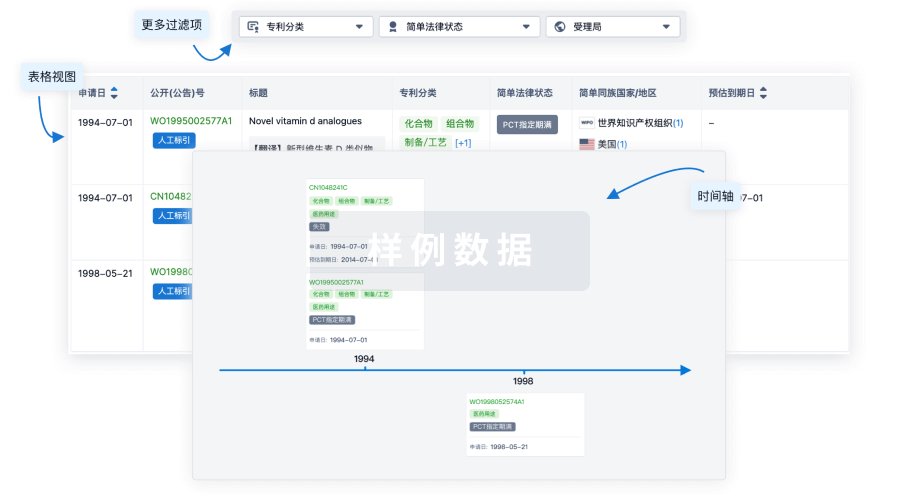
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
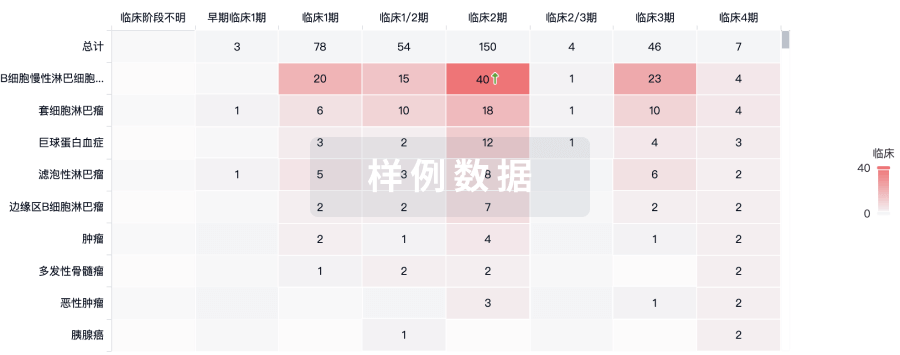
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
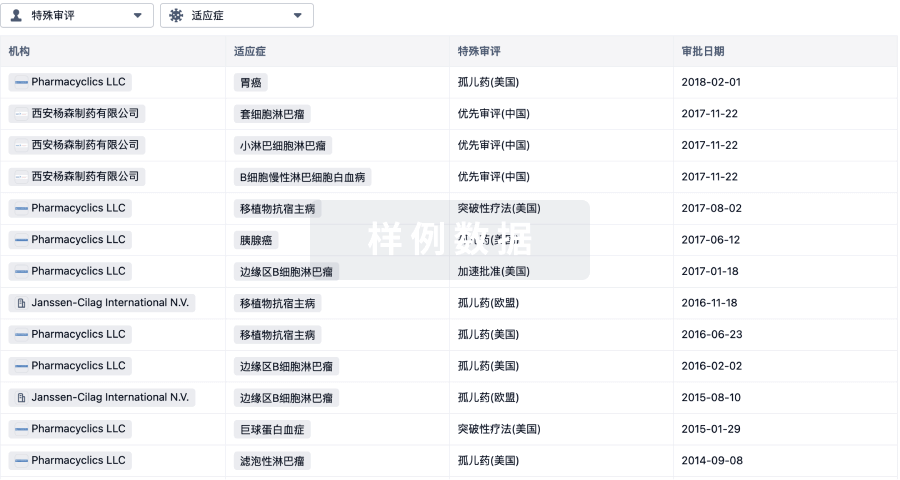
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


