更新于:2024-06-20
CFTR (Vanda Pharmaceuticals)
更新于:2024-06-20
概要
基本信息
药物类型 小分子化药 |
别名- |
靶点- |
作用机制- |
治疗领域- |
在研适应症- |
非在研适应症- |
在研机构- |
最高研发阶段无进展临床1/2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 CFTR (Vanda Pharmaceuticals) 相关的临床结果
登录后查看更多信息
100 项与 CFTR (Vanda Pharmaceuticals) 相关的转化医学
登录后查看更多信息
100 项与 CFTR (Vanda Pharmaceuticals) 相关的专利(医药)
登录后查看更多信息
7
项与 CFTR (Vanda Pharmaceuticals) 相关的新闻(医药)2024-06-14
·奇点网
*仅供医学专业人士阅读参考
肺直接接触外部的“恶劣”环境,具备了超强的防御机制,可有效清除各种颗粒物和病原体。
但这也为经由气道的治疗带来了阻碍。理论上来说,由CFTR单基因失活突变导致的囊性纤维化(CF)非常适合基因治疗,但超过27项基因疗法都未能突破坚固的肺屏障而败走。
今日,《科学》杂志发表了来自德克萨斯大学西南医学中心科学团队的论文,研究者们这次“绕道而行”,选择从静脉给药,从基底膜一侧进入肺部,并在囊性纤维化小鼠中成功实现了体内编辑。
研究者使用了选择性肺靶向脂质纳米颗粒(lung SORT LNP),通过LNP组分优化避免了LNP在肝脏中的聚集。实验中,基因编辑成功矫正了小鼠肺干细胞中50%的CFTRR553X突变,有效增加了功能正常的CFTR水平。
论文题图
研究者首先测试了这种基因编辑方法的持久性,给小鼠静脉注射LNP,2mg/kg间隔48小时注射两次,随后定期收集肺组织进行分析。
lung SORT LNP的效果相当持久,在实验第660天仍旧能够观察到很高的编辑率。分析结果可见,第二次注射后,已经有超过32%的肺细胞被编辑,在第7天上升到51%,并持续至实验结束。
编辑效果可持续长达22个月
基因编辑也基本覆盖了小鼠肺部的主要细胞,包括内皮细胞、上皮细胞、免疫细胞和干细胞在内的多种细胞类型。
660天时,内皮细胞编辑率>93%,免疫细胞>23%、上皮细胞>48%。
而在干细胞中,以NGFR为标志物,编辑率在实验第2天达到28%,180天时升高至75%,660天时仍能维持在45%到70%;以KRT5为标志物,编辑率在第2天达到27%,120天达到峰值97%,660天时维持在45%到80%。
在干细胞中能够维持不错的编辑效率
lung SORT LNP的安全性也很不错,在240天时检测,小鼠肾和肝功能正常,心脏、脾脏未见组织损伤。
研究者分析LNP转运机制发现,玻连蛋白会在LNP外形成类似斗篷的结构,使其更容易被有相应受体VtnR的细胞吸收,这也避免了LNP被免疫系统清除,有效地提高了编辑效率。
肺部各种细胞类型中VtnR表达比例都不低
接下来,研究者尝试了lung SORT LNP对囊性纤维化的治疗效果,目标是通过ABE将目前无法治疗的CFTR无义突变CFTRR553X编辑为野生型CFTR。
在人类囊性纤维化患者支气管上皮细胞中,LNP-ABE实现了约60%的编辑效率,成熟CFTR表达增加了5.5倍。将LNP-ABE与F508del突变患者的标准疗法联合使用,可将CFTR表达进一步增加至7.8倍。
基因编辑联合药物效果更佳
在人源化CFTRR553X突变小鼠中,1.5mg/kg的LNP-ABE静脉注射治疗10天后,可见肺干细胞中编辑率约50%,肺细胞总编辑率12.2%。
在小鼠中完成了体内编辑
这一比例看似不高,但已经足以带来有希望的临床增益。此前有研究结果表明,10-20%的CFTR表达细胞已经足以维持机体所需CFTR功能,相关临床试验设计目标为将CFTR功能提升至野生型的10%;就基因编辑来说,有研究证实,肺干细胞编辑率达到1.5%就足以起到治疗效果。
不过,小鼠并不具有相应的囊性纤维化表型,在更好的动物模型中进行实验,以确定疗效和安全性是必须的。
参考资料:
[1]https://www-science-org.libproxy1.nus.edu.sg/doi/10.1126/science.adk9428
[2]https://www-science-org.libproxy1.nus.edu.sg/doi/10.1126/science.adq0059
本文作者丨代丝雨
基因疗法临床研究临床结果
2024-05-29
·生物探索
引言囊性纤维化跨膜传导调节因子(CFTR)是一个重要的离子通道,其功能丧失导致囊性纤维化,而其过度激活导致分泌性腹泻。改善CFTR折叠(校正剂)或功能(增强剂)的小分子在临床上可用。然而,唯一的增强剂ivacaftor具有次优的药代动力学,抑制剂尚未临床开发。2024年5月28日,洛克菲勒大学陈珏等团队合作在Cell 在线发表题为“Structure-based discovery of CFTR potentiators and inhibitors”的研究论文,该研究结合分子对接、电生理学、冷冻电镜和药物化学来鉴定CFTR调节剂。该研究将约1.55亿个分子对接到CFTR上的增效剂位点,合成了53个测试配体,并使用基于结构的优化来鉴定候选调节剂。这种方法发现了中纳摩尔的增强剂,以及抑制剂,结合到相同的变构位点。这些分子代表了开发更有效的囊性纤维化和分泌性腹泻药物的潜在线索,证明了离子通道药物发现大规模对接的可行性。囊性纤维化跨膜传导调节剂(CFTR)是一种阴离子通道,广泛表达于肺、肠、胰腺和生殖道上皮细胞中,在这些细胞中调节盐和液体稳态。破坏CFTR生物合成、折叠、运输或离子渗透的突变会导致囊性纤维化(CF),这是一种无法治愈的致命遗传疾病。此外,获得性CFTR功能障碍(例如,通过吸烟)在慢性阻塞性肺疾病(COPD)的发生和发展中起着重要作用。另一方面,霍乱弧菌和产肠毒素大肠杆菌等细菌病原体对CFTR的过度激活会导致分泌性腹泻,这是5岁以下儿童死亡的主要原因。CFTR的过度活跃也是常染色体显性多囊肾病(ADPKD)发病的关键驱动因素。由于这些原因,上调或下调CFTR活性的调节剂长期以来一直被视为候选药物。虽然负CFTR调节剂尚未应用于临床,但正调节剂的开发已经取得了相当大的进展,包括增加细胞表面CFTR丰度的校正剂和增强阴离子通量的增强剂。到目前为止,已经为CF患者提供了一个增强器(ivacaftor或VX-770),两个校正器(lumacaftor, tezacaftor)和一个双活性增强器和校正器(eleexacaftor)。Ivacaftor适用于178种不同的CFTR突变,可以单独使用,也可以与校正剂联合使用。虽然它确实改善了许多CF患者的健康,但它的物理性质和药代动力学远未达到最佳。Ivacaftor水溶性低(<0.05 μg/mL;cLogP = 5.6)。此外,其生物利用度变化很大,99%与血浆蛋白结合;由于副作用,包括肝病和儿童白内障,它的使用受到限制。为了降低ivacaftor的每日剂量,目前正在进行新的研究,以评估其氘化版本VX-561。与此同时,该药的高昂费用(每年超过20万美元)对公共健康保险造成了压力,使许多人买不起该药。因此,替代CFTR增强剂,包括受ivacaftor启发的CFTR增强剂,将对CF患者有益。电生理测量表明,ivacaftor增加了许多突变体以及野生型(WT)、CFTR通道的打开概率。WT、ΔF508和G551D CFTR的Cryo-EM结构显示,ivacaftor与所有三种CFTR变体在同一位点结合,靠近一个对门控重要的铰链区域。结合位点不与致病突变如ΔF508或G551D的位置重叠,表明ivacaftor是一种变弹性调节剂。一种化学性质不同的CFTR增强剂GLPG1837与CFTR上的相同位点结合,表明该结合袋是调节配体的热点。由于该口袋是CFTR独有的,并且在密切相关的蛋白质中不保守,因此它是发现CFTR调节剂的极好靶标,具有最小的脱靶效应。模式图(Credit: Cell)由于化学文库用于分子对接的最新发展,现在可以通过计算筛选大型和最近的超大型化学文库来识别潜在的配体。例如,通过基于结构的虚拟筛选,已经确定了多巴胺D4、褪黑激素MT1、sigma2和alpha2a肾上腺素能受体的纳摩尔和亚纳摩尔配体。到目前为止,大多数大型文库筛选都集中在酶和G蛋白偶联受体(GPCRs)上。对膜转运体或离子通道的研究很少。此外,CFTR中的电位结合位点很浅,直接暴露在膜上,这给虚拟筛选带来了额外的挑战。该研究试图通过迭代分子对接、电生理学、冷冻电镜(cryo-EM)和药物化学的努力来鉴定CFTR配体。利用CFTR与ivacaftor配合物的结构,对一个包含多种化学支架的大型虚拟库进行了计算对接。通过迭代优化,该研究确定了一种具有中纳摩尔亲和力的增强剂支架,它在化学上与已知的CFTR增强剂不同,具有良好的物理性质和药代动力学。该研究还发现了与增强位点结合但抑制CFTR活性的调节剂,这表明可以探索膜暴露的变构位点来下调CFTR活性。原文链接https://www-cell-com.libproxy1.nus.edu.sg/cell/fulltext/S0092-8674(24)00472-0#%20责编|探索君排版|探索君文章来源|“iNature”End往期精选围观一文读透细胞死亡(Cell Death) | 24年Cell重磅综述(长文收藏版)热文Nature | 破除传统:为何我们需要重新思考肿瘤的命名方式热文Nature | 2024年值得关注的七项技术热文Nature | 自身免疫性疾病能被治愈吗?科学家们终于看到了希望热文CRISPR技术进化史 | 24年Cell综述
2024-04-09
·药研发
SARS-CoV-2感染破坏上皮屏障并引发气道炎症。冠状病毒的核心毒力结构成分包膜(E)蛋白可能在这一过程中发挥作用。病原体可能通过破坏囊性纤维化跨膜传导调节剂(CFTR)来干扰Cl-的经上皮转运,CFTR调节核因子κB (NF-κB)信号。然而,SARS-CoV-2 E蛋白对气道上皮屏障功能、Cl−转运和强烈炎症反应的病理影响仍有待阐明。2024年3月25日,广州医科大学钟南山团队在Signal Transduction and Targeted Therapy(IF=39)在线发表题为”SARS-CoV-2 envelope protein impairs airway epithelial barrier function and exacerbates airway inflammation via increased intracellular Cl− concentration“的研究论文,该研究证明了E蛋白下调紧密连接蛋白的表达,导致气道上皮屏障的破坏。E蛋白通过上调气道上皮细胞磷酸二酯酶4D (PDE4D)表达,激活Toll样受体(TLR) 2/4和下游c-Jun N末端激酶(JNK)信号,导致细胞内Cl−浓度([Cl−]i)升高。这种升高的[Cl−]i通过促进血清/糖皮质激素调节激酶1 (SGK1)的磷酸化而导致气道炎症加剧。此外,阻断SGK1或PDE4可减轻E蛋白诱导的强烈炎症反应。总的来说,这些发现为SARS-CoV-2 E蛋白在SARS-CoV-2感染期间气道上皮损伤和持续气道炎症中的致病作用提供了新的见解。SARS-CoV-2是导致COVID-19大流行的病原体,对全球公共卫生构成了重大挑战。SARS-CoV-2可能破坏肺泡上皮屏障,引发气道炎症加剧,导致呼吸困难,严重时进展为急性呼吸衰竭。然而,上皮屏障功能破坏和炎症增强的确切分子机制尚不完全清楚。了解SARS-CoV-2的致病机制有助于确定临床干预的新靶点。SARS-CoV-2是一种包膜病毒,具有正义单链RNA基因组。该病毒可破坏上皮细胞的完整性,加剧呼吸道上皮细胞的炎症,这是抵御病毒感染的第一道防线。SARS-CoV-2编码四种结构蛋白——刺突蛋白(S)、包膜蛋白(E)、膜蛋白(M)和核衣壳蛋白(N)。S蛋白介导病毒与宿主受体血管紧张素转换酶2 (ACE2)的结合和病毒与细胞膜的融合。M蛋白在病毒组装中起着至关重要的作用,而N蛋白对病毒基因组的包装和存活至关重要。值得注意的是,E蛋白是一种核心结构毒力因子,在维持病毒生命周期(如病毒组装)中起着至关重要的作用。一些研究探索了SARS-CoV-2 S、M和N蛋白的致病作用。然而,SARS-CoV-2 E蛋白在上皮紧密连接和粘膜炎症中的作用和机制尚不清楚。气道屏障由紧密连接、纤毛粘液清除和免疫细胞组成。紧密连接是由claudin家族跨膜蛋白组成的超分子实体,通过含有支架蛋白的细胞质PDZ结构域与肌动蛋白细胞骨架相连。紧密连接通过维持粘膜单层的完整性和细胞极性,建立物理屏障,调节分子的细胞旁通透性,调节先天免疫。然而,在呼吸道病毒感染期间,由于紧密连接蛋白的表达失调,屏障功能可能受损,导致入侵的病原体进入上皮下间隙。先前的研究表明,SARS-CoV-2的高病毒载量可破坏气道上皮紧密连接,部分涉及与Lin-7-1相关蛋白(PALS1)的相互作用。此外,SARS-CoV-2 E蛋白还可能与紧密连接蛋白zona occluden-1 (ZO-1)相互作用,导致上皮紧密连接损伤。这些观察结果表明,SARS-CoV-2 E蛋白在触发上皮屏障功能障碍中起关键作用。纤毛粘膜清除在维持气道微环境的稳态,确保有效清除入侵病原体方面起着至关重要的作用。纤毛黏液清除的有效性部分取决于水和离子运输的动力学。氯离子(Cl−)是人体内的主要阴离子,细胞内的Cl−浓度([Cl−]i)受到多种Cl−通道和转运体的严格调控。最近的证据表明,细胞内Cl-可能调节信号,细胞内Cl-稳态的破坏可能与多种细胞功能的改变有关,如炎症和免疫紊乱。文章模式图(图源自Signal Transduction and Targeted Therapy )因此,细胞内Cl−的积累可能在病原体(如病毒)感染后持续气道炎症的放大中发挥重要作用。囊性纤维化跨膜传导调节剂(CFTR)是一种3',5' -环单磷酸盐(cAMP)激活的Cl-通道,表达于全身上皮细胞的顶端膜。在上皮细胞中,各种病原体的感染可导致CFTR表达降低或功能障碍,导致阴离子分泌受损,细胞内Cl−失衡。有趣的是,CFTR和TMEM16介导的Cl-外排参与了SARS-CoV-2的进入和复制,这表明细胞内Cl-信号在SARS-CoV-2感染过程中发挥了作用。Toll样受体(TLRs)是一种模式识别受体(PRRs),通过识别病原体相关分子模式(PAMPs)在感染过程中启动炎症反应和先天防御反应。研究证实TLR2能够识别SARS-CoV-2的S蛋白和E蛋白,在COVID-19的发生发展中发挥了至关重要的作用。丝裂原活化蛋白激酶(MAPK)级联是高度保守的信号分子,负责将细胞外刺激转导为细胞信号。哺乳动物细胞中有三种主要的MAPK通路,包括细胞外信号调节激酶(ERK,也称为p42/p44 MAPK)、c-Jun N-末端激酶(JNK,也称为应激激活蛋白激酶,SAPK)和p38激酶。MAPK通路已被证明可被多种病毒激活,因此是缓解病毒诱导的炎症细胞因子风暴的关键靶点。因此,研究TLR信号通路和MAPK通路在SARS-CoV-2感染过程中的参与可能有助于阐明COVID-19的免疫发病机制,并探索有价值的抗病毒治疗靶点。因此,该研究旨在探讨SARS-CoV-2 E蛋白对气道上皮完整性和炎症反应的病理影响及其潜在机制。参考文献:https://www-nature-com.libproxy1.nus.edu.sg/articles/s41392-024-01753-z来源:iNature
临床结果紧急使用授权临床研究
100 项与 CFTR (Vanda Pharmaceuticals) 相关的药物交易
登录后查看更多信息
研发状态
登录后查看更多信息
临床结果
临床结果
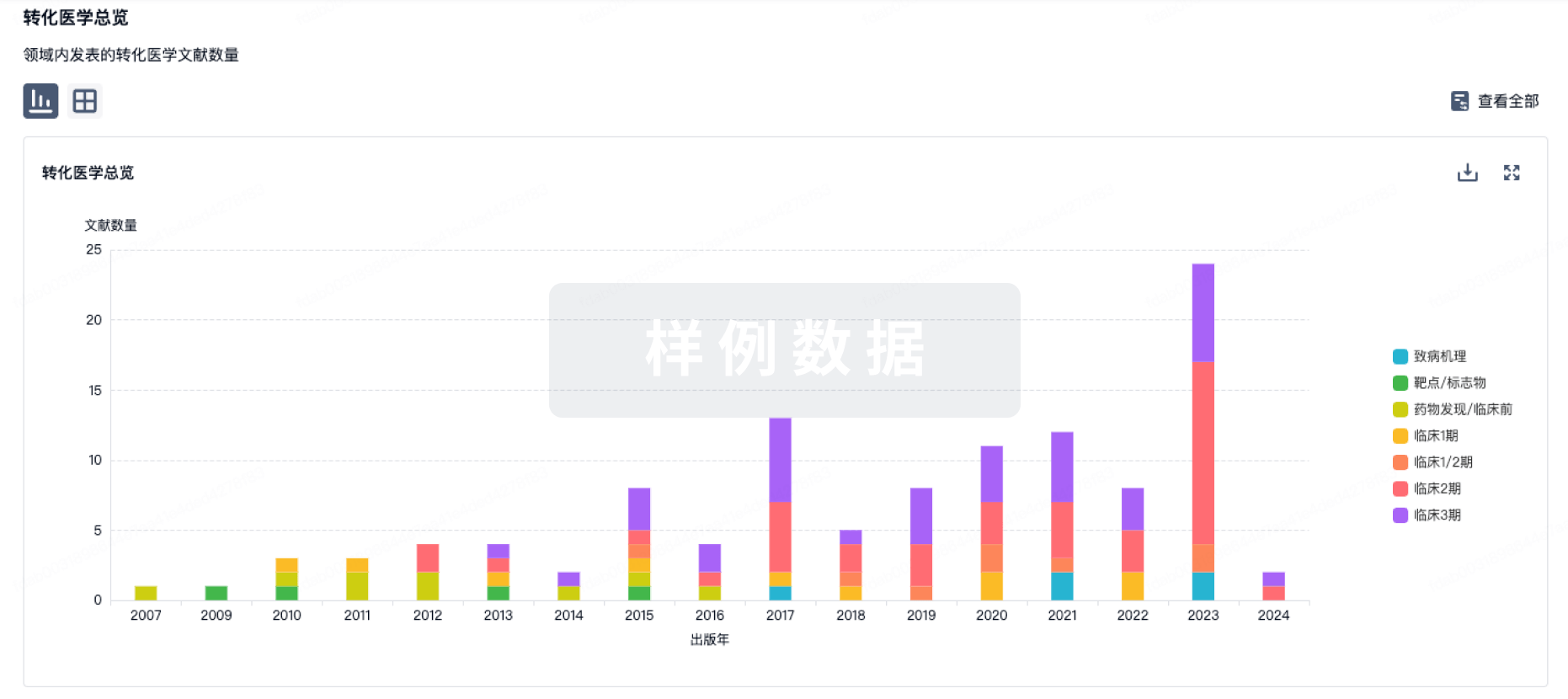
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
